Eliminační reakce
A) Dehydrogenace – radikálová eliminace
Při dehydrogenaci dochází k eliminaci vodíkových atomů ze sousedících uhlíkových atomů po homolytickém rozštěpení chemických vazeb. Probíhá za přítomnosti dehydrogenačních katalyzátorů (např. Ni nebo Pt) při teplotě 200–400 °C. Dehydrogenací vznikají nenasycené uhlovodíky (alkeny, alkadieny, alkyny atd.):
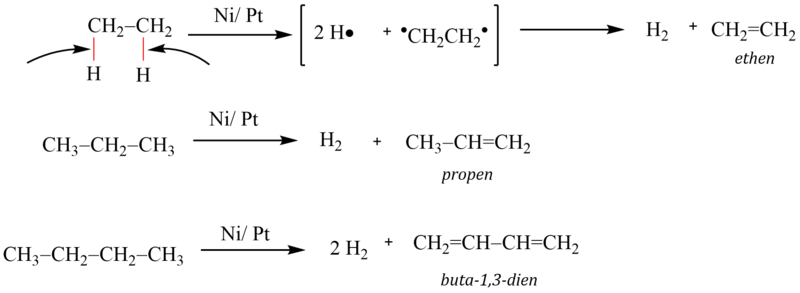
B) Krakování alkanů
Tepelné krakování (z anglického to crack – trhat) je odborný název pro pyrolýzu uhlovodíků. Jedná se o krátkodobé zahřívání uhlovodíků za nepřístupu vzduchu na 400–600 °C. Při vysokých teplotách dochází k odštěpování vodíku, trhání uhlíkových řetězců a následné rekombinaci (izomeraci) vzniklých radikálů. Celý proces má tedy radikálový průběh, protože dochází k homolytickému štěpení vazeb C-C a C-H alkanů.
Hlavními produkty krakování jsou tak nižší a rozvětvené nasycené uhlovodíky a alkeny. Tímto způsobem se zpracovávají výševroucí podíly frakční destilace ropy s cílem vyrobit kvalitní benzíny.
Př. krakování propanu:

Vedle tepelného krakování existuje krakování katalytické. Zde se k rozštěpení molekuly alkanu nepoužívá tak vysokých teplot, ale postačuje zahřívání na nižší teploty v přítomnosti katalyzátorů na bázi zeolitů. Průběh reakce je iontový. Při tomto procesu vznikají hlavně rozvětvené alkany, cykloalkany a aromáty, zatímco zastoupení alkenů je nízké.
V dnešní době se dává přednost katalytickému krakování, které umožňuje vhodným výběrem katalyzátoru ovlivnit výsledné složení reakční směsi.
Izomerace
Izomerací alkanů vznikají řetězové izomery. V praxi je nejdůležitější tvorba alkanů obsažených v benzínu (alkany s šesti až devíti uhlíkovými atomy) s co nejrozvětvenějšími řetězci, tzv. reformování.
Například přesmykem oktanu může vzniknout 2,2,4-trimethylpentan:

- FIKR, Jaroslav a Jaroslav KAHOVEC. Názvosloví organické chemie. Olomouc: Rubico, 2002, ISBN 80-7346-017-3.
- HONZA, Jaroslav a Aleš MAREČEK. Chemie pro čtyřletá gymnázia 2. díl. Olomouc: Nakladatelství Olomouc, 2005, ISBN 80-7182-141-1.
- JANECZKOVÁ, Anna a Pavel KLOUDA. Organická chemie. Ostrava: Nakladatelství Pavel Klouda, 1998, ISBN 80-902155-6-4/9802.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie v kostce II.. Havlíčkův Brod: Fragment, 1997, ISBN 80-7200-342-9.
- PACÁK, Josef. Jak porozumět organické chemii. Praha: Karolinum, 1997, ISBN 80-7184-261-3.
- SVOBODA, Jiří a kol. Organická chemie I. Praha: Vysoká škola chemicko-technologická, 2005, ISBN 80-7080-561-7.
Pokud není uvedeno jinak, autorem obrázků je Mgr. Michal Bezděk.
Eliminace
Eliminace je reakce, při které se ze dvou sousedních uhlíkových atomů v molekule odštěpí atomy nebo skupina atomů, které poskytnou nízkomolekulární produkt a mezi těmito uhlíkovými atomy vznikne násobná vazba nebo se zvyšuje násobnost vazby.
Katalyzátor
Katalyzátor je látka vstupující do chemické reakce, kterou urychluje (nebo zpomaluje), a přitom z ní vystupuje nezměněná.
Význam a základy katalytického krakování
Co se vyrábí z ropy?
Automobilový benzín
Význam a základy reformování benzinů