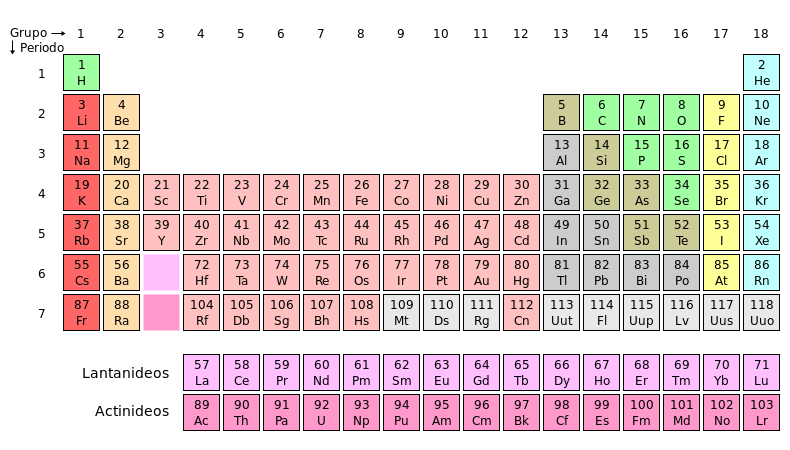
p3 – prvky – pentely
V V. A skupině (15. skupině) se nachází dusík N, fosfor P, arsen As, antimon Sb a bismut Bi.
Mají 5 valenčních elektronů v orbitalech ns a np, jejich elektronová konfigurace ve valenční vrstvě je tedy ns2 np3 . Do stabilní elektronové konfigurace jim chybí 3 elektrony, které mohou získat vytvořením tří kovalentních vazeb nebo vznikem aniontu N3– (P3–), ale to jen ve výjimečných případech, protože je to děj energeticky velmi nevýhodný.
Dusík je maximálně čtyřvazný ( v NH4+ ), ostatní prvky mohou být až pětivazné (ve vzbuzeném stavu).
Ve skupině shora dolů klesá stabilita sloučenin s oxidačním číslem V a roste stabilita sloučenin s oxidačním číslem III.
Ve skupině shora dolů narůstá kovový charakter.
Tab.1: Vlastnosti pentelů
|
Z |
Značka |
Elektronová konfigurace |
Elektrone- gativita |
Teplota tání °C |
Teplota varu °C |
Oxidační číslo |
Vlastnosti |
|
7 |
N |
[He] 2s2 2p3 |
3,0 |
– 210 |
– 196 |
–III, –II, –I I,II,III,IV,V |
plyn |
|
15 |
P |
[Ne] 3s2 3p3 |
2,1 |
44 (bílý) |
280 (bílý) |
– III, III, V |
nekovová pevná látka |
|
33 |
As |
[Ar] 3d10 4s2 4p3 |
2,0 |
|
633* |
– III, III, V |
polokov |
|
51 |
Sb |
[Kr] 4d10 5s2 5p3 |
1,9 |
630 |
1 640 |
(– III), III, V |
polokov |
|
83 |
Bi |
[Xe] 4f14 5d10 6s2 6p3 |
1,9 |
271 |
1 560 |
III, (V) |
kov |
* šedý arsen (sublimuje)
- BENEŠOVÁ, Marika a Hana SATRANOVÁ. Odmaturuj z chemie. 1.vydání. Brno: Didaktis, 2002. 208 s. ISBN 80-86285-56-1.
- DVOŘÁČKOVÁ, Svatava. Rychlokurz chemie. 1. vydání. Olomouc: Rubico, 2000. 238 s. ISBN 80-85839-42-3.
- FLEMR, Vratislav a Bohuslav DUŠEK. Chemie I/Obecná a anorganická. 1. vydání. Praha: SPN, 2001. 120 s. ISBN 80-7235-147-8.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie I v kostce. 1. vydání. Havlíčkův Brod: Fragment, 1996. 120 stran. ISBN 80-7200-056-X.
- ŠRÁMEK, Vratislav a Ludvík KOSINA. Obecná a anorganická chemie. 1. vydání. Olomouc: FIN, 1996. 262 stran. ISBN 80-7182-003-2.
Obrázky
- Obr. 1: Cepheus. commons.wikimedia.org [online]. [cit. 2014-10-17]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Periodic_table_pt.svg?uselang=cs.