Kovy alkalických zemin a jejich sloučeniny
Vlastnosti
| Ca | Sr | Ba | Ra | ||
| Teplota tání [ºC] | 839 | 769 | 725 | 700 | 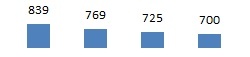 |
| Hustota [g·cm–3] | 1,55 | 2,6 | 3,5 | 5 | 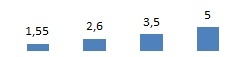 |
| Eº (M2+ / M) [V] | –2,87 | –2,89 | –2,9 | –2,92 | ![Hodnoty standardních redoxních potenciálů [V]](/storage/uploads/images/15035/content_kaz-E0.jpg) |
| Ionizační energie [kJ·mol–1] | 589,6 | 549,2 | 502,7 | 509,1 | 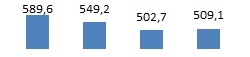 |
Konfigurace valenčních elektronů: ns2, kde n = 4 až 7
Kovy alkalických zemin, tj. vápník (Ca), stroncium (Sr), baryum (Ba) a radium (Ra) jsou stříbrobílé, poměrně měkké kovy (tvrdostí odpovídající olovu).
Z hodnot standardních redoxních potenciálů v tabulce vyplývá, že
-
jsou to kovy neušlechtilé, které snadno odevzdávají své dva valenční elektrony:
M → M2+ + 2 e–, -
v chemických reakcích tak vystupují jako silná redukční činidla,
-
redukční schopnosti se ve skupině s rostoucím protonovým číslem zvyšují.
S těmito závěry korespondují také klesající hodnoty ionizačních energií ve skupině.
Všechny kovy alkalických zemin (podobně jako alkalické kovy) reagují s vodou za vzniku hydroxidu, přitom redukují kationty vodíku na vodík. Reakce však není tak bouřlivá jako u alkalických kovů.
| Obecně: | M + 2 H2O → H2 + M(OH)2 |
| Např.: | Ca + 2 H2O → H2 + Ca(OH)2 |
Výroba
Kovy alkalických zemin se vyrábějí elektrolýzou tavenin solí.
Např. vápník se vyrábí elektrolýzou taveniny chloridu vápenatého. Na grafitové anodě se vylučuje chlor a na železné katodě se redukují vápenaté ionty na vápník.
V elementárním stavu kovy alkalických zemin nenacházejí širšího uplatnění, avšak velký význam mají jejich sloučeniny.
Sloučeniny kovů alkalických zemin
Hydridy kovů alkalických zemin MH2
jsou podvojné sloučeniny s vodíkem, které vznikají mírným zahřátím obou prvků. Jsou to bílé krystalické látky.
Struktura hydridů je iontová s anionty H–.
S vodou bouřlivě reaguji za vzniku vodíku:
MH2 + 2 H2O → 2 H2 + M(OH)2
Jde o reakci synproporcionační:
2 H–I + 2 H+ → 2 H20
Hydrid vápenatý CaH2 se používá jako silné redukční činidlo a také sušidlo (pro svou reaktivitu s vodou).
Halogenidy kovů alkalických zemin MX2
Fluoridy MF2 jsou ve vodě nerozpustné (s rostoucí teplotou rozpustnost roste), tepelně stálé látky, které krystalují ve formě bezvodých solí.

|
| Obr. 1: Minerál fluorit |
Významným zástupcem je fluorid vápenatý CaF2, mineralogicky fluorit (kazivec). Používá se jako surovina pro výrobu sloučenin fluoru.
Ostatní halogenidy jsou na rozdíl od fluoridů ve vodě rozpustné. Z vodných roztoků krystalují halogenidy vápenaté a strontnaté jako hexahydráty a halogenidy barnaté jako dihydráty.
CaCl2 – bezvodý chlorid vápenatý |
 |
Rozpouštěním CaCl2 ve vodě se uvolňuje hydratační teplo.
Použití:
-
je silně hygroskopický a používá se proto jako vysoušedlo,
-
elektrolýzou jeho taveniny se vyrábí kovový vápník.
CaCl2 · 6 H2O hexahydrát chloridu vápenatého |
 |
Rozpouštěním CaCl2 · 6 H2O ve vodě se naopak teplo spotřebovává a vznikající směs se ochlazuje.
Použití:
-
do chladicích směsí (směs ledu a CaCl2 · 6 H2O v poměru 1:1,5 dosahuje teploty –49 ºC),
-
k ochraně sypkých materiálů (např. uhlí) před zamrzáním (30% vodný roztok CaCl2 · 6 H2O tuhne až při teplotě –55 ºC),
-
zimní posyp komunikací (NaCl je účinný do –7 ºC, roztok CaCl2 je účinný do –35 ºC),
-
ve farmacii (infuzní roztoky),
-
v potravinářství (E 509) jako protispékavá látka – zabraňuje tvorbě hrudek v sypkém materiálu.
SrCl2 · 6 H2O – hexahydrát chloridu strontnatého |
 |
Používá se:
 |
| Obr. 2: Zabarvení zábavné pyrotechniky ionty kovů |
-
k výrobě stroncia elektrolýzou taveniny SrCl2,
-
k výrobě dalších strontnatých solí,
-
v zábavní pyrotechnice (barví plamen intenzivně červeně).
BaCl2 · 2 H2O – dihydrát chloridu barnatého |
 |
Dihydrát chloridu barnatého je vysoce toxickou sloučeninou.
Používá se:
-
v analytické chemii k důkazu síranových aniontů: Ba2+ + SO42- → BaSO4 ↓(bílý),
-
při výrobě pigmentů,
-
v zábavní pyrotechnice (barví plamen do zelena).
Acetylidy kovů alkalických zemin MC2
Tyto sloučeniny se vyrábějí zahříváním oxidu kovu s uhlíkem na vysokou teplotu (2000 ºC):
MO + 3 C → MC2 + CO
Jsou to velmi tvrdé látky, které bouřlivě reagují s vodou za vzniku acetylenu (ethynu) a hydroxidu:
MC2 + 2 H2O → H–C ≡ C–H + M(OH)2
Např.:
CaC2 – acetylid vápenatý |
 |
Výroba: V elektrické peci ze směsi CaO a uhlíku: CaO + 3 C → CaC2 + CO
CaCN2 – kyanamid vápenatý |
 |
 |
Strukturní vzorec: N≡C–N2- Ca2+
Výroba: zahřívání acetylidu vápenatého s dusíkem:
CaC2 + N2 → CaCN2 + C
Používá se jako hnojivo v zemědělství
– v půdě se působením vody a bakterií rozkládá na uhličitan vápenatý a amoniak:
CaCN2 + 3 H2O → CaCO3 + 2 NH3
Oxidy kovů alkalických zemin – MO
CaO, SrO, BaO jsou bílé krystalické látky iontového charakteru. Mají vysoké teploty tání (viz graf).
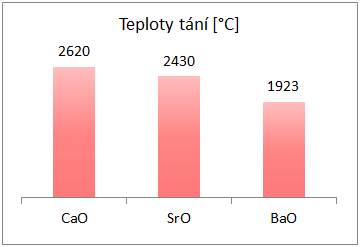 |
| Obr. 3: Graf porovnání teplot tání oxidů kovů alkalických zemin |
Všechny reagují s vodou i vodní párou za vzniku hydroxidů:
MO + H2O → M(OH)2
CaO – Oxid vápenatý (pálené vápno) |
 |
Vyrábí se tepelným rozkladem (pyrolýzou) rozemletého vápence při teplotě asi 900 ºC ve vápenkách:
CaCO3 → CaO + CO2
Tato reakce je vratná, po ochlazení oxid vápenatý váže vzdušný oxid uhličitý.
Pálené vápno má velký význam ve stavebnictví, užívá se ho k výrobě hašeného vápna.
Hydroxidy kovů alkalických zemin – M(OH)2
Vytvářejí silně zásadité vodné roztoky.
Zásaditost hydroxidů roste od Ca(OH)2 (středně silná zásada) k Ba(OH)2 (silná zásada).
Rozpustnost ve vodě ve skupině vzrůstá.
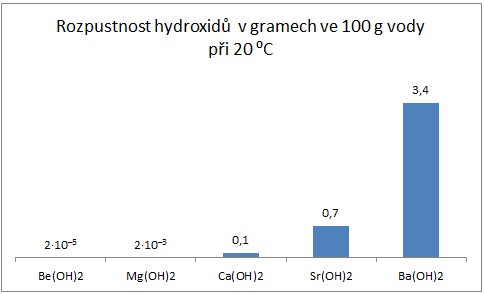 |
| Obr. 4: Porovnání rozpustnosti hydroxidů kovů skupiny II.A |
Ca(OH)2 – hydroxid vápenatý (hašené vápno) |
 |
Hydroxid vápenatý vzniká reakcí CaO (páleného vápna) s vodou – tzv. hašením vápna:
CaO + H2O → Ca(OH)2 ∆H = –67 kJ∙mol-1
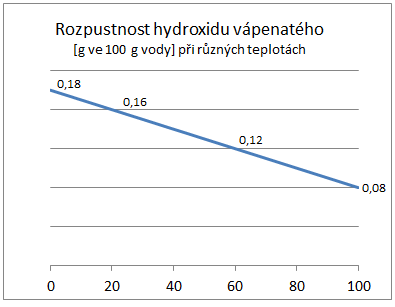
Vzhledem k silně exotermickému průběhu reakce se vždy sype CaO do vody a ne naopak! Při použití malého množství vody může teplota směsi přesáhnout 100 ºC. Protože hydroxid vápenatý má žíravé účinky, je nutné si chránit pokožku a především zrak. Vzhledem k nebezpečí přehřátí a vystříknutí je nutno směs promíchávat. Hydroxid vápenatý je velmi málo rozpustný ve vodě. Patří k těm málo sloučeninám, jejichž rozpustnost se s rostoucí teplotou snižuje.
Rozpustnost hydroxidů strontnatého a barnatého se naopak s rostoucí teplotou zvyšuje.
 |
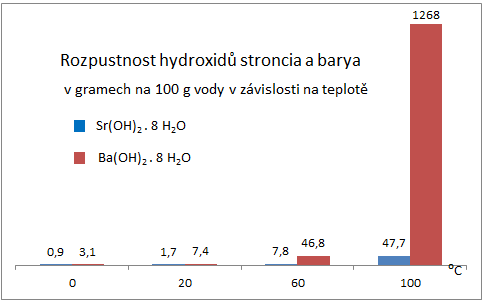 |
| Obr. 5: Graf závislosti rozpustnosti Ca(OH)2 na teplotě | Obr. 6: Porovnání rozpustnosti Ca(OH)2 a Ba(OH)2 |
Vodný roztok hydroxidu vápenatého se nazývá vápenná voda. Používá se k důkazu oxidu uhličitého, který se projeví tvorbou zákalu vznikajícím uhličitanem vápenatým podle rovnice:
Ca(OH)2 + CO2 → CaCO3 + H2O
Suspenze Ca(OH)2 ve vodě je označována jako vápenné mléko nebo vápenná kaše.
Použití:
- ve stavebnictví je součástí malty a omítkových směsí;
podstatou tuhnutí malty (tj. směsi písku, hašeného vápna a vody) je reakce hydroxidu vápenatého se vzdušným oxidem uhličitým za vzniku nerozpustného uhličitanu vápenatého:
Ca(OH)2 + CO2 → CaCO3 + H2O, - k neutralizacím kyselin a výrobě vápenatých solí,
- ve stomatologii v prostředcích s baktericidním účinkem k čištění kořenových kanálků.
Soli kyslíkatých kyselin
Soli kovů alkalických zemin jsou bezbarvé, pokud jejich barevnost není způsobena aniontem (např. žlutý chroman). Na rozdíl od většiny solí alkalických kovů, jsou soli kovů alkalických zemin jako například uhličitany, sírany, fosforečnany a šťavelany, ve vodě nerozpustné.
Uhličitany MCO3
Uhličitany kovů alkalických zemin jsou pevné, ve vodě nerozpustné látky. S vodným roztokem CO2 reagují za vzniku rozpustných hydrogenuhličitanů M(HCO3)2. Hydrogenuhličitany kovů alkalických zemin jsou tepelně nestálé a existují pouze ve formě vodných roztoků.
CaCO3 – uhličitan vápenatý
tvoří dvě krystalové modifikace: vápenec (kalcit) a aragonit.
 |
 |
|
| Obr. 7: Kalcit | Obr. 8: Aragonit |
Používá se k výrobě páleného vápna pyrolýzou:
CaCO3 → CaO + CO2
Další formy a výskyt:
-
mramor – vápenec přeměněný vlivem vysokých teplot a tlaků v zemské kůře (je leštitelný),
-
křída – usazená hornina vzniklá rozpadem vápencových schránek mořských mikroorganismů,
-
islandský vápenec (odrůda kalcitu) – velmi čistý klencový minerál. Vykazuje tzv. dvojlom.
 |
| Obr. 9: Islandský vápenec - dvojlom |
Ca(HCO3)2 – hydrogenuhličitan vápenatý
je rozpustná sůl, která je příčinou přechodné tvrdosti vody spolu s Mg(HCO3)2.
Přechodnou tvrdost vody lze odstranit povařením. Hydrogenuhličitan se rozkládá za vzniku uhličitanu a oxidu uhličitého:
Ca(HCO3)2 ⇄ CaCO3 + CO2 + H2O
Reakce probíhá i zpětně a je podstatou rozpouštění vápence ve vodě s obsahem oxidu uhličitého, např. v místech krasových jevů.
 |
| Obr. 10: Krasová výzdoba Javoříčských jeskyní |
Ca3(PO4)2 – fosforečnan vápenatý (apatit)
Fosforečnan vápenatý je nerozpustný ve vodě. Vyskytuje se ve formách smíšených solí, jako např.:
-
hydroxyapatit – Ca5(PO4)3(OH) – je složkou zubů a kostí,
-
fluorapatit – Ca5(PO4)3F – tvoří se v zubní sklovině působením fluoridu,
-
chlorapatit – Ca5(PO4)3Cl.
Ca(H2PO4)2 – dihydrogenfosforečnan vápenatý
je rozpustný ve vodě a používá se jako hnojivo. Je součástí hnojiva superfosfát.
Rovnice výroby superfosfátu: Ca3(PO4)2 + 2H2SO4 → Ca(H2PO4)2 + 2CaSO4
Sírany MSO4 kovů alkalických zemin
Na rozdíl od síranu beryllnatého a hořečnatého jsou sírany kovů alkalických zemin ve vodě téměř nerozpustné.
CaSO4 · 2 H2O – dihydrát síranu vápenatého (sádrovec)
Při zahřívání nad 100 ºC dochází k částečné dehydrataci a vzniká CaSO4 · ½ H2O, tzv. pálená sádra.
CaSO4 · ½ H2O – hemihydrát síranu vápenatého tzv. pálená sádra
Pálená sádra po smíchání s vodou opět přechází na dihydrát a tuhne, přitom zvětší svůj objem asi o 2 %.
Použití:
-
ve stavebnictví,
-
umění,
-
medicíně,
-
k tvorbě odlitků.
CaSO4 – bezvodý síran vápenatý (anhydrit)
Anhydrit nemá vlastnosti pálené sádry co se týká míchání s vodou. Hydratuje příliš pomalu a nevzniká spleť jehlicovitých krystalů, které dodávají utuhlé sádře pevnost. Pro svou velmi malou teplotní roztažnost však nachází uplatnění jako základ pro samonivelační lité podlahy, které lze aplikovat i na větších plochách bez použití dilatačních spár.
 |
| Obr. 11: Anhydritová litá podlaha |
- BANÝR, Jiří a Renata HŘÍCHOVÁ. Základy anorganické chemie. Praha: Univerzita Karlova v Praze, 1981, 256 s. ISBN 60-69-81.
- GAŽO, Ján a kol. Všeobecná a anorganická chémia. Bratislava: Alfa, 1981, 804 s. ISBN 63-557-81.
- GREENWOOD; EARNSHAW. Chemie prvků. Praha: Informatorium, 1993, 793 s. ISBN 80-85427-38-9.
- JURSÍK, František. Anorganická chemie kovů. Praha: Vysoká škola chemickotechnologická v Praze, 2002, 152 s. ISBN 80-7080-504-8.
- ŠRÁMEK, Vratislav. Chemie obecná a anorganická. Olomouc: Nakladatelství Olomouc, 2000, ISBN 80-7182-099-7.
- Autor neznámý. Termodynamika a termochémia [online]. [cit. 15.1.2015]. Dostupný na WWW: http://www.kmti.szm.com/ch-p5.pdf
- Autor neznámý. Tvrdost vody [online]. [cit. 31.1.2015]. Dostupný na WWW: http://cs.wikipedia.org/wiki/Tvrdost_vody
Obrázky
- Obr. 1: Autor neznámý. http://is.muni.cz/elportal/estud/pedf/js07/mineraly/materialy/mineraly/halogenidy_fluorit.html [online]. [cit. 28.10.2014].
Dostupný na WWW: http://is.muni.cz/elportal/estud/pedf/js07/mineraly/materialy/img/mineraly/big/fluorit1.jpg - Obr. 2: SHIMIN. http://en.wikipedia.org/wiki/Fireworks [online]. [cit. 31.10.2014].
Dostupný na WWW: http://upload.wikimedia.org/wikipedia/commons/thumb/a/a7/ColorfulFireworks.png/1280px-ColorfulFireworks.png - Obr. 7: Autor neznámý. http://cs.wikipedia.org/wiki/Kalcit [online]. [cit. 29.10.2014].
Dostupný na WWW: http://upload.wikimedia.org/wikipedia/commons/thumb/a/a3/Calcit_2.jpg/248px-Calcit_2.jpg - Obr. 8: Autor neznámý. http://cs.wikipedia.org/wiki/Aragonit [online]. [cit. 29.10.2014].
Dostupný na WWW: http://cs.wikipedia.org/wiki/Aragonit#mediaviewer/File:Aragonit_1.jpg - Obr. 9: Autor neznámý. http://www.travelguide.cz/cz/turistika/jeskyne-stoly-a-dulni-expozice/javoricske-jeskyne [online]. [cit. 27.11.2014]. Dostupný na WWW: http://www.travelguide.cz/facilities/tg/full/28-985-2.jpg
- Obr. 10: Autor neznámý. http://kvinta-html.wz.cz/fyzika/optika/vlnova_optika/polarizace_svetla.htm [online]. [cit. 9.11.2014].
Dostupný na WWW: http://kvinta-html.wz.cz/fyzika/optika/vlnova_optika/obrazky/19.jpg
Video:
- Autorem videa "Titrační stanovení tvrdosti vody v ŠPVS" je Jaroslav Svatoň
- Existuje mezi kovy alkalických zemin prvek, který se některou svou vlastností vymyká tendencím ve skupině?
- Jaké znaménko mají hodnoty standardních redoxních potenciálů kovů alkalických zemin?
- Který z kovů alkalických zemin je nejsilnějším redukčním činidlem?
- Hydrid vápenatý je silné činidlo redukční, nebo oxidační?
- Který z halogenidů vápenatých není ve vodě rozpustný?
- Je rozpouštění bezvodého chloridu vápenatého ve vodě exotermický děj? Svou odpověď zdůvodněte.
- Jako součást zimního posypového materiálu se používá bezvodý chlorid vápenatý, nebo jeho hydrát? Odpověď zdůvodněte.
- Hydroxid vápenatý je ve vodě málo rozpustný. Je možné jeho rozpustnost zvýšit zahřátím směsi?
- Co je to vápenné mléko?
- Změní se hmotnost malty po jejím ztuhnutí? Pokud ano, zvýší se hmotnost, nebo dojde k jejímu poklesu?
- Jakou barvou budou zářit ohňostroje obsahující chlorid strontnatý?
- Jakou barvou budou zářit ohňostroje obsahující chlorid barnatý?
- V jakém rozmezí hodnot se má pohybovat celková tvrdost pitné vody, vyjádřená obsahem Ca2+ a Mg2+ v jednotkách mmol·l–1 ?
Jakým způsobem lze posunout rovnováhu ve prospěch produktu u reakcí, kde jedním z produktů je voda?
Příkladem takové reakce je esterifikace:
kyselina + alkohol ⇄ ester + voda
Vyberte vhodnou sloučeninu, jejíž přídavek do soustavy by tento posun rovnováhy zajistil.
Samoohřívací káva
Princip bezplamenného ohřevu nápoje v plechovce spočívá v průběhu exotermické reakce
CaO + H2O → Ca(OH)2 + teplo,
která proběhne v dvojitém dně. Po stlačení dna dojde k promísení oxidu vápenatého s vodou a teplo uvolňované vzájemnou reakcí ohřeje kávu až na 40 ºC.
Titrační stanovení tvrdosti vody v Šumperské provozní vodohospodářské společnosti – ŠPVS
Tvrdost vody je způsobena rozpuštěnými ionty, především vápenatými a hořečnatými. Jejich stanovení lze provést chelatometricky.
Proveďte stanovení tvrdosti vody používané ve vaší obci.
Pro práci lze využít pracovních listů v přílohách.
Tvrdost vody
Tvrdost vody způsobují rozpuštěné soli vápenaté a hořečnaté. Původně se tvrdost vody vyjadřovala ve stupních německých, kde jeden stupeň odpovídá obsahu 10 mg CaO nebo 7,2 mg MgO v jednom litru vody. V současnosti se k vyjádření tvrdosti vody používá celkový obsah vápníku a hořčíku v mmol·l–1.
| Platí, že obsah 1 mmol·l–1 Ca a Mg odpovídá asi 5,6 stupně německého. |
| Voda s tvrdostí do 0,7 mmol·l–1 je velmi měkká, nad 3,75 mmol·l–1 je velmi tvrdá. |
| Pitná voda má mít tvrdost 10–20 stupňů německých. |
| Voda do parních kotlů musí být co nejměkčí, aby nevznikal kotelní kámen. |
Rozlišujeme tvrdost vody přechodnou a trvalou.
Přechodná tvrdost vody neboli karbonátová tvrdost je způsobena rozpuštěnými hydrogenuhličitany: Ca(HCO3)2 a Mg(HCO3)2.
Přechodnou tvrdost lze odstranit povařením. Varem dochází k rozkladu hydrogenuhličitanů na uhličitany, oxid uhličitý a vodu: Ca(HCO3)2 ⇄ CaCO3↓ + CO2 + H2O. Uhličitan vápenatý a hořečnatý jsou nerozpustné, a proto se vyloučí ve formě sraženiny.
Trvalá tvrdost vody neboli nekarbonátová tvrdost je způsobena rozpustnými solemi vápenatými a hořečnatými, které se varem příslušného roztoku nerozkládají. Jde především o rozpuštěné sírany: CaSO4 a MgSO4.
Některé způsoby odstraňování trvalé tvrdosti vody:
- Srážením pomocí CaO a Na2CO3:
MgSO4 + Ca(OH)2 → Mg(OH)2 + CaSO4,
CaSO4 + Na2CO3 → CaCO3 + Na2SO4.
- Změkčováním pomocí ionexů:
Podstatou ionexů jsou syntetické pryskyřice s navázanými ionty, které mohou být ve vodném prostředí disociovány a na jejich místo jsou navázány ionty z původního roztoku. Ionexy se dělí na katexy a anexy.
Katexy obsahují iontově vázaný sodík, popřípadě vodík. Při průchodu tvrdé vody přes katex dochází k uvolnění kationtů Na+, resp. H+ z katexu do vody a navázání kationtů Ca2+ a Mg2+ na katex. Označíme-li hmotu katexu M, lze děj zapsat rovnicí: MNa2 + CaSO4 → MCa + Na2SO4.
Když jsou všechny kationty Na+ z katexu vyčerpány, provádí se regenerace:
MCa + 2 NaCl → MNa2 + CaCl2.
Obdobně lze z vody odstraňovat anionty (SO42–, NO3–, Cl–) jejich záměnou za OH– pomocí anexů.
Úkol:
Nalezněte informace o dalších metodách přípravy čisté vody (reverzní osmóza, využití oxidu grafenu)