Železo, ferrum, 26Fe
Železo je v zemské kůře čtvrtý nejrozšířenější prvek po O, Si, Al. V přírodě se vzácně objevuje ryzí – meteorické, běžné je ve sloučeninách: magnetit (magnetovec) FeO ∙ Fe2O3, hematit (krevel) Fe2O3, limonit (hnědel) Fe2O3 ∙ n H2O, siderit (ocelek) FeCO3, pyrit FeS2 (krychlová soustava), markazit FeS2 (kosočtverečná soustava). Železo (II) je součástí červeného krevního barviva hemoglobinu.
Připravit železo lze redukcí z oxidů například vodíkem:
Fe2O3 + 3 H2 → 2 Fe + 3 H2O
Můžeme použít tepelný rozklad železnatých solí karboxylových kyselin (např. šťavelanu železnatého):
(COO)2Fe → Fe + 2 CO2
Takto získané železo je na vzduchu samozápalné.
Výroba surového železa
Výroba probíhá ve vysoké peci redukcí rud koksem (uhlíkem) při teplotě 1 600 °C - 2 000 °C za přítomnosti struskotvorných přísad (vápenec, dolomit) a vzduchu.
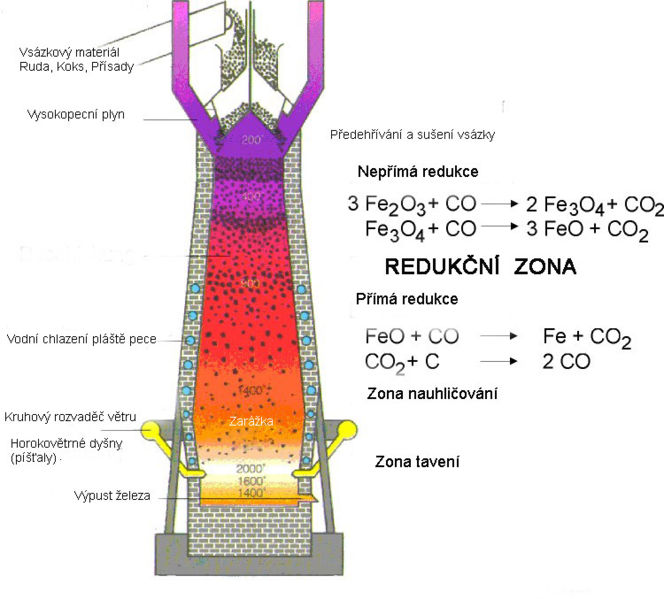
Obr. 1: Schéma vysoké pece
V dolní části pece probíhá hoření koksu:
C + O2 → CO2 Qm = – 393 kJ ∙ mol–1
A přímá redukce:
Fe2O3 + 3 C → 2 Fe + 3 CO
Fe3O4 + 4 C → 3 Fe + 4 CO
FeO + C → Fe + CO
V horní části pece se oxid uhličitý redukuje na oxid uhelnatý:
CO2 + C → 2 CO Qm = 172 kJ ∙ mol–1
A probíhá nepřímá redukce:
3 Fe2O3 + CO → 2 Fe3O4 + CO2
Fe3O4 + CO → 3 FeO + CO2
FeO + CO → Fe + CO2
Surové železo obsahuje příměsi: 3 % - 5 % uhlíku, 2 % křemíku a další prvky, takže není kujné. Ochlazením surového železa vzniká křehká a těžká litina, která se používá k výrobě radiátorů, poklopů na kanály a stojanů.
Z většiny surového železa se vyrábí ocel. Výroba oceli spočívá ve snížení obsahu uhlíku (pod 1,7 %), křemíku, manganu a fosforu oxidací vzdušným kyslíkem. Probíhá v konvertorech s kyselou nebo zásaditou vyzdívkou, v Siemens-Martinských pecích, kde se využívá k oxidaci rezavý šrot, nebo v elektrických pecích. Vzniklá ocel se může obohacovat jinými kovy (legování), čímž vznikají různé typy oceli např. chromniklová nerez ocel, velmi tvrdá wolframová ocel, s přídavkem manganu a chromu pružinová ocel.
Vlastnosti
Železo je stříbrobílý lesklý kov, měkký, křehký, kujný a feromagnetický. Železo koroduje do hloubky – vzniká Fe2O3 ∙ n H2O. Reaguje se zředěnými kyselinami:
Fe + 2 HCl → FeCl2 + H2
Fe + H2SO4 → Fe SO4 + H2
Fe + 4 HNO3 → Fe(NO3)3 + NO + 2 H2O
Nereaguje s koncentrovanou kyselinou sírovou, proto se kyselina sírová může přepravovat v železných cisternách. Reaguje s kyslíkem, sírou a chlorem.
Použití
Čisté železo nemá výhodné vlastnosti, takže se používá jen v laboratořích a na jádra elektromagnetů. Vyrábí se z něj ocel, která má široké využití.
Sloučeniny železa
Sloučeniny železnaté obsahují kation Fe2+. Ve vodných roztocích jsou kationty Fe2+ hydratovány, takže tvoří zelené kationty [Fe(H2O)6]2+. Kationty Fe2+ mají redukční účinky:
Fe2+ + Ag+ → Ag + Fe3+
Železnaté sloučeniny se pomalu oxidují vzdušným kyslíkem na stálejší sloučeniny železité, které jsou žlutohnědé.
Oxid železnatý FeO je černý prášek, na vzduchu se oxiduje na oxid železitý, který je červený.
Šedozelený hydroxid železnatý Fe(OH)2 vzniká srážením roztoků železnatých solí roztokem alkalického hydroxidu:
Fe2+ + 2 OH– → Fe(OH)2 šedozelená sraženina
Heptahydrát síranu železnatého (zelená skalice) FeSO4 ∙ 7 H2O je zelená krystalická látka, na vzduchu se oxiduje na síran železitý a hnědne.

Obr. 2: Zelená skalice
Hexahydrát síranu amonnoželeznatého (Mohrova sůl) (NH4)2Fe(SO4)2 ∙ 6 H2O je zelená krystalická látka, nepodléhá oxidaci vzdušným kyslíkem. Používá se v analytické chemii.
Tetrahydrát chloridu železnatého FeCl2 ∙ 4 H2O je světle zelená krystalická látka.
Sulfid železnatý FeS má černou barvu, je nerozpustný ve vodě, reaguje s kyselinami a používá se na přípravu sulfanu:
FeS + H2SO4 → FeSO4 + H2S
Hydrogenuhličitan železnatý Fe(HCO3)2 se vyskytuje v pitné vodě. Oxidací vzdušným kyslíkem se vylučuje rezavá sraženina hydroxidu železitého.
Sloučeniny železité obsahují kation Fe3+. Z vodných roztoků krystalizují železité soli jako bledě růžové až bílé hydráty. Kationty Fe3+ mají sklon k hydrolýze a mají oxidační účinky:
Fe + 2 Fe3+ → 3 Fe2+
Zn + 2 Fe3+ → Zn2+ + 2 Fe2+
Cu + 2 Fe3+ → Cu2+ + 2 Fe2+
Tyto reakce probíhají v kyselém prostředí.
Oxid železitý Fe2O3 je červená pevná látka, která má schopnost jinou látku zabarvit, proto se používá jako pigment.
Oxid železnatoželezitý Fe3O4 (FeO ∙ Fe2O3) vzniká působením vodní páry na rozžhavené železo.
Hydroxid železitý Fe(OH)3 vzniká srážením roztoků železitých solí roztokem alkalického hydroxidu:
Fe3+ + 3 OH– → Fe(OH)3
Má hnědou barvu a používá se k přípravě železitých sloučenin.
Síran železitý Fe2(SO4)3 se přípravuje reakcí oxidu železitého s koncentrovanou kyselinou sírovou:
Fe2O3 + 3 H2SO4 → Fe2(SO4)3 + 3 H2O
Vodný roztok hydrolyzuje, proto má hnědou barvu.
Dodekahydrát síranu amonnoželezitého (kamenec amonnoželezitý) (NH4)Fe(SO4)2 ∙ 12 H2O tvoří světle fialové krystalky.
Červenohnědý chlorid železitý FeCl3 se připravuje reakcí železa s chlorem:
2 Fe + 3 Cl2 → 2 FeCl3
Hexahydrát chloridu železitého FeCl3 ∙ 6 H2O vzniká reakcí kyseliny chlorovodíkové s oxidem nebo hydroxidem železitým:
Fe2O3 + 6 HCl → 2 FeCl3 + 3 H2O
Fe(OH)3 + 3 HCl → FeCl3 + 3 H2O
Z vodného roztoku krystalizuje žlutý.
Koordinační sloučeniny železa
Hexakyanoželeznatan draselný (ferrokyanid draselný, žlutá krevní sůl) K4[Fe(CN)6] se používá v analytické chemii k důkazu železitých iontů, vzniká sraženina berlínské modři:
Fe3+ + [Fe(CN)6]4- → Fe4[Fe(CN)6]3
Hexakyanoželezitan draselný (ferrikyanid draselný, červená krevní sůl) K3[Fe(CN)6] má použití rovněž v analytické chemii k důkazu železnatých iontů, vzniká sraženina Turnbullovy modři:
Fe2+ + [Fe(CN)6]3- → Fe3[Fe(CN)6]2
K důkazu železitých iontů slouží i reakce:
Fe3+ + SCN– → [Fe(SCN)]2+
Vzniklá koordinační sloučenina s thiokyanatoželezitým kationtem má červenou barvu.