Přehled metod přípravy alkynů
Alkyny se připravují obdobnými eliminačními reakcemi jako alkeny.
1. Dehydrogenace alkanů nebo alkenů
Reakce se prakticky provádí na stejných katalyzátorech jako hydrogenace. Vodík se při reakci odštěpuje (eliminuje) a za podmínek reakce odstraňuje:

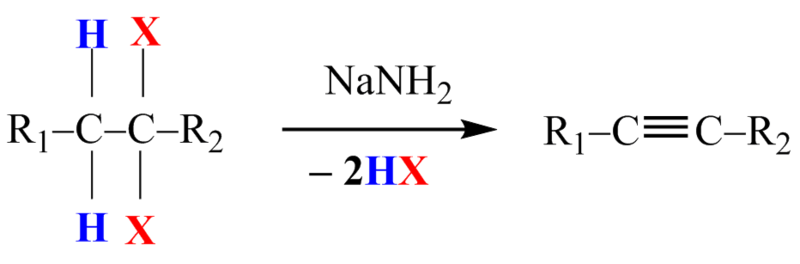
2. Dvojnásobná dehydrohalogenace vicinálních dihalogenderivátů
Pokud sloučenina obsahuje více molekul halogenů, pak může dojít k eliminaci i více molekul halogenovodíku za vzniku buď trojné vazby, nebo více dvojných vazeb. Dehydrohalogenace vicinálních (1,2-) dihalogenderivátů se provádí nejčastěji účinkem silných zásad (KOH, NaNH2…). Reakce probíhá postupně, pčičemž odštěpení první molekuly halogenovodíku nastává působením roztoku hydroxidu draselného, zatímco na odštěpení druhé molekuly je třeba použít ještě silnější zásadu, například amid sodný, NaNH2. Jeho účinnou složkou je anion NH2-.
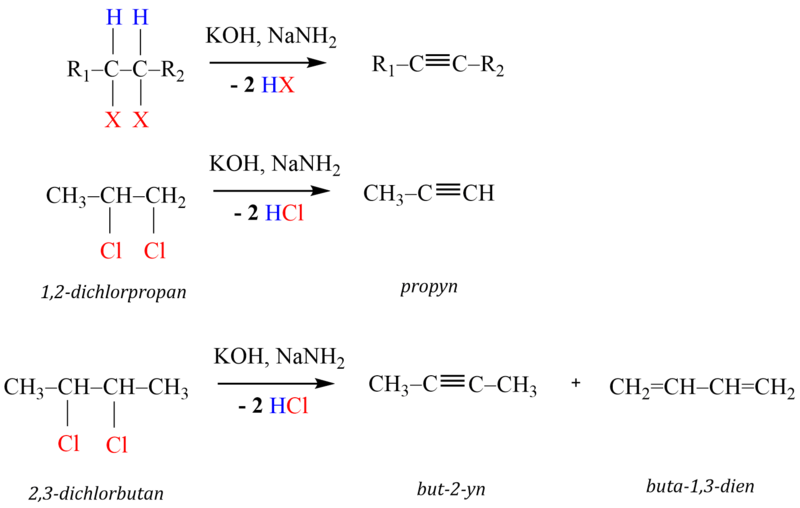
Pokud existují dvě možnosti eliminace halogenovodíku, dochází také ke vzniku dienů, jak je vidět na dehydrohalogenaci 2,3-dichlorbutanu.
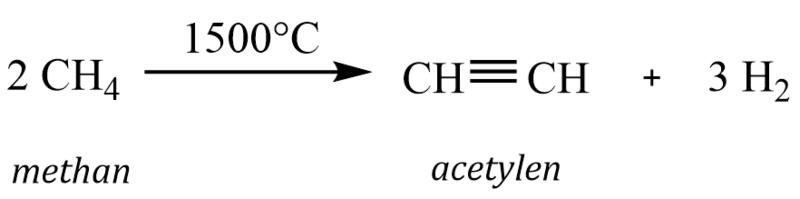
3. Ethyn (acetylen)
Samotný acetylen se tradičně připravoval rozkladem karbidu vápníku vodou (viz dříve), dnes však byla tato výroba zcela vytlačena ekonomičtější pyrolýzou methanu v elektrickém oblouku.
Přehled nejdůležitějších alkynů
Ethyn (acetylen)
Ethyn je bezbarvý plyn; čistý je bez zápachu, zatímco technický páchne (obsahuje fosfiny a arsiny). Se vzduchem tvoří výbušnou směs. Uchovává se v tlakových lahvích (s bílým pruhem) rozpuštěný v acetonu, kterým je napuštěn porézní materiál. Spolu s kyslíkem se používá ke svařování a řezání kovů, neboť reakce acetylenu s kyslíkem je vysoce exotermická a ve speciálních hořácích tvoří plamen o teplotě až 3000 °C.
Hoření acetylenu:
2 CH≡CH + 2 O2 → 3 C + CO2 + 2 H2O
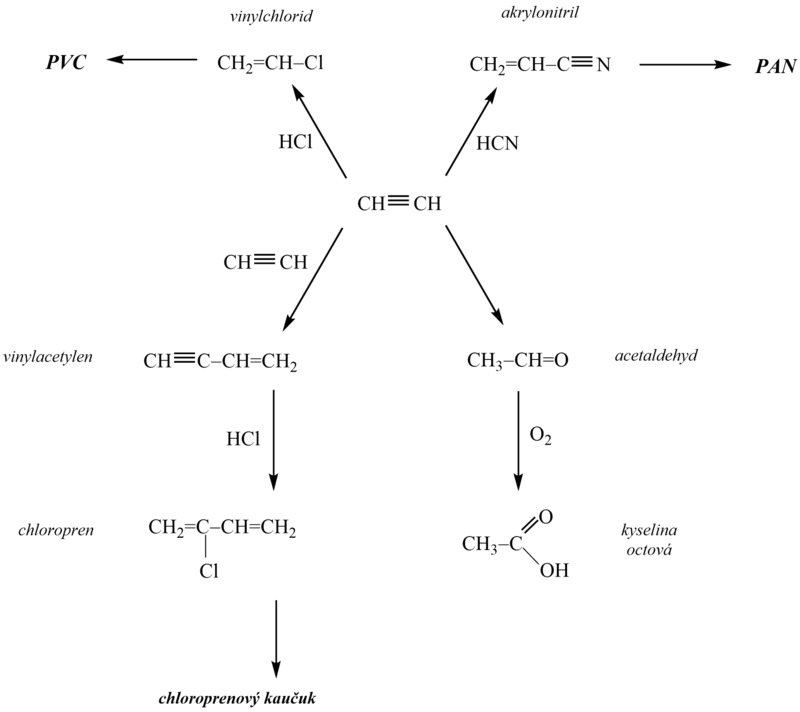
Z acetylenu se připravují adičními reakcemi průmyslově významné monomery, jako vinylchlorid, akrylonitril a další. Jeho dimerizací působením přechodných kovů se získává vinylacetylen.
Schéma reaktivity a využití:
- FIKR, Jaroslav a Jaroslav KAHOVEC. Názvosloví organické chemie. Olomouc: Rubico, 2002, ISBN 80-7346-017-3.
- HONZA, Jaroslav a Aleš MAREČEK. Chemie pro čtyřletá gymnázia 2. díl. Olomouc: Nakladatelství Olomouc, 2005, ISBN 80-7182-141-1.
- JANECZKOVÁ, Anna a Pavel KLOUDA. Organická chemie. Ostrava: Nakladatelství Pavel Klouda, 1998, ISBN 80-902155-6-4/9802.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie v kostce II.. Havlíčkův Brod: Fragment, 1997, ISBN 80-7200-342-9.
- PACÁK, Josef. Jak porozumět organické chemii. Praha: Karolinum, 1997, ISBN 80-7184-261-3.
- SVOBODA, Jiří a kol. Organická chemie I. Praha: Vysoká škola chemicko-technologická, 2005, ISBN 80-7080-561-7.
Obrázky
- Obr. 1: Autor neznámý. www.wikiwand.com [online]. [cit. 25.10.2014]. Dostupný na WWW: http://upload.wikimedia.org/wikipedia/commons/2/22/Carbide_lamp_on_a_bicycle.jpg
- Obr. 2: Autor neznámý. www.cms-kh.cz [online]. [cit. 25.10.2014]. Dostupný na WWW: http://www.cms-kh.cz/sites/default/files/images/1921-80s.jpg?1326204204
Pokud není uvedeno jinak, autorem obrázků je Mgr. Michal Bezděk.
Eliminace
Eliminace je reakce, při které se ze dvou sousedních uhlíkových atomů v molekule odštěpí atomy nebo skupina atomů, které poskytnou nízkomolekulární produkt, a mezi těmito uhlíkovými atomy vznikne násobná vazba nebo se zvyšuje násobnost vazby.
Příprava alkynů - video
Katalyzátor
Katalyzátor je látka vstupující do chemické reakce, kterou urychluje (nebo zpomaluje), a přitom z ní vystupuje nezměněná.
Vicinální dihalogenderivát
Jedná se o halogenderivát se dvěma funkčními skupinami (halogeny) na sousedních (vicinálních) atomech uhlíku.
Geminální dihalogenderiváty
Kromě vicinálních dihalogenderivátů se v praxi používají i tzv. geminální dihalogenderiváty, které se taktéž dehydrohalogenují účinkem silných bází. Označení geminální znamená, že obě dvě funkční skupiny se nachází na tomtéž uhlíku (viz vzorec):
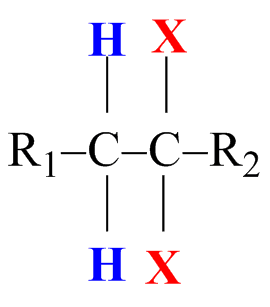
Dehydrogenace geminálních dihalogenderivátů:
Napiš rovnice dehydrohalogenačních reakcí a pojmenuj produkt:
- dehydrochlorace 3,4-dichlorhexanu účinkem amidu sodného
- dehydrojodace 2-jod-2-methylbutanu účinkem hydroxidu draselného v alkoholu
- dehydrochlorace 1-chlorprop-1-enu účinkem amidu sodného
- dehydrochlorace 1,1-dichlorpropanu účinkem amidu sodného
- dehydrochlorace 2,2-dichlorpropanu účinkem amidu sodného
- dehydrochlorace 2,2-dichlorbutanu účinkem amidu sodného
Napiš rovnice dehydrogenačních reakcí a pojmenuj produkt:
- dehydrogenace propanu
- dehydrogenace butanu
Acetylen
Reakce dikarbidu vápenatého s vodou se dříve využívalo v hornictví – horníci v dolech si svítili lampami – karbidkami, ve kterých se uvedenou reakcí vyvíjel ethyn, jenž po zapálení osvětloval prostory.

Obr. 1: Karbidka na jízdním kole

Obr. 2: Rozebraná hornická karbidka
Karbidová lampa - video
Demonstrace hořlavosti acetylenu - video
Zmínku o tomto plynu najdeme i v knize Karla Poláčka „Bylo nás pět“.
Ukázka:
… Pak jsme šli, Bejval nic neříkal a my jsme taky nic neříkali a on nás vedl do polí. Když jsme byli v polích, tak Bejval pravil, jestli víme, že když se ta látka hasí vodou, tak se z ní vyvine plyn, který byv zapálen vydává jasné světlo? Odvětili jsme, že to víme, a já jsem pravil, že jsem jednou viděl takovou lampu, jak s ní o pouti svítil medák na turecký med. Bejval pravil, dobře že to víme, a pak nám vysvětlil, v čem spočívá ten vynález, z něhož bude děsná legrace. Na poli leželo sněhu velice moc a my jsem to všechno zahrabali do sněhu, a když už to bylo zahrabaný, tak jsme rozškrtli zápalku a chvilku drželi u toho. Za chvilánku to začalo prudce syčet, pak to chytlo a hořelo jasným plamenem. Kdo by nevěděl, co v tom je, tak by si myslil, že hoří sníh, což by mu bylo divné. A my jsme šli od toho dál, a když jsme byli dál, tak šlehaly plameny velice vysoko a bylo velké světlo a my jsme se z toho radovali. …
Jakou látku kluci zahrabali do sněhu?
Napiš rovnici reakce této látky s vodou.
Vinylchlorid
Vinylchlorid je surovina na výrobu PVC (polyvinylchlorid).
Akrylonitril
Akrylonitril je surovina na výrobu akrylových vláken (PAN), dále akrylonitril–butadien–styrenových pryskyřic (ABS) a adiponitrilu.
Akrylová vlákna jsou používána pro výrobu oděvů, jako jsou svetry, vlněné a sportovní oděvy, ale i pro různá domácí bytová zařízení, jako koberce nebo čalounění.
ABS pryskyřice jsou používány především v automobilovém průmyslu (vnitřní panely dveří, lemování sedaček, mřížky, přístrojové desky, pouzdra zrcátek).
Adiponitril se používá k výrobě hexamethylendiaminu (hexan-1,6-diamin), který slouží k výrobě nylonu 66.
Chloropren
Chloropren je surovina na výrobu chloroprenového kaučuku, známého pod názvem Neopren, který slouží jako materiál pro výrobu kombinéz pro vodní sporty.
Chloroprenový kaučuk
Jedná se o první syntetickou „gumu“ použitou komerčně. Je velmi elastický a má vysokou odolnost proti stárnutí. Byl to první syntetický kaučuk vyráběný v předválečném Československu firmou Baťa pod obchodním označením Baťapren a SK-Baťa.