Názvosloví
Názvosloví aromatických monocyklických i polycyklických uhlovodíků vychází z triviálních názvů základních představitelů této skupiny.
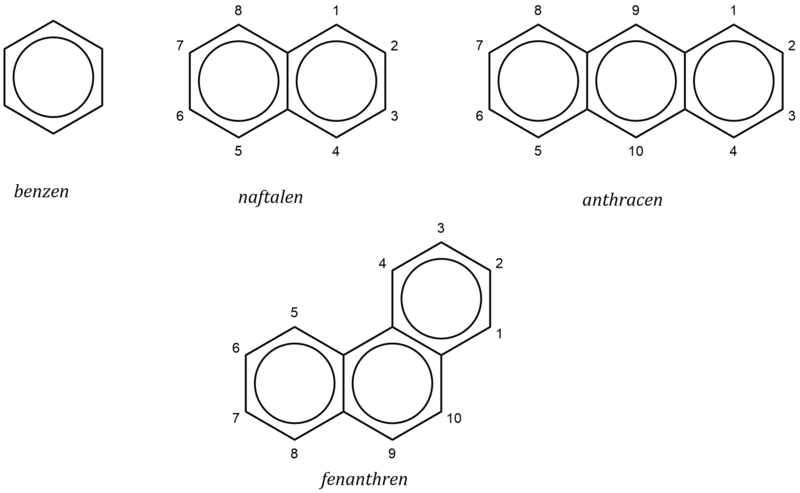
Základním arenem je benzen. Je to tzv. jednojaderný aren. Jeho šestičlenný kruh se též nazývá benzenové jádro. Uhlovodíky, které mají dvě a více těchto jader spojených dohromady společnou stranou, se nazývají kondenzované aromatické uhlovodíky.
Základními kondenzovanými aromatickými uhlovodíky jsou naftalen, anthracen a fenanthren.
V benzenu jsou všechny uhlíky rovnocenné, proto existuje pouze jeden monosubstituovaný derivát, takže číslování je závislé na dalších přítomných substituentech. Kondenzované areny se číslují podle dohodnuté konvence, jak je uvedeno ve schématu:
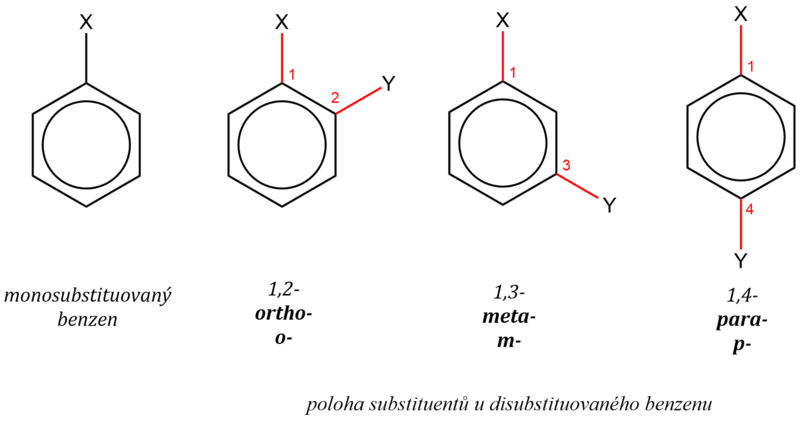
Disubstituované deriváty benzenu mohou (při stejných substituentech) existovat ve třech izomerních formách (polohové izomery). Vzájemnou polohu substituentů vyjadřujeme buď čísly, nebo předponami:
- 1, 2 –ortho (o),
- 1, 3 – meta (m) a
- 1, 4 – para (p).
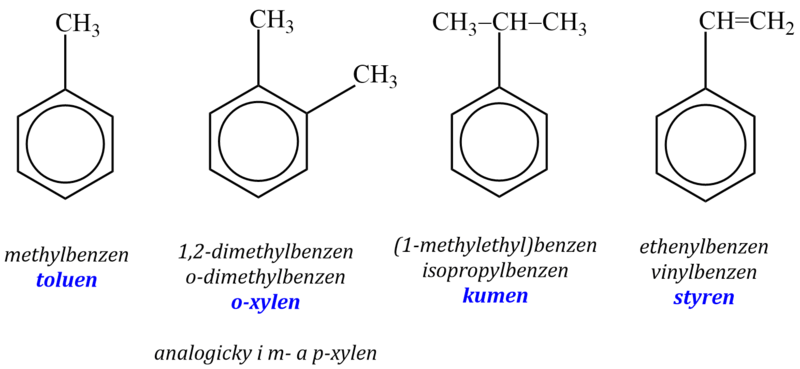
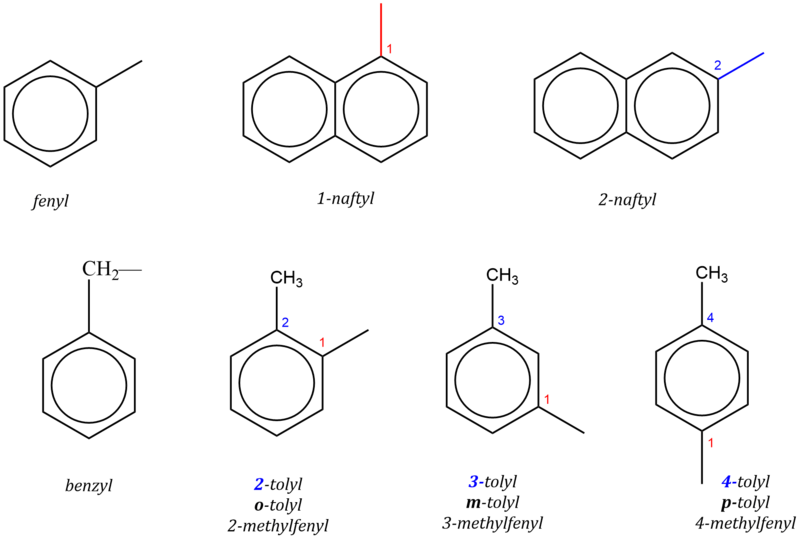
U mnoha aromatických uhlovodíků se běžně používají triviální názvy. V následujícím schématu je uvedeno několik z nich spolu s uvedením systematických názvů.
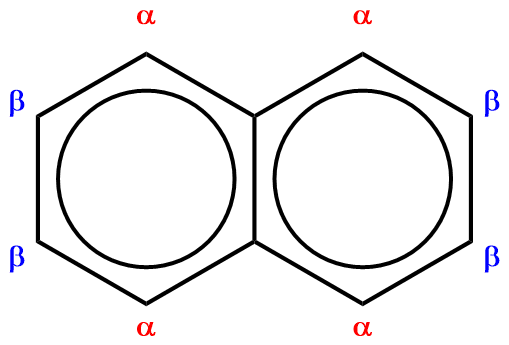
U derivátů naftalenu se běžně označují polohy 1, 4, 5, 8 písmenem α, zbývající polohy písmenem β.
Odtržením vodíku z molekuly aromatického uhlovodíku získáme uhlovodíkový zbytek, tzv. aryl.
Názvy arylů tvoříme připojením koncovky –yl ke kmeni názvu příslušného aromatického uhlovodíku (výjimkou je fenyl odvozený od benzenu ), přičemž uhlík, ze kterého vychází volná vazba, má lokant 1.
Fyzikální vlastnosti
Benzen a jeho homology jsou kapaliny charakteristického zápachu (proto název aromatické). Jsou lehčí než voda a ve vodě nerozpustné, dobře se rozpouštějí v organických rozpouštědlech (ethanol, aceton, chloroform…)
Většina kapalných arenů jsou výbornými rozpouštědly (průmysl barev a laků). Některé z nich jsou značně jedovaté, jejich zhoubný vliv se projevuje při vdechování par, ale mohou se vstřebávat také pokožkou.
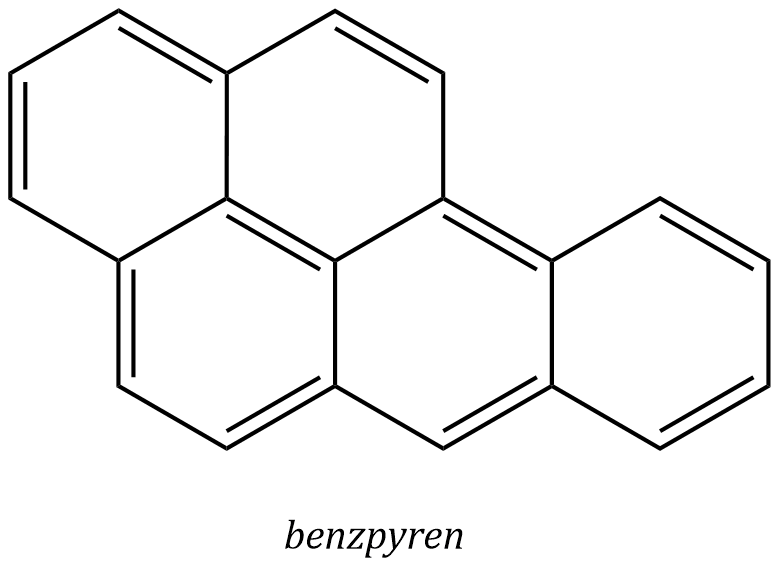
Kondenzované aromatické uhlovodíky (naftalen, anthracen…) jsou pevné, ve vodě rovněž nerozpustné. Aromatické sloučeniny mají často výraznou biologickou aktivitu. Jak benzen, tak i řada dalších aromátů jsou látky jedovaté a mnoho z nich patří mezi potenciální nebo prokázané karcinogeny. Mezi takové karcinogeny patří např. benzo[a]pyren, který je obsažen ve spalných produktech uhlí a jehož přítomnost byla prokázána i v cigaretovém kouři.
Teploty tání a varu některých vybraných zástupců jsou uvedeny v tabulce:
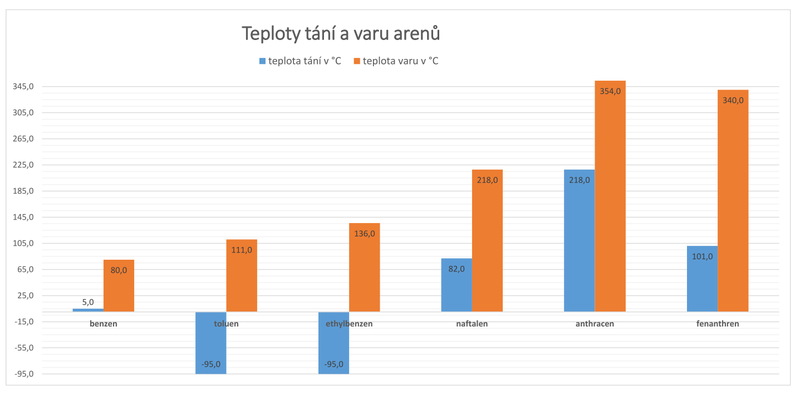
Tab. 1: Teploty tání a varu arenů
Vzhledem k přítomnosti rozsáhlého π-elektronového systému absorbují aromatické uhlovodíky světlo. Zatímco jednoduché areny (benzen, toluen) absorbují záření pouze v ultrafialové oblasti (do 270 nm), a jsou tedy bezbarvé, vyšší kondenzované systémy s rozšířenou konjugací absorbují světlo ve viditelné oblasti, a jsou tudíž barevné. Prakticky všechna používaná barviva jsou založena na substituovaných aromatických systémech.
Zdroje arenů
Zdrojem aromatických uhlovodíků je uhlí a ropa. Uhlí se podrobuje vysokotepelné karbonizaci za nepřístupu vzduchu. Vedle plynných zplodin a koksu se z něj získává kapalný produkt = dehet. Ten se zpracovává frakční destilací na sloučeniny kyselé povahy (fenoly), zásadité povahy (pyridinové báze) a neutrální aromatické sloučeniny. Při zpracování neutrálních sloučenin destilací se získá nejníže vroucí frakce obsahující benzen, toluen a všechny tři izomerní xyleny, vyšší frakce obsahuje hlavně naftalen a jeho homology. Další frakční destilací a jinými speciálními technikami lze získat jednotlivé aromáty v čistém stavu.
- FIKR, Jaroslav a Jaroslav KAHOVEC. Názvosloví organické chemie. Olomouc: Rubico, 2002, ISBN 80-7346-017-3.
- HONZA, Jaroslav a Aleš MAREČEK. Chemie pro čtyřletá gymnázia 2. díl. Olomouc: Nakladatelství Olomouc, 2005, ISBN 80-7182-141-1.
- JANECZKOVÁ, Anna a Pavel KLOUDA. Organická chemie. Ostrava: Nakladatelství Pavel Klouda, 1998, ISBN 80-902155-6-4/9802.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie v kostce II.. Havlíčkův Brod: Fragment, 1997, ISBN 80-7200-342-9.
- PACÁK, Josef. Jak porozumět organické chemii. Praha: Karolinum, 1997, ISBN 80-7184-261-3.
- SVOBODA, Jiří a kol. Organická chemie I. Praha: Vysoká škola chemicko-technologická, 2005, ISBN 80-7080-561-7.
Obrázky
- Obr. 1: Autor neznámý. www.wikiwand.com [online]. [cit. 25.10.2014]. Dostupný na WWW: http://upload.wikimedia.org/wikipedia/commons/thumb/c/cc/Colonne_distillazione.jpg/800px-Colonne_distillazione.jpg
Pokud není uvedeno jinak, autorem obrázků je Mgr. Michal Bezděk.
Kondenzované aromatické uhlovodíky
Jedná se o polycyklické aromatické uhlovodíky obsahující ve své molekule 2 – 6 benzenových jader, těsně k sobě připojených (se společnými uhlíkovými atomy).
Kromě již uvedených sem také patří: pyren, chrysen, koronen, benzo[a]pyren, tetracen, [18] annulen a další.
Vyhledej uvedené zástupce a urči, kolik π–elektronů obsahuje jejich delokalizovaný systém.
Úvod do názvosloví derivátů benzenu - video
Úvod do názvosloví organické chemie - uhlovodíky
Polohové izomery
Jednotlivé izomery se liší polohou substituentů nebo násobných vazeb. Polohovými izomery jsou např. 1-chlorpentan, 2-chlorpentan a 3-chlorpentan. Dále pent-1-en a pent-2-en.
K jakému druhu izomerie řadíme polohové izomery?
Uveďte, které z následujících sloučenin jsou ortho-, meta- nebo para- substituované:
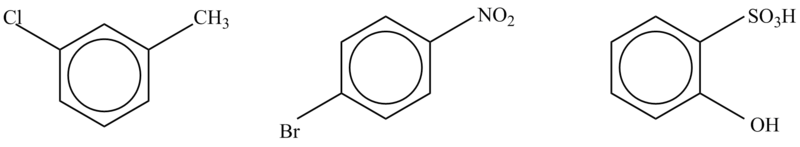
Názvosloví arenů - viz přílohy
Názvosloví arylů odvozených od kondenzovaných arenů
Aryly odvozené od kondenzovaných aromátů musí respektovat dohodnuté číslování. Například u naftalenu nepoužíváme název naftalen-2-yl, ale stažený název 2-naftyl, obdobně je tomu i u fenanthrenu a anthracenu.
Vytvoř vzorce následujících arylů:
- 2-fenanthryl
- 1-anthryl
- 2-anthryl
- 9-anthryl
- 2-methyl1-naftyl
- 1-methyl2-naftyl
- 9-vinyl-2-anthryl
Vysvětli, proč jsou aromatické uhlovodíky nerozpustné ve vodě.
Ropa
Výskyt ropy v současnosti
Výhled do budoucnosti
Složení ropy
Těžba ropy
Co se vyrábí z ropy?
Automobilový benzín
Frakční destilace
Oddělení jednotlivých složek na základě rozdílné teploty varu.

Obr. 1: Kolony pro průmyslovou frakční destilaci