Adiční reakce
Vedle typických substitučních reakcí mají u aromatických uhlovodíků technický význam i některé reakce adiční. Adice na aromatický systém probíhá obtížně (většinou radikálovým mechanismem), protože aromatický systém je velmi stabilní a ruší se jen těžko.
Mezi nejvýznamnější adiční reakce patří hydrogenace a halogenace (chlorace, bromace).
1. Hydrogenace
Adici vodíku na aromatický systém katalyzují některé kovy (Raneyův nikl, platina) a produktem jsou nasycené cyklické uhlovodíky:
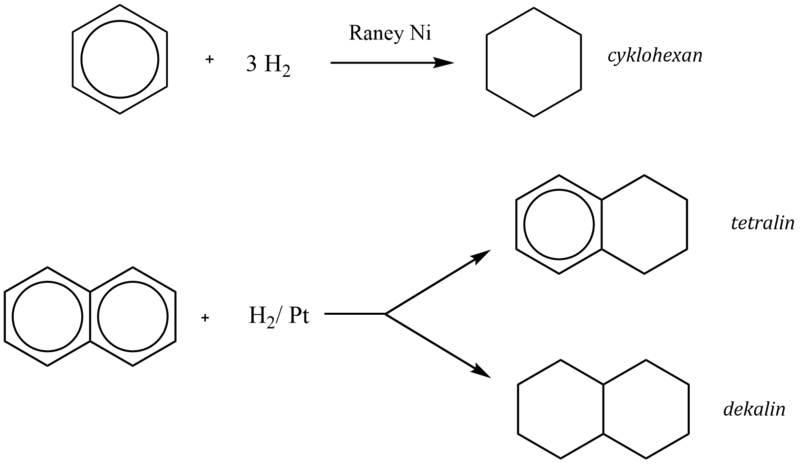
2. Halogenace
Adice halogenu je iniciována homolytickým štěpením vazby v molekule činidla, např. UV zářením:
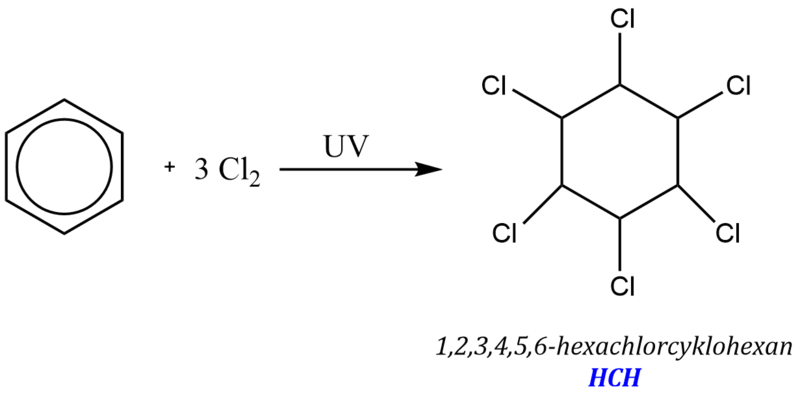
Produkt této reakce označovaný jako Lindan nebo „HCH“, byl používaným insekticidem. Dnes je již používání této látky zakázáno vzhledem k její stabilitě, a s tím související špatné biologické odbouratelnosti.
Oxidace arenů
Vzhledem ke stabilitě aromatického systému je přímá oxidace arenů velmi obtížnou záležitostí, neboť areny jsou vůči mírným oxidačním činidlům poměrně stálé.
1. Oxidace na aromatickém systému
V praxi se nejčastěji provádí vzdušným kyslíkem za přítomnosti katalyzátoru oxidu vanadičného a zvýšené teploty. Při reakci dochází k zániku aromatického charakteru.
Katalytickou oxidací benzenu lze připravit maleinanhydrid, zatímco katalytickou oxidací naftalenu anhydrid kyseliny benzen-1,2-dikarboxylové, tzv. ftalanhydrid, důležitý meziprodukt při výrobě kyseliny ftalové.

2. Oxidace na postranním řetězci – oxidace alkylhomologů benzenu
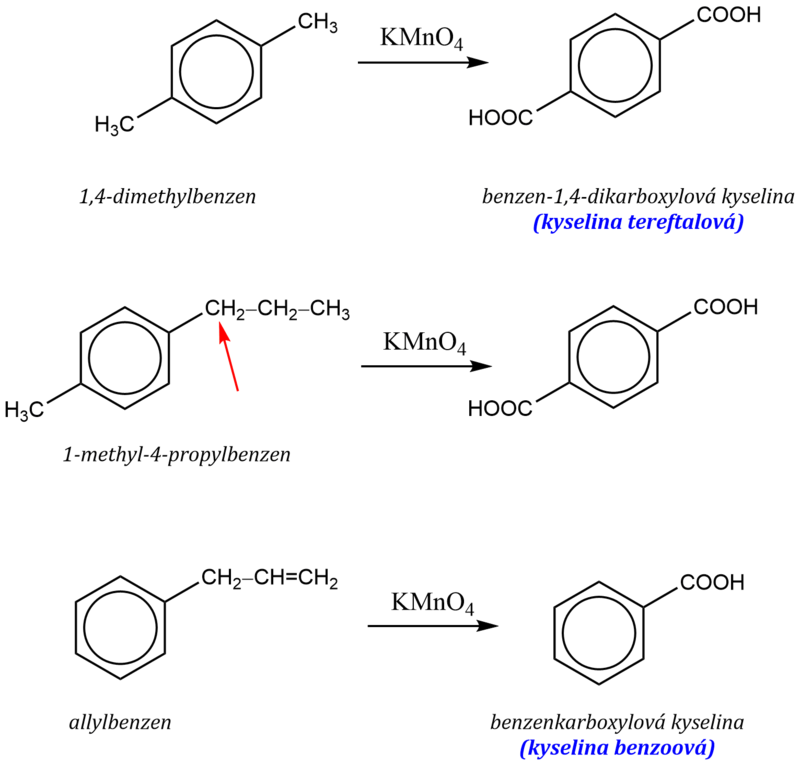
Alkylhomology benzenu oxidujeme již běžnými oxidačními činidly. Při působení těchto činidel se však neoxiduje benzenové jádro, ale postranní řetězec. Reakce probíhá bez ohledu na délku postranního řetězce vždy na uhlíku v sousedství benzenového jádra – na tzv. benzylovém uhlíku. Pokud oxidujeme vyšší alkylskupiny (ethyl apod.), vede použití silného oxidačního činidla ke štěpení vazby uhlík–uhlík vedle benzylového uhlíku a k oxidaci na karboxylové kyseliny.



 Obr. 3: Socha Václava Havla z polyesterové pryskyřice autorky Barbory Dausové (2010), Měštanská beseda, Plzeň
Obr. 3: Socha Václava Havla z polyesterové pryskyřice autorky Barbory Dausové (2010), Měštanská beseda, Plzeň

