Metabolismus lipidů
Transport lipidů v našem těle, zejména triacylglycerolů a cholesterolu, je velmi složitý. Lipidy nemohou být v organismu transportovány v podobě samostatných volných molekul z důvodu nerozpustnosti v polárních rozpouštědlech. Jsou dopravovány buď jako celek, nebo v hydrolyzované podobě mastných kyselin a glycerolu. Cholesterol může být při transportu vázán jako ester na mastnou kyselinu. Celistvé molekuly triacylglycerolů jsou transportovány jako součást lipoproteinů.
V potravě je obsaženo 20 – 40 % lipidů, z nichž 90 % tvoří triacylglyceroly. Jsou součástí rostlinné i živočišné stravy.
Katabolismus lipidů
Trávení lipidů probíhá na fázovém rozhraní tuk – voda (z důvodu jejich nerozpustnosti ve vodě).
Štěpení lipidů začíná v žaludku, kde jsou z důvodu silně kyselého prostředí (kyselina chlorovodíková) štěpeny pouze mléčné tuky. Dále štěpení pokračuje ve dvanáctníku, kde se pomocí lipas odbourává 1 až 2 mastné kyseliny z krajních poloh C1 nebo C3.
Vzniká směs mastných kyselin, mono- a diacylglycerolů, která je pomocí žlučových kyselin absorbována sliznicí tenkého střeva. Ty jsou ve střevních buňkách převedeny na triacylglyceroly a včetně cholesterolu jsou zabaleny do chylomikronů, které jsou vysílány do lymfy. Odtud jsou uvolňovány do krve a jí přenášeny do tkání. Ve tkáních jsou před přijetím hydrolyzovány lipoproteinovou lipasou na mastné kyseliny a glycerol. Část mastných kyselin se uvolní do krve vázána na albumin. Mastné kyseliny jsou v buňkách tkání (v mitochondriích) oxidovány (β-oxidace) a slouží jako vydatný zdroj energie. Mastné kyseliny, které vstupují do tukových buněk, se znovu esterifikují na triacylglycerol. Glycerol je zachycován v játrech a ledvinách, je využíván buď ke glukoneogenezi, nebo k syntéze triacylglycerolů.
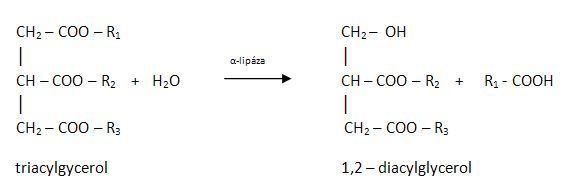
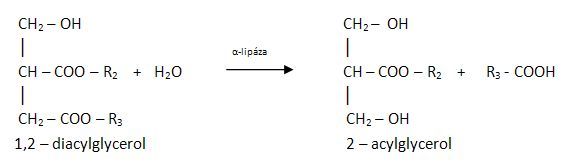
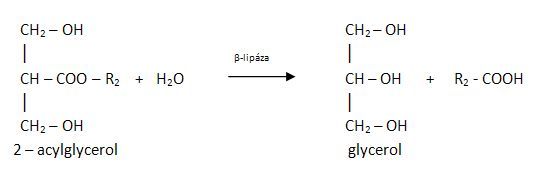
Obr. 1: Hydrolýza triacylglycerolu
β-oxidace karboxylových kyselin probíhá následovně:
Molekula karboxylové kyseliny se musí nejprve aktivovat vazbou na molekulu koenzymu A. Vzniká acylkoenzym A za současného hydrolytického štěpení ATP (spotřeba energie).
Po aktivaci molekuly následují přeměny v metabolické dráze, jejichž výsledkem je odštěpování dvouuhlíkového zbytku karboxylové kyseliny ve formě acetylkoenzymu A.
Reakce probíhá na druhém uhlíkovém atomu vedle karboxylové skupiny (β-uhlíku, odtud β-oxidace).
Po odštěpení první molekuly acetylkoenzymu A reakce pokračuje – a to tak, že o dva uhlíkové atomy kratší molekula karboxylové kyseliny se přeměňuje ve stejné metabolické dráze.
Děj se opakuje tak dlouho, dokud není molekula původní karboxylové kyseliny zcela neodbourána na dvouuhlíkaté zbytky ve formě acetylkoenzymu A.
Vzniklé molekuly acetylkoenzymu A vstupují do citrátového (Krebsova) cyklu. Jsou oxidovány za vzniku oxidu uhličitého a vody.
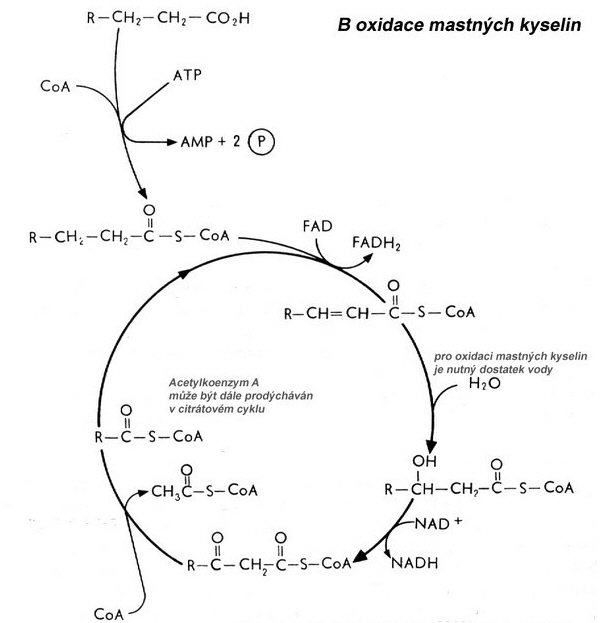
Obr. 2: Schema β-oxidace mastných kyselin
Oxidací karboxylových kyselin získávají buňky velké množství energie ve formě ATP. Například při úplné oxidaci jedné molekuly kyseliny palmitové získávají buňky 131 molekul ATP.
Anabolismus lipidů (biosyntéza)
Pro syntézu lipidů je nutná přítomnost všech základních složek v organismu - glycerol a mastné kyseliny, které musí být aktivovány.
Mastné kyseliny vznikají „opačným“ pochodem k β-oxidaci. Syntéza mastných kyselin probíhá v cytoplazmě (β-oxidace v mitochondriích), výchozí látkou pro syntézu je acetylkoenzym A. K průběhu syntézy je potřeba značné množství energie.
