Charakteristika enzymů jako biokatalyzátorů, struktura enzymů
Příroda vyřešila problém zajištění přísunu energie a stavebního materiálu z okolí a jejich využití pro provoz organismu a výstavbu vytvořením složité sítě chemických dějů. Na řízení a koordinaci tohoto systému chemických reakcí a s ním spojených energetických změn se podílí pestrá škála biokatalyzátorů. Jejich nejpočetnější a nejdůležitější skupinu tvoří bílkovinné makromolekuly, které urychlují chemické přeměny a nazývají se enzymy.
Enzymy se nacházejí ve všech živých systémech, i nejjednodušší buňky obsahují přes 3000 enzymů. Každý biologický druh produkuje své vlastní enzymy, které se mohou v některých vlastnostech lišit od enzymů jiného druhu. Počet existujících enzymů se odhaduje na miliardy.
Vlastnosti enzymů:
-
Enzymy umožňují, aby reakce proběhla, nebo ji urychlují.
-
Enzymy umožňují, aby reakce probíhala za mírných podmínek (normální atmosférický tlak, teplota a pH). Obvykle enzymové reakce probíhají při pH blízkém neutrální oblasti (pH 5-7), ale mohou také probíhat při nízkém pH (pepsin: pH 1,5 - 2) nebo vysokém (arginasa: pH 9,5).
-
Enzymy obvykle katalyzují přeměnu jedné látky (nebo skupiny látek) na produkt, případně katalyzují určitý typ chemické reakce.
-
Přítomnost některých látek může ovlivnit enzymovou reakci (urychlit - aktivátor, zpomalit nebo zastavit - inhibitor).
Struktura enzymů
Enzym je vždy složená bílkovina. Má velikou molekulu s Mr mezi 25 000 a několika miliony. Velikostí až na výjimky převyšuje velikost molekuly substrátu.
Bílkovinná část enzymu se nazývá apoenzym, neproteinová část koenzym (kofaktor nebo prostetická skupina). Samotný apoenzym je katalyticky neúčinný, ovšem ani koenzym sám o sobě katalytickou aktivitu neprojevuje.
Kofaktor lze od enzymu oddělit, kdežto prostetická skupina je trvalou součástí enzymu.
Obr. 1: Obrázek enzymu – lidská glyoxyláza (převažují bílkovinné řetězce, koenzymem jsou ionty zinku – fialové)
Aby byl enzym účinný, musí vytvořit se substrátem enzym-substrátový komplex.
Na povrchu enzymu je relativně malé místo, na které se napojuje substrát. Nazývá se aktivní centrum. Na povrchu enzymu je obvykle jen jedno aktivní centrum. Jde o jakýsi zářez, do kterého zapadne molekula substrátu a zde se naváže. Na této vazbě se uplatňují nevazebné interakce – vodíkové vazby, hydrofobní interakce, elektrostatické síly apod.
Na povrchu enzymu se najdou kromě aktivního centra i determinantní skupiny, čili místa určující imunitní charakteristiku molekuly, nebo mnohá místa vážící jedy a farmaka.
Substrát se navazuje na enzym podle teorie „zámku a klíče“, která byla upravena na teorii indukovaného přizpůsobení. Substrát je do jisté míry schopen vyvolat změnu konformace enzymu, který se tak dokáže přizpůsobit substrátu – tedy tvaru „klíče“. Rovněž tvar substrátu se někdy přizpůsobuje enzymu.
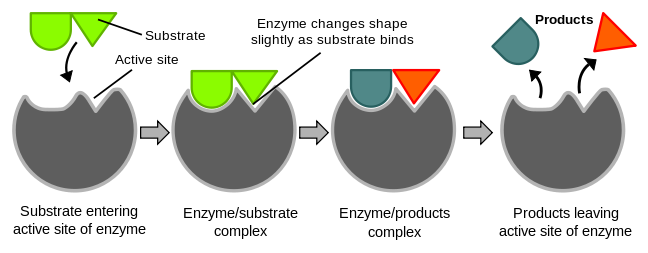
Obr. 2: Schéma indukovaného přizpůsobení
- LEDVINA, Miroslav, Alena STOKLASOVÁ a Jaroslav CERMAN. Biochemie pro studující medicíny I. díl, 2. vydání, Praha: Karolinum, 2009, ISBN 978-80-246-1416-4
- VODRÁŽKA, Zdeněk. Biochemie. 2. opravené vydání, Praha: Akademia, 2002, ISBN 80-200-0600-1
Obrázky:
- Obr. 1: PyMOL. http://cs.wikipedia.org [cit. 10. 5. 2014] dostupné na www http://cs.wikipedia.org/wiki/enzym
- Obr. 2: TimVickers. http://cs.wikipedia.org [cit. 10. 5. 2014] dostupné na www http://cs.wikipedia.org/wiki/enzym
- Obr. 3: Labrador2. http://cs.wikipedia.org [cit. 1.11.2014] dostupné na www: http://cs.wikipedia.org/wiki/Enzym#mediaviewer/File:Carbonic_anhydrase.png
Historický přehled enzymologie
Enzymologie – věda o enzymech – se vyvíjela společně s biochemií od devatenáctého století sledováním fermentací a trávení. Za začátek výzkumu fermentací je považováno zjištění J. L. Guy-Lussaca z roku 1810, že kvasinky rozkládají cukr převážně na ethanol a CO2. Louis Pasteur ověřil nereprodukovatelnost většiny biochemických reakcí v laboratoři, což vedlo k předpokladu, že fermentace je vázána na živé buňky. Pasteur proto předpokládal, že živé systémy jsou vybaveny „životní silou“, která jim dovoluje obcházet přírodní zákony, řídící neživou hmotu. Na druhé straně Justus Liebig dokazoval, že příčinou biochemických procesů je činnost chemických sloučenin tehdy známých jako „fermenty“. A tak název „enzym“ (řecky: en ,v; zyme, kvasinka), který navrhl Fridrich Wilhelm Kűhne, měl zdůraznit, že ne kvasinky samy, ale něco v kvasinkách katalyzuje reakce kvašení neboli fermentace.
Emil Fischer v roce 1894 objevil, že glykolytické enzymy rozlišují stereoizomery cukrů, což vedlo k vyslovení hypotézy zámku a klíče: Specifita enzymu (zámku) k jeho substrátu (klíči) vzniká jejich komplementárními geometrickými tvary. Avšak chemické složení enzymů bylo objevem až dvacátého století. V roce 1926 vykrystalizoval James Summer první enzym ureázu, katalyzující hydrolýzu močoviny na amonné a uhličité ionty a prokázal, že jde o protein.
Většina našich znalostí o povaze a funkci enzymů pochází z druhé poloviny dvacátého století. Až s příchodem nových technik separace a analýz bylo možno enzymy běžně izolovat a charakterizovat. V roce 1963 byla zveřejněna první aminokyselinová sekvence enzymu, a to hovězí pankreatické ribonukleázy A.
ELISA
Enzymová imunoanalýza - ELISA - je jednou z kvantitativních imunochemických metod (viz Imunochemické metody stanovení proteinů). Jedna z reagujících složek – antigen nebo protilátka - je značena enzymem, jehož detekce (průkaz) je vysoce citlivý. Tak se dosahuje možnosti zjistit i zcela nepatrné množství antigenu.
Tento princip je využíván k určení koncentrací různých proteinů a dalších látek, např. hormonů (steroidů, hormonů štítné žlázy) nebo hladiny léků v biologických tekutinách.
Enzymoimunoanalýza je používána i v různých testovacích proužcích, např. těhotenský test (stanovení hormonu hCG), diagnostické proužky na drogy.