Energetika a kinetika enzymových katalýz
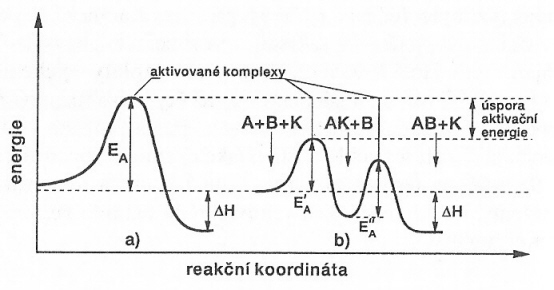
K průběhu chemické reakce je zapotřebí dodání energie, které se říká aktivační energie. Pro každou chemickou reakci existuje jistá aktivační energie, kterou musí mít molekuly, aby jejich srážky při chemické reakci byly účinné. Přítomnost katalyzátoru vede reakci jiným reakčním mechanismem, u kterého je aktivační energie každé dílčí reakce nižší, než energie původní nekatalyzované reakce. Bez katalyzátoru by některé reakce neproběhly vůbec, anebo za velmi složitých podmínek (vysoká teplota, tlak, dlouhá reakční doba apod.).
Pro enzymově katalyzované reakce tedy platí, že pro jejich zahájení je zapotřebí dodat mnohem méně aktivační energie, než pro reakce, které probíhají bez přítomnosti enzymu.
Vysoká účinnost enzymových reakcí a jejich specifita jsou dány:
-
možností aktivního centra enzymu deformovat a polarizovat vazby v substrátech tak, aby byly reaktivnější,
-
možností koncentrovat substrát z roztoku ve vazebném místě,
-
možností přesné orientace substrátu v aktivním centru enzymu,
-
možností pevného připoutání substrátu ve vazebném místě.
Rychlost enzymové reakce je závislá na:
-
koncentraci substrátů,
-
množství enzymu,
-
fyzikálně-chemických vlastnostech prostředí,
-
přítomnosti aktivátorů a inhibitorů.
Nejjednodušší enzymové reakce jsou jednosubstrátové, přičemž vodu za substrát nepovažujeme, jelikož se reakce neúčastní. Znamená to, že jediný substrát je přeměňován na jeden nebo dva produkty. Takovýchto reakcí je menšina.
Nejčastější jsou reakce dvousubstrátové, při nichž enzym katalyzuje přeměnu dvou substrátů, obvykle na dva produkty. Existují i reakce třísubstrátové i vícesubstrátové.
Při vysokých koncentracích substrátu je reakční rychlost konstantní, při nízkých koncentracích substrátu je časový průběh enzymové reakce vystižen kinetickou rovnicí I. řádu a křivka vyjadřuje sycení enzymu substrátem. To znamená, že při jednosubstrátových reakcích a dostatečném množství substrátu se množství vznikajících produktů mění s časem lineárně. Této skutečnosti se využívá při tzv. kinetickém určování množství enzymu (zjistí se rychlost přeměny substrátu za časovou jednotku).
Množství enzymu se udává jako enzymová aktivita enzymu v jednotkách katal, což je množství, které přemění 1 mol substrátu za 1 sekundu. V praxi se obvykle používá jednotka mnohem menší, a to nkat (nanokatal), což je 10-9 katalu.
Rychlost enzymových reakcí stoupá s rostoucí teplotou. Při vysoké teplotě však dochází k denaturaci (poškození) bílkoviny, která je součástí enzymu, a tím k inaktivaci celého enzymu. K maximu rychlosti proto dochází při optimální teplotě enzymu. Katalytický účinek enzymů působí při optimálním pH (většině enzymů vyhovuje pH 5 – 7, ale např. pepsin má optimální pH 1,5 - 2 nebo naopak arginasa má optimální pH 9,5). Změnou pH lze aktivitu ovlivňovat (využívají toho i živé buňky).
Katalytický účinek enzymů ovlivňuje řada látek, kterým říkáme efektory nebo modifikátory. Zvyšují-li aktivitu, hovoříme o aktivátorech. Snižují-li aktivitu, hovoříme o inhibitorech.