Významné výbušniny a jejich užití v praxi
Třaskaviny
Třaskavá rtuť Hg(CNO)2 fulminát rtuťnatý
Je bílá krystalická látka, ve vlhkém stavu málo citlivá, exploduje na slabý tepelný nebo mechanický podnět. Vyrábí se reakcí rtuti, ethanolu a kyselina dusičné.
Detonační rozklad: Hg(ONC)2 → Hg + 2 CO + N2 v = 6500 m/s, Q= – 1500 kJ/kg
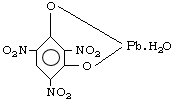
Azid olovnatý Pb(N3)2
Vytváří bílé až slabě narůžovělé krystalky; má vynikající roznětnou sílu a poměrně vysokou stabilitu. Je nejdůležitější třaskavinou ve výbušinářské technice. Je méně citlivý než fulminát, dává mohutnější detonační roznět.
Vyrábí se působením azidu sodného na vodný roztok dusičnanu olovnatého. Podobné vlastnosti má azid stříbrný Ag(N3), ale azid mědnatý je nebezpečný (velmi citlivý ke tření a k nárazu), dutinky proto nesmí obsahovat měď.
Detonační rozklad: Pb(N3)2 → Pb + 3 N2
Tricinát olovnatý (trinitrorezorcinát olovnatý) TNR
Hnědočervená látka, obvykle se používá ve směsích s třaskavou Hg nebo azidy, snadno se zapaluje a hoří dlouhým plamenem. Vyrábí se z trinitroresorcinátu hořečnatého a vodného roztok dusičnanu olovnatého. Je velmi citlivý vůči plamenu a elektrické jiskře, musí se chránit před účinky statické elektřiny.
Acetylidy - acetylid měďný Cu-C≡C-Cu a stříbrný Ag-C≡C-Ag
Detonační rozklad: Ag2C2 → 2 Ag + 2 C
Bertholetovo třaskavé stříbro Ag3N
Tato látka může vzniknout při Tollensově reakci.
Detonační rozklad: 3 [Ag(NH3)2]Cl → Ag3N + 3 NH4Cl + 2NH3
Jododusík NI3 * nNH3
Černo-zelená krystalická látka kovového lesku, je velmi citlivou třaskavinou, ale má relativně slabou výbušnou sílu. Používá se v zábavné pyrotechnice a to v množství pod 1 g. Při výbuchu vzniká růžovo-fialový kouř obsahující jód.
Střeliviny (střelné prachy)
Černý prach
Znali jej již v dávných dobách Číňané a Řekové, jako střelivina se používal od 14. století a od 17. století jako trhavina.
Složení: 75 % dusičnanu draselného, 15 % dřevěného uhlí, 10 % síry.
Schéma hoření (liší se podle podmínek): 2 KNO3 + S + 3 C → K2S + N2 + 3 CO2
10 KNO3 + 3S + 8C → 3K2SO4 + 2K2CO3 + 5N2 + 6CO2

Obr. 1: Různé granulace střelného prachu
Dnes se jako střelivina nepoužívá, používá se jako náplň zápalnice, k trhacím pracím v lomu, jako pomocná náplň nábojů, do dělostřelecké munice.
Bezdýmné prachy
v = 3800 – 7000 m/s; Q = - 2900 až - 4000 kJ/kg
Vyrábí se nitrací velmi čisté buničiny, nitruje se nitrační kyselinou, jejíž složení a poměr se mění podle požadovaného stupně nitrace. Výšenitrovaná celuloza se označuje jako střelná bavlna, níženitrovaná jako koloidní bavlna, ta se snadno rozpouští v řadě organických rozpouštědel. Nitroceluloza se želatinuje hnětením s těkavými rozpouštědly. Nitrocelulóza se zpočátku rozpouštěla v organických rozpouštědlech (ether, aceton), po jejichž odpaření vznikne „blána“, hořící pomaleji. Po zformování zrna se těkavá rozpouštědla odpaří a vzniká nitrocelulozový prach. Roku 1888 A. Nobel navrhl rozpouštět nitrocelulózu v „nitroglycerínu“ (vznikl tzv. „balistit“), takže běžná hlaveň děla „vydržela“ až 1700 výstřelů; přídavkem „nitrodiglykolu“ se výdrž zvýšila až přes 10 000 výstřelů.
Vyrobený prach se expeduje ve formě malých šupinek či destiček nebo se lisuje do tyčinek. Pokud se použije nitroglycerol, zůstává trvalou složkou - tzv. nitroglycerinový prach, hmota se tvaruje lisováním, válcováním a řezáním na různé tvary.
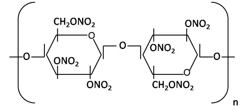
Trinitrát celulózy – střelná bavlna
Více na: http://canov.jergym.cz/urbanski/u2/ch2a_92.htm
Trhaviny
Průmyslové trhaviny
Průmyslové trhaviny se vyrábějí ve tvaru válcovitých plastikových náložek, do nichž lze lehce vtlačit rozbušku, odpalují se elektricky nebo pomocí zápalnice.
Používají se hlavně dynamity, jejich hlavní složkou jsou nitráty, které jsou vhodným způsobem znecitlivěny, a černý prach.
Nitráty se vyrábějí esterifikací vícesytných alkoholů kyselinou dusičnou, výroba probíhá podobně jako nitrace aromátů. Chemická stabilita nitrátů je značně nižší než nitrosloučenin, jsou silnými výbušninami, mají větší obsah kyslíku než nitrolátky, takže tepelný efekt výbušného rozkladu esterů je větší než u nitrosloučenin se stejným počtem C a NO2. Jsou velice citlivé k nárazu a tření, pro dopravu a manipulaci je nutné je stabilizovat, výroby jsou automatizované a mají dálkové ovládání.
Trinitroglycerol (trinitrát glycerolu) CH2ONO2-CHONO2-CH2ONO2
v = 8000 m/s; Q = 6 380 kJ/kg
Bezbarvá až nažloutlá, olejovitá, jedovatá kapalina, tuhne při 8 °C, má vysokou citlivost, samotný se nedá používat, vždy se provádí desaktivace.
Vyrábí se působením bezvodé nitrační směsi (kyselina dusičná + kyselina sírová) na glycerol, postup je buď přetržitý nebo nepřetržitý, teplota nesmí překročit 25°C.
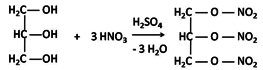
Výroba „nitroglycerolu“
Provádí se v olověném reaktoru, k míchání se používá stlačený vzduch, po esterifikaci se v separátoru oddělí nitroglycerol od těžší odpadní kyseliny a vypere se v pračce vodou a sodou do neutrální reakce.
Při výbušném rozkladu dochází k dokonalé oxidaci jeho uhlíku a vodíku vlastním kyslíkem podle rovnice:
4 CH2ONO2-CHONO2-CH2ONO2 →12 CO2 + 10 H2O + 6N2 + O2
Patří k výbušninám s pozitivní kyslíkovou bilancí.
Nobelův “ hlinkový dynamit “: 75 % trinitroglycerolu se sytí do hlinky - křemeliny 25%.
“Trhací želatina = želatinový dynamit “: nitroceluloza + trinitroglycerol + další látky (dusičnan sodný, dusičnan amonný,…).
Historická poznámka: Méně citlivý je rozpuštěný v methanolu, dříve se využívalo k znecitivění, na místě se do roztoku nalila voda a nitroglycerol vypadl v podobě oleje. Oddělil se a lil přímo do vyvrtaných děr, velmi nebezpečná manipulace. Náhodný objev (?): při rozbití nádoby nasákl nitroglycerol do křemeliny, která byla použita pro obložení převážených lahví, došlo k desaktivaci za současné zachováni brizance.
Dinitroglykol (dinitrát glykolu) CH2ONO2-CH2ONO2
Bezbarvá olejovitá kapalina, teplota tuhnutí - 22 °C, má o něco vyšší detonační rychlost než nitroglycerol, je o něco méně citlivý k nárazům, lépe se želatinuje. Vyrábí se esterifikací glykolu s použitím bezvodé nitrační směsi podobně jako probíhá výroba nitroglycerolu.
Rovnice výroby:
CH2OH-CH2OH + 2HNO3 ⇆ CH2ONO2-CH2ONO2 + 2H2O (dehydratační činidlo kyselina sírová)
Nemrznoucí dynamit - jeho základem dezaktivovný dinitrát glykolu.
Amonledkové trhaviny ( tzv. bezpečnostní) NH4NO3
Hlavní součástí je dusičnan amonný + příměsi aromatických nitrolátek a minerálního oleje, do důlních trhavin se přidávají tzv. chladící přísady (tyto látky spotřebují ke svému rozkladu a odpaření část výbuchového tepla). Mají poměrně malou citlivost k tření a úderu, nevýhodou je hygroskopičnost.
Údajná bezpečnost vede k lehkovážnému zacházení, např. 1921 v Oppau došlo ke katastrofě, 600 lidí zahynulo při odstřelu ztvrdlého ledku ve vagónu.
K průmyslovým účelům se dále používají: chlorátové směsi (chlorečnan a chloristan draselný).
Vojenské trhaviny
Používají se k plnění granátů, pum, min, náloží... Používají se i průmyslové výbušniny.
Nejpoužívanější jsou: tritol, hexogen, pentrit a řada směsí.
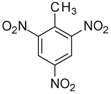
Tritol ( 2,4,6 – trinitrotoluen) TNT
Vzorec TNT
v = 7400 m/s; Q = 4000 kJ/kg
Nažloutlá, krystalická látka, teplota tání je 80,7 °C, ale již od teplot nad 35 °C se stává plastickou. TNT je velmi stabilní a málo citlivý vůči vnějším vlivům, ale zároveň se vyznačuje velmi vysokou brizancí a razancí výbuchu. Je ideální látkou pro přípravu vojenských i průmyslových trhavin. Z 1 kg vzniká 700 l plynu.
Jedná se o nejvýznamnější vojenskou trhavinu, slouží k vyjadřování účinku i ostatních trhavin. Tritolový ekvivalent je ukazatel mohutnosti účinků jaderné náplně. Je to množství energie uvolněné při jaderném výbuchu rovnající se energii uvolněné výbuchem příslušného množství tritolu. Uvádí se v tunách /t/, kilotunách /kt/ nebo megatunách /Mt/.
Používá se k plnění dělostřelecké munice, min, torpéd, bomb, granátů, používá se i do průmyslových trhavin.
Vyrábí se stupňovou nitrací toluenu, stupňovitá nitrace umožňuje racionálně hospodařit s kyselinami a zvyšovat čistotu tritolu čištěním produktů jednotlivých stupňů. V současné době se dává přednost dvoustupňové výrobě.
Složení nitrační směsi: 1. stupeň 40-60 °C 28 % k.dusičné, 56 % k. sírové, 16 % vody.
2. stupeň 60-90 °C 32 % k.dusičné, 61 % k.sírové, 7 % vody.
Odpadní kyselina z 2. stupně je po úpravě koncentrovanou k.dusičnou používána k nitraci v 1. stupni, kde vzniká směs mono- a dinitro- derivátů, tato směs se po oddělení odpadní kyseliny donitruje v 2. stupni při teplotě 120 °C na konečný produkt nitrační směsí připravenou z 20 % olea a 98% k.dusičné.
Surový TNT se vypráním zbavuje kyselin a podrobuje se rafinaci (sulfitová rafinace roztok siřičitanu sodného), vedlejší zplodiny částečně denitrují a přecházejí do roztoku jako rozpustné nitrosulfany.
Rozklad probíhá podle rovnice:
2 C7H5N3O6(s) → 7 C (s) + 7 CO(g) + 5 H2O(g) + 3N2(g)
Pro vysokou toxicitu výbuchových plynů není použitelný k trhacím pracím v uzavřených prostorech.
Hexogen (1,3,5-trinitro-1,3,5-triazacyklohexan, cyklotrimethylentrinitramin)
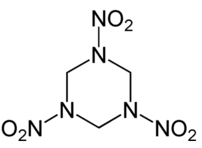
Vzorec hexogenu
Krystalická látka, chemicky velmi stabilní, vysoce brizantní, nereaguje s kovy, zředěnými minerálními kyselinami a hydroxidy. Výše koncentrovaná (nad 70 %) kyselina sírová ho rozkládá, proto nelze používat při jeho výrobě nitrační směs.
Vyrábí se nitrolýzou hexamethylentetraaminu (urotropinu) bezvodou kyselinou dusičnou nebo reakcí s dusitanem:
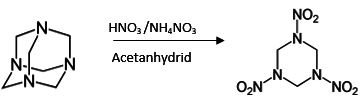
urotropin (hexamethylentetramin) hexogen (1,3,5-trinitro-1,3,5-triazocyklohexan)
Výroba hexogenu
Používá se jako protipancéřová munice, k výrobě bleskovnic (bleskovnice slouží ke spojení a odpálení většího počtu náloží).
Rozklad probíhá podle rovnice:
C3H6N6O6(s) → 3 CO(g) + 3 H2O(g) + 3N2(g)
Pentrit - pentaerytrittetranitrát C(CH2ONO2)4 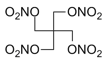
Bílá krystalická látka s teplotou tání 141,4 °C (při této teplotě se také samovolně explozivně rozkládá). Velmi brizantní, dost citlivý (méně ale než nitroglycerol), citlivost k tření není vysoká, ale je velmi citlivý k iniciaci detonací (stačí 0,01 g azidu olovnatého).
Vyrábí se esterifikací pentaerytritolu nadbytkem dýmavé 99% k. dusičné za silného chlazení:
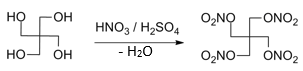
C(CH2OH)4 + 4HNO3 → C(CH2ONO2)4 + 4H2O
Používá se jako náplň rozbušek, bleskovnice, trhací náplně.