Absorpční spektrum
Absorpční spektrum (nebo-li absorpční křivka) je grafické vyjádření závislosti absorbance na vlnové délce elektromagnetického záření, procházejícího přes roztok zkoumané látky.
Absorpční spektrum je kvalitativní charakteristikou látky – na základě změření absorpčního spektra můžeme identifikovat látku ve vzorku, případně potvrdit identitu látky.
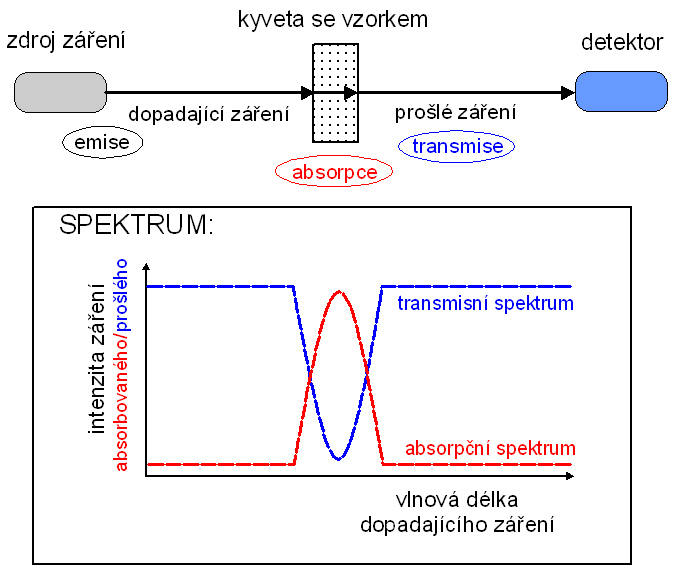
Obr. 1: Princip, na němž je založeno měření absorpčního/transmisního spektra
Změření spektra
Vhodný zdroj VIS záření produkuje paprsky různých vlnových délek, které nesou různá množství energie. Sledovaná složka vzorku, analyt, je schopna díky své chemické struktuře pohltit pouze fotony určité vlnové délky a tím se excitovat. Záření ostatních vlnových délek prochází přes vzorek beze změny. Při měření absorpčního/transmisního spektra posíláme na vzorek postupně záření z celé VIS oblasti a sledujeme, u kterých vlnových délek se projeví rozdíl v intenzitě dopadajícího a prošlého paprsku. Rozdíl můžeme vyhodnotit buď z hlediska transmise nebo z hlediska absorpce a zaznamenat jako transmisní spektrum nebo jako absorpční spektrum – v obou případech získáme jakýsi „otisk prstu“ analytu.
Absorpční spektrum se měří i v jiných oblastech elektromagnetického spektra, např. UV nebo IR.
Interpretace spektra
Na každé absorpční křivce sledujeme především počet a polohu absorpčních píků - poloha se určuje pomocí vlnové délky, při níž nastává buď výraznější nárůst absorbance nebo dokonce absorpční maximum, tj. nejvyšší dosažená absorbance. Polohu absorpčního maxima popisuje vlnová délka, kterou označujeme indexem max. Počet a poloha píků nezávisí na koncentraci látky v roztoku, pouze na jejím chemickém charakteru. Koncentrace látky ovlivňuje pouze velikost absorbance - výšku píků.
Pro hodnocení identity vzorku na základě absorpčního spektra je nutné, aby zkoumaná látka byla v čistém stavu. I malá příměs nečistot způsobí deformaci spektra. Toho lze naopak využít při hodnocení čistoty látek, u nichž známe jejich identitu.
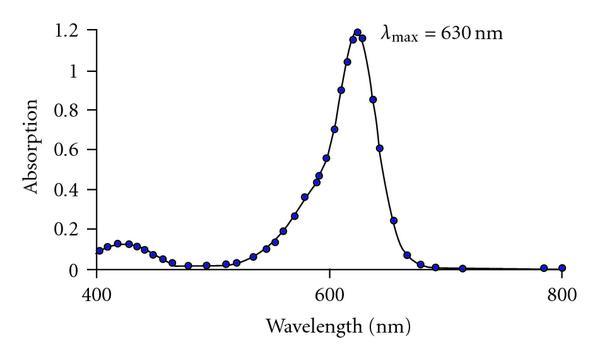
Obr. 2: Ukázka absorpčního spektra ve VIS oblasti
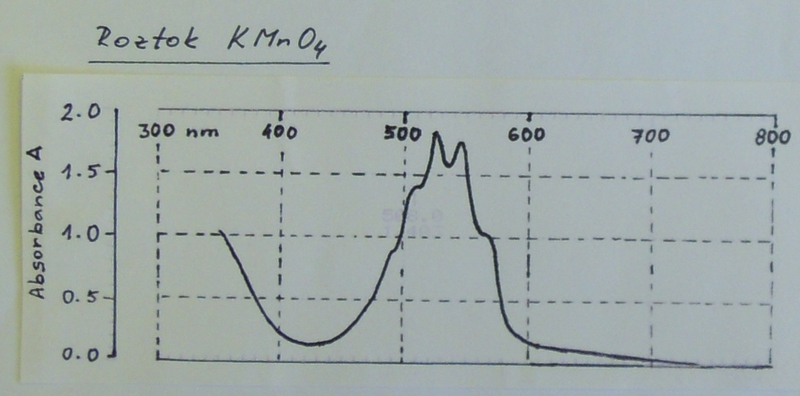
Obr. 3: Ukázka absorpčního spektra manganistanu draselného
Spektrum na obr.3 bylo změřeno na roztoku manganistanu draselného o koncentraci 0,8mmol/l. Maximální absorbance nastává při vlnové délce 525nm, další výrazný pík je při 545nm. Pokud bychom změřili roztok manganistanu draselného o jiné koncentraci, budou poloha píků a tvar spektra stejné, změní se pouze absolutní hodnoty absorbancí.
- KARLÍČEK, Rolf a kol. Analytická chemie pro farmaceuty. 1. vydání.Praha: Nakladatelství Karolinum, 2001 ISBN 80-246-0348-9
- OPEKAR, František a kol. Základní analytická chemie. 1. vydání. Praha: Nakladatelství Karolinum, 2005. ISBN 978-80-246-0553
Obrázky
- Obr. 1: Archiv autora
- Obr. 2: Autor neznámý. www.hindawi.com [cit. 24. 3. 2014] Dostupné z www: http://www.hindawi.com/journals/ijo/2009/371974/fig4/
- Obr. 3: Archiv autora
- Obr. 4: JANOUŠEK, Jiří. www.wikipedia.cz [cit. 16. 12. 2013] Dostupné z www: http://cs.wikipedia.org/wiki/Chlorofyl
- Obr. 5: Autor: TheTexasCichlidMasacre. www.perthcichlid.com [cit. 6. 5. 2014] Dostupné z www: http://www.perthcichlid.com.au/forum/index.php?app=members&module=reputation§ion=most
- Obr. 6: PRAHL, Scott. www.omlc.ogi.edu [cit. 14. 5.2014] Dostupné z www: http://omlc.ogi.edu/spectra/mb/
- Obr. 7: Autor neznámý. www.beafunmum.com [cit.16.5. 2014] Dostupné z www: http://beafunmum.com/2010/04/dare-to-paint/
Absorpční spektrum chlorofylu
Chlorofyl je přírodní barvivo, které díky absorpci viditelného záření umožňuje rostlinám syntetizovat sacharidy z oxidu uhličitého a vody. Chlorofyl absorbuje červené a modré záření, proto se jeví jako zelený a dodává zelené zbarvení rostlinám. Je známo několik typů chlorofylů lišících se chemickou strukturou.
Methylenová modř
Methylenová modř se užívá jako antidotum při otravě kyanidy, ve veterinární praxi jako antiseptikum. Další možnost jejího využití je jako reverzibilní redoxní indikátor, redukovaná forma je bezbarvá, oxidovaná forma je modrá.
Na milimetrový papír zakreslete VIS absorpční spektrum, které má tři píky a absorpční maximum při 480nm. Do obrázku zakreslete další spektrum téže látky, které však bylo získáno měřením roztoku látky o nižší koncentraci než první spektrum.
Svět je barevný, bohudík - experimenty i pro žáky ZŠ
Pracovní list do chemického kroužku pro žáky střední školy nebo i základní školy najdete v příloze - jednoduché experimenty s barvami a základní měření na spektrofotometru v oblasti viditelného záření.

Obr. 7: Hra s barvami
Měření absorbance barevných roztoků
Pracovní list k experimentu najdete v příloze. Každý barevný roztok absorbuje některou část záření z VIS oblasti a jeví se v doplňkové barvě k barvě tohoto absorbovaného záření. Porovnejte rozdíly v absorbanci různě zbarvených roztoků.