Chemické složení tiskových barev
Tisková barva je dvoufázová disperzní soustava, která je složena ze čtyř základních složek: pigmenty, pojiva, rozpouštědla, aditiva.
Složení tiskových barev
Suroviny pro výrobu tiskových barev lze rozdělit do 4 skupin:
Pigmenty a rozpustná barviva
Pigmenty jsou látky, které dodávají tiskovým barvám požadovaný barevný tón (nositelé barevnosti). Jde o látky schopné absorbovat/emitovat světlo. Jsou to nerozpustné složky barvy (částečky) rovnoměrně rozptýlené v pojivu. Velikost pigmentů je řádově několik µm nebo několik desetin µm.
Pigmenty mohou být anorganické (například oxidy kovů) nebo organické (např. azobarviva).
Rozpustná barviva jsou látky, které se zcela rozpustí v rozpouštědle a pojivu, vytvoří roztok. Mají nižší sytost a menší odolnost proti chemickým vlivům. Používají se jako přísady k pigmentům a korigují původní barevný odstín tiskové barvy (krášlidla).
Zvláštní skupinou pak mohou být barviva přírodní (karotenoidy – v mrkvi, rajčatech, květech rostlin; chlorofyl – v zelených listech; xantofyly – ve žlutých listech nebo také červené krevní barvivo hemoglobin).
V tiskových barvách jsou typickou barevnou složkou pigmenty. Na jejich částicích dochází k absorpci a rozptylu světla. Výsledný efekt je značně ovlivněn velikostí částic pigmentu i povahou potiskovaného materiálu. Hlavními požadovanými vlastnostmi pigmentů jsou obvykle barvivost, barevná stálost a velikost částic.
Na změnu barvy má značný vliv UV záření. Stálost vůči UV záření se požaduje především pro pigmenty UV barev a barev vystavených slunečnímu záření. Velikost částic pigmentů by měla být podstatně menší než je tloušťka suchého barvového filmu, která v závislosti na tiskové technice dosahuje hodnot asi od 1 μm (u ofsetového tisku) do desítek μm (u sítotisku).
Průměrná velikost částic anorganických pigmentů je 0,5-5 μm, organických 0,01-1 μm.
Pigmenty dělíme:
-
podle chemické povahy:
-
anorganické
-
organické
-
-
podle barevnosti:
-
bílé
-
černé
-
pestré
-
kovové.
-
ANORGANICKÉ PIGMENTY
Anorganické pigmenty se získávají z přírodních látek. Jejich význam v posledních letech klesl a v současnosti jsou nahrazovány nejedovatými organickými pigmenty. Svůj význam si udržely pouze bílé a černé pigmenty, ostatní se používají jen omezeně.
Bílé pigmenty
Bílé pigmenty jsou základní složkou bílé barvy. Jednotlivé pigmenty se liší ve svých vlastnostech a také v ceně. Navíc je lze použít ke snížení sytosti barvy a na úpravu tiskových vlastností. Lze rozlišit krycí nebo transparentní bílé barvy – u krycích potiskovaný materiál získává barvu krycí běloby, transparentní naopak vytváří průhlednou vrstvu. Mezi nejpoužívanější bílé pigmenty patří:
Titanová běloba (TiO2 - oxid titaničitý)
Obr. 1: Titanová běloba
První z bělob je jedním z nejlepších krycích pigmentů s typickým čistým bílým tónem. Titanová běloba má vysokou krycí schopnost a je odolná vůči působení kyselin a vysoké teplotě. Používá se do nátěrových hmot, smaltů, v kosmetice, farmacii i potravinářství.
Je nenahraditelná v chemicky odolných nátěrech. Nevýhodou může být vysoká cena.
Zinková běloba (ZnO - oxid zinečnatý)
Obr. 2: Zinková běloba
Zinková běloba je další významný bílý pigment, který však nedosahuje tak vysokých kvalit jako běloba titanová. Zinková běloba má nižší krycí schopnosti, je méně odolná vůči vysokým teplotám. Její vrstvy jsou tvrdé a málo pružné. Používá se do venkovních nátěrových barev, protože je na světle stálejší než většina jiných bělob.
Olovnatá běloba (PbCO3·2Pb(OH)2 - směs uhličitanu a hydroxidu olovnatého)
Tento pigment se využíval již ve 4. stol. př. n. l. Vzhledem k jeho toxicitě (nebezpečí otrav) se používá hlavně na venkovní nátěry, které dokáží odolat nepříznivým povětrnostním podmínkám. Dále je používána pro nátěry mořských lodí, a to díky antikorozním vlastnostem.
Barytová běloba (BaSO4 - síran barnatý) neboli BLANC FIXE
Obr. 3: Barytová běloba
Jde o na světle velmi stálý bílý pigment, který je odolný vůči působení kyseliny a zásad. Díky své chemické odolnosti je vhodnou příměsí do jiných pigmentů. Není jedovatá.
Hydroxid hlinitý (Al(OH)3)

Obr. 4: Hydroxid hlinitý
Hydroxid hlinitý je transparentní bílý pigment, který při tisku vytváří průhlednou vrstvu (opačně od ostatních). Lze jej použít pro všechny typy tisku.
Mezi bílé pigmenty lze také zařadit uhličitan vápenatý (CaCO3), uhličitan hořečnatý (MgCO3), kaolinit či sádru.
Černé pigmenty
Černé pigmenty jsou v polygrafickém průmyslu nezbytné. Mezi černé pigmenty patří:
Saze (kopt)
Saze jsou základním pigmentem pro výrobu černých barev, přestože mají nahnědlý tón. Saze jsou ve skutečnosti amorfní uhlík, který vzniká nedokonalým spalováním látek obsahujících uhlík (zemní plyn, methan, …). Saze mají výborné tiskové vlastnosti – jsou stálé na světle i teple, jsou odolné vůči působení kyselin a zásad. Pro zvýraznění barvy se přidávají například modré pigmenty (krášlidla).
Obr.5: Saze
Manganová čerň (MnO2 – oxid manganičitý) - burel - patří také mezi černé pigmenty.
Pestré pigmenty
Mezi pestré pigmenty řadíme barevné pigmenty – červené, žluté nebo například modré. Používají se pouze v omezeném množství,
a to z důvodu obsahu těžkých kovů, které jsou nebezpečné pro životní prostředí.
Žluté pigmenty:
Chromová žluť – žlutý/žlutooranžový pigment s dobrou krycí schopností (PbCrO4 s příměsí PbSO4). Všechny sloučeniny obsahující šestimocný chrom mohou mít karcinogenní účinky!!
Kadmiová žluť – CdS

Obr. 6: Kadmiová žluť
Barytová žluť (BaCrO4)
Uranové žlutě – jako pigmenty (Na2U2O7) byly sloučeniny uranu ve větším množství průmyslově vyráběny od roku 1852 v Jáchymově. Šlo o škálu odstínů žlutých, oranžových i červených odstínů, které se využívaly pro barvení skla a v keramických glazurách. Dnes je jejich použití omezeno. Pod UV zářením fosforeskují.
Červené pigmenty:

Obr. 7: Oxid železitý
Červené okry (Fe2O3 - oxid železitý) – přírodní hydratované a nehydratované oxidy trojmocného železa se používaly jako pigmenty již ve starší době kamenné. Zajímavé je, že odstín pigmentu závisí na stupni hydratace daného oxidu – bezvodý oxid je tmavě hnědočervený a zcela hydratovaný oxid pak žlutý. Jde o velmi stálé pigmenty s vysokou krycí schopností. Jsou netoxické. Užití pigmentů na bázi železa je široké – uplatnění našly například ve stavebnictví (barvy pro stavební materiály – omítky, cihlářské výrobky), jako nátěry kovů, příměsi do plastů, glazur, kosmetiky a jiných.

Obr. 8: Oxid olovnato-olovičitý
Minium (Pb3O4 – oxid olovnato-olovičitý), jiným názvem také suřík, byl používán již před naším letopočtem. Vyniká výbornou adhezí ke kovům, proto je využíván na nátěry střech nebo jako základní nátěr na ocel.
Modré pigmenty:
Ultramarín (NaAl (SO3)2)
Azurit (Cu3(CO3)2(OH)2)
Měďnaté modře - pigmenty na bázi mědi (různé směsi hydroxidů, uhličitanů a organických sloučenin mědi).
Kobaltová modř (CoO · Al2O3 ) - pigment s malou krycí schopností, používá se do keramických glazur.
Manganová modř (BaMnO4 · BaSO4) - stálý pigment odolný vůči vysokým teplotám.
Pařížská modř (K4[Fe(CN)6] - hexakyanoželeznatan draselný) - známá umělecká modř.
Zelené pigmenty:

Obr. 9: Chromová zeleň
Chromová zeleň (Cr2O3 - oxid chromitý)
Kovové pigmenty:
Kovové pigmenty se používají k imitaci odstínů drahých kovů – stříbrných a zlatých.
Zlaté pigmenty – v těchto pigmentech je obsažena mosaz – slitina mědi a zinku (podle obsahu Cu jsou pak zlaté pigmenty světle žluté až načervenalé).
Stříbrné pigmenty – jsou tvořeny čistým hliníkem (jemný hliníkový prášek).
ORGANICKÉ PIGMENTY
Jako koloranty pro tiskové barvy se uplatňují také organické pigmenty. Organické pigmenty jsou chemické sloučeniny odvozené od aromatických uhlovodíků (benzen, naftalen, anthracen), ale mohou to být také sloučeniny kovů (Cu, Cr, Co, apod.).
Chemická struktura organických pigmentů obsahuje skupiny atomů schopné selektivně absorbovat světlo - tzv. CHROMOFORY a dále skupiny zvané AUXOCHROMY, které žádanou barvu zesilují.
K typickým chromoforům organických pigmentů patří nenasycené skupiny jako:
- azoskupina -N=N-
- karbonylová skupina C=O
Jako auxochrom v organických pigmentech působí:
- hydroxylová skupina - OH
- aminoskupina - NH2
- sulfoskupina - SO3H
- halogeny - Cl, - Br …
- nitroskupina - NO2
SYNTETICKÁ ORGANICKÁ BARVIVA
Syntetická barviva jsou uměle (synteticky) vyráběná organická barviva (pigmenty).
Azobarviva
Azobarviva jsou po chemické stránce azosloučeniny – tedy deriváty uhlovodíků, které obsahují charakteristickou funkční skupinu:
– N = N –
azoskupina
Azobarviva jsou nejpočetnější a nejdůležitější skupinou organických barviv, zahrnující všechny odstíny od žluté až do černé. Azobarvivy je možno barvit téměř všechny druhy přírodních, chemických a syntetických vláken, plastů, usní, papíru, výrobků z pryže. Nevýhodou může být jejich jedovatost, takže jsou nepoužitelné pro dobarvování potravin.
Příklady azobarviv:

Obr. 10: Methylčerveň

Obr. 11: Methyloranž Oranž II

Obr. 12: Kongo červeň
Příprava azobarviv: Výchozí surovinou pro přípravu azobarviv bývá anilin. Ten se nejprve diazotací (reakcí s kyselinou dusitou) převede na odpovídající diazoniovou sůl, ze které se pak připraví příslušná azosloučenina.
Chinonová barviva
Barviva fialová, zelená i světle žlutá.
Arylmethanová barviva
Malachitová zeleň
Fenolftalein. Fenolftalein patří mezi tzv. acidobazické indikátory. Tato látka je různě zbarvena v prostředí o různém pH. V alkalickém prostředí je fenolftalein zbarven jasně červenofialově, v kyselém a neutrálním prostředí je bezbarvý.
Obr. 13: Fenolftalein
Indolová barviva
Do této skupiny patří známé barvivo Indigo (modré barvivo). Jsou odvozené od heterocyklické sloučeniny indolu.
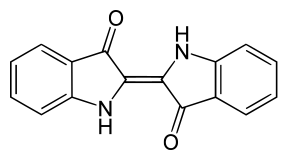
Obr.14: Indigo
Obr.15: Indol
Ftalocyaninová barviva
Přírodní velmi stálé pigmenty zahrnující širokou škálu barev – od modré, až po zelenou. Používají se pro hlubotisk, ofset a flexotisk. Zajímavostí může být, že ve své struktuře nesou kov (Cu, Ni, Co).
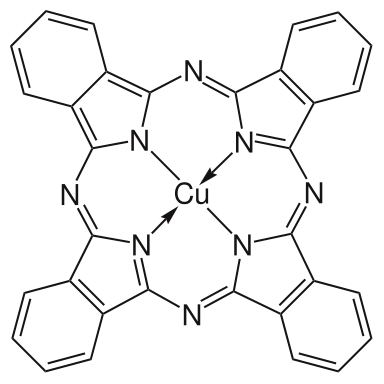
Obr.16: Ftalocyanin mědi
Chinakridonová barviva
Červené a červenofialové barviva. Slouží k barvení tkanin a umělých materiálů.
Další organická barviva:
Fanálová barviva, Azinová barviva, Oxazinová barviva, Thioazinová barviva, Sirná barviva
Pro příklad uvádíme pigmenty používané pro čtyřbarvotisk (CMYK model):
-
pro azurovou (Cyan) – ftalocianinové pigmenty
-
pro purpurovou (Magenta) – chinakridonová červeň
-
pro žlutou (Yellow) – diarylová žluť
-
pro černou (Key) – saze + krášlidla.
Filmotvorné látky – POJIVA
Pojiva neboli filmotvorné látky jsou důležitou součástí tiskových barev. Pojivo váže dispergované (rozptýlené) částice – pigmenty a plniva, zajišťuje stabilitu celého systému, umožňuje přenos barvy v procesu tisku a nakonec vytváří spojitou fázi nánosu barvy (pružný film), které pevně ulpívá na potiskovém materiálu. Základem pojiv jsou filmotvorné látky, schopné při vhodném způsobu aplikace vytvářet kompaktní hladké povlaky požadovaných vlastností (pružnost, přilnavost, tvrdost atd.). Součástí pojiva mohou být
i další rozpuštěné netěkavé látky (např. změkčovadla).
Filmotvorné látky dělíme na:
Vysychavé oleje
Vysychavé oleje jsou oleje přírodního původu, chemicky definované jako estery glycerolu s nenasycenými vyššími mastnými kyselinami. Oleje lze získat lisováním a extrakcí olejů z plodů či semen rostlin, přičemž nejvýznamnějším zástupcem vysychavých olejů je olej lněný. Oleje se dále zahušťují za vzniku fermeží (polyesterů), které se využívají také jako filmotvorné látky. Vysychavé oleje se používají při výrobě ofsetových a knihtiskových barev.
Přírodní pryskyřice
Další filmotvorné látky – pryskyřice – získáváme zpracováním rostlinných a živočišných silic. Nejčastěji se používá kalafuna (destilační zbytek pryskyřic borovice) – hlavní složkou je zde kyselina abietová. Mezi pryskyřice dále patří: damarová pryskyřice, jantar, dříve se používal také šelak.
Syntetické pryskyřice
Uměle vyrobené pryskyřice nahrazují obtížně dostupné přírodní pryskyřice. Jde o estery celulózy, deriváty kaučuku, epoxidové pryskyřice a jiné. Syntetické pryskyřice se proti přírodním vyznačují lepšími vlastnostmi.
Asfalty a smoly
Asfalty a smoly jsou produkty ropné destilace, které se přidávají do barev tmavých tónů.
Rozpouštědla
Rozpouštědla přidávaná do tiskových barev jsou zpravidla organické kapaliny, ve kterých se dobře rozpouští pojivo ale i další složky barvy. Společně pak vytvářejí stabilní systém s určitými vlastnostmi. Výběr rozpouštědla pro tiskové barvy je ovlivněn toxikologickými, hygienickými a ekologickými aspekty, přičemž důraz je kladen také na vhodný výběr rozpouštědla pro jednotlivé tiskové formy. Procento zastoupení rozpouštědla v tiskových barvách je v rozsahu od 20-65 %.
Pomocí rozpouštědel (ředidel) lze tedy upravit tekutost barvy, potažmo její viskozitu a také rychlost jejího schnutí. Ředidlo vždy vybíráme podle jeho rozpouštěcí schopnosti pro použité pojivo i pro další složky tiskové barvy. V praxi se často využívá kombinace několika rozpouštědel.
Rozpouštědla se z tiskové barvy uvolňují dvěma možnými způsoby: vsáknutím či těkáním (odpařením).
Rozpouštědla dělíme na:
-
anorganická
-
organická.
Nejvýznamnějším anorganickým rozpouštědlem je voda. Je také nejvhodnějším rozpouštědlem z hlediska bezpečnosti a zdravotní nezávadnosti. Voda má však omezené rozpouštěcí schopnosti. Používá se v případech, kdy se tisková barva připravuje na bázi disperzí polymerů (vodou ředitelné barvy).
Mezi organická rozpouštědla patří:
-
alifatické uhlovodíky – alkany, cykloalkany, benzíny, petroleje
-
aromatické uhlovodíky – benzen, toluen, xylen
-
alkoholy – ethanol, izopropylalkohol
-
aldehydy a ketony – aceton
-
estery a étery – ethylacetát.
Organická rozpouštědla jsou hořlavé a výbušné látky s výrazným zápachem. Jde o látky těkavé, které mohou ohrozit zdraví člověka.
Příklady organických rozpouštědel:

Obr. 17: Aceton

Obr. 18: Ethanol

Obr. 19: Toluen
Ostatní látky – ADITIVA
Aditiva jsou látky, které významně ovlivňují určité vlastnosti barev, ačkoliv jejich obsah je zpravidla nízký (desetiny až jednotky procenta). Pomocí aditiv lze ovlivnit viskozitu, tažnost, lepivost nebo rychlost schnutí tiskové barvy.
Mezi aditiva patří:
-
vosky (odolnost proti otěru, kluznost)
-
sušidla = sikativa (zasychání)
-
povrchově aktivní látky = tenzidy (smáčedla)
-
přípravky snižující lepivost (vosky, parafín)
-
zvláčňovadla (vláčnost a pružnost, zvýšení lesku).
Dále látky proti prášení, odpěňovače, biocidy či deodoranty.
-
KAPLANOVÁ, Marie. Moderní polygrafie. Praha: Svaz polygrafických podnikatelů, 2010, 391 s. ISBN 978-80-254-4230-2.
-
LEDERLEITNER, Milan, Jozef HAMAR a Vladimír THOMKA. Polygrafické materiály pro 1.-3. ročník SOU. 1. vyd. Překlad Zdeněk Niepel. Praha: SPN, 1990, 93 s. Učebnice pro stř. školy. ISBN 80-042-4132-8.
-
PŘIKRYLOVÁ, Eva. Tiskové barvy (DUMY). Dostupné v archivu autora. Materiál vznikl v rámci projektu Kvalitní a efektivní vzdělávání pro žáky (DUMY)/ VY_32_INOVACE_02 (číslo projektu: CZ.1.07/1.5.00/34.0772)
-
Pigmenty a barviva. [online]. [cit. 2014-07-01]. Dostupné z: http://geologie.vsb.cz/loziska/suroviny/pigmenty_barviva.html#ZELENÁ
-
Wikipedie. Otevřená encyklopedie. [online]. [cit. 2014-07-01]. Dostupné z: https://cs.wikipedia.org/wiki
Obrázky:
- Obr. 1: Mangl, Ondřej. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/3/3a/Oxid_titani%C4%8Dit%C3%BD.PNG/220px-Oxid_titani%C4%8Dit%C3%BD.PNG
- Obr. 2: Mangl, Ondřej. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/b/ba/Oxid_zine%C4%8Dnat%C3%BD.PNG
- Obr. 3: Mangl, Ondřej. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/7/7b/S%C3%ADran_barnat%C3%BD.PNG/250px-S%C3%ADran_barnat%C3%BD.PNG
- Obr. 4: Mangl, Ondřej.http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/a/a9/Hydroxid_hlinit%C3%BD.PNG/240px-Hydroxid_hlinit%C3%BD.PNG
- Obr. 5: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/9/98/Carbon_black.jpg
- Obr. 6: Oelen, W. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/0/0e/Cadmium_sulfide.jpg
- Obr. 7: Autor neznámý. http://cs.wikipedia.org/wiki/. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/e/ee/Iron%28III%29-oxide-sample.jpg/800px-Iron%28III%29-oxide-sample.jpg
- Obr. 8: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/a/ae/Red_lead.jpg/800px-Red_lead.jpg
- Obr. 9: Autor neznámý. http://cs.wikipedia.org/wiki/. 800px-Chromium%28III%29-oxide-sample.jpg. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/3/34/Chromium%28III%29-oxide-sample.jpg/800px-Chromium%28III%29-oxide-sample.jpg
- Obr. 10: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/b/b4/Methyl_red.svg/364px-Methyl_red.svg.png
- Obr. 11: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/5/54/Methyl-orange-2D-skeletal.png
- Obr. 12: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/c/c9/Congo-red-2D-skeletal.png
- Obr. 13: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/0/01/Fenolftaleina_struttura.PNG
- Obr. 14: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/2/22/Indigo_skeletal.svg/287px-Indigo_skeletal.svg.png
- Obr. 15: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/0/02/Indol2.svg
- Obr. 16: Werk Eigenes. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/e/ec/Copper_phthalocyanine.svg/384px-Copper_phthalocyanine.svg.png
- Obr. 17: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/b/ba/Aceton.png
- Obr. 18: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/b/be/Ethanol_Lewis.svg/160px-Ethanol_Lewis.svg.png
- Obr. 19: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/2/2e/Toluol.svg/70px-Toluol.svg.png
- Obr. 20: Bauer, Scott. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/9/9a/Tomato_slices.jpg
- Obr. 21: Peters, Kristian. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/4/49/Plagiomnium_affine_laminazellen.jpeg
- Obr. 22: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/1/13/Redbloodcells.jpg
- Obr. 23: Baum, Modris. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/5/58/Ilmenite-173863.jpg/640px-Ilmenite-173863.jpg
- Obr. 24: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/7/79/Diesel-smoke.jpg
- Obr. 25: Dulyan, Aram. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/5/5d/Pyrolusite_radiating.jpg
- Obr. 26: Descouens, Didier. http://cs.wikipedia.org/wiki/. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/7/77/Lazurite.jpg/640px-Lazurite.jpg
- Obr. 27: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/6/67/Ultramarinepigment.jpg
- Obr. 28: Rubashkyn. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/9/9f/Methyl_orange_02035.JPG/1024px-Methyl_orange_02035.JPG
- Obr. 29: Autor neznámý. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/7/70/Olej_lniany.jpg/640px-Olej_lniany.jpg
- Obr. 30: Mills, Ben. http://cs.wikipedia.org/wiki/. [online]. [cit. 2014-10-28]. Dostupné z: http://upload.wikimedia.org/wikipedia/commons/thumb/e/ec/Acetone-3D-vdW.png/640px-Acetone-3D-vdW.png
Červená krvinka čili erytrocyt (z řec. erythros – červený a kytos – buňka) je nejběžnější krevní buňka. Její funkcí je zejména přenášení kyslíku z plic nebo žaber do ostatních tělních tkání. Obsahují červené krevní barvivo hemoglobin, které váže kyslík.
... že přírodní oxid titaničitý se nevyskytuje jako čistý. Většinou bývá kontaminován ionty jiných kovů, například železa. Přírodní minerály oxidu titaničitého jsou průmyslově těženy jako zdroj titanu. K dalším zrojům titanu patří rudy obsahující ilmenit nebo leukoxen či písky s obsahem rutilu.
Většina ilmenitu je užita k výrobě bílého pigmentu (titanové běloby) – oxidu titaničitého TiO2 - reakcí s kyselinou sírovou za vzniku zelené skalice (FeSO4·7H2O):
FeTiO3 + H2SO4 → FeSO4 + TiO2 + H2O

Obr. 23: Ilmenit
... síran barnatý se často využívá v klinické praxi jako radiokontrastní látka pro rentgenové zobrazování nebo jiné diagnostické procedury. Týká se to zejména zobrazování zažívacího ústrojí, při kterém se kolokviálně hovoří o „baryové suspenzi“.
Podává se orálně nebo klystýrem jako suspenze jemných částic ve vodném roztoku (často oslazeném). Přestože baryum patří mezi těžké kovy a jeho ve vodě rozpustné sloučeniny jsou prudce jedovaté, extrémně nízká rozpustnost síranu barnatého znemožňuje, aby pacient vstřebal škodlivá množství kovu. Síran barnatý je také snadno odstraňován
z těla, na rozdíl od Thorotrastu, který ho nahrazuje. Vzhledem k poměrně vysokému atomovému číslu
(Z = 56) barya pohlcují barnaté sloučeniny rentgenové záření silněji než sloučeniny s lehčím jádrem.
Saze vznikají zvláště při spalování na uhlík bohatých organických paliv za nedostatku kyslíku. Hromadí se v komínech, automobilových výfucích (hlavně
u automobilů se vznětovým /dieselovým/ motorem)
a dalších površích vystavených kouři.

Obr. 24: Nákladní automobil se vznětovým motorem bez filtru pevných částic vypouští oblak sazí
Saze byly užívány jako černé barvivo v barvách a inkoustech již od prehistorických časů a jsou ještě široce používány v tiskařských inkoustech, tonerech pro xerografii, laserových tiskárnách a v chemickém průmyslu. Jsou také využívány jako potravinářské barvivo, například lékořicové bonbóny.
Nejdůležitějším způsobem využití je jako plnivo kaučukových pneumatik. Toto použití spotřebuje 85 % průmyslově vyrobených sazí.
Barviva jsou chemické látky, které mění barvu odraženého světla, což je způsobeno selektivním pohlcováním určitých vlnových délek. Výsledná barva je dána spektrem odražených vlnových délek světla.
Pigment je obvykle nerozpustný v pojivu, zatímco barvivo je buď přímo kapalné, nebo je v pojivu rozpustné.

Obr. 26: Ultramarín
Ultramarín – (Na,Ca)8[(S,SO4,Cl2)|Al6Si6O24]
Minerál lazurit (či ultramarín) se jako pigment využívá už déle než 2 tisíce let. Protože jde o poměrně vzácný minerál, byl odedávna přírodní ultramarín velmi drahý. To také způsobilo hledání levnějších náhrad. Syntetický ultramarín stejného chemického složení jako lazurit se vyrábí od roku 1828. Podobně jako přírodní materiál je také nestálý v kyselém prostředí.

Obr. 27: Syntetický ultramarín
Dodnes je používán jako umělecký pigment ve třech barvách (načervenale modrá, fialová a růžová), hodí se i pro barvení cementových výrobků a omítek. Další příklady pestrého využití jsou plasty, tiskařské inkousty, kosmetika a hračky.
CHROMOFOR (chromoforní skupina) je část sloučeniny – skupina, která způsobuje
absorpci světla v UF a viditelné oblasti světelného spektra. Např. –N=N− ; =C=O;
=C=C= ; −C≡N
AUXOCHROM (auxochromní skupina) je charakteristická skupina, která v blízkosti
chromoforů způsobuje rovněž posun absorpce světla, což se zpravidla projeví změnou barvy
nebo jejího odstínu. Jako auxochromy se projevují různé zásadité i kyselé skupiny.
Např. –OH ; −OCH3 ; −NHR ; −NR2 ; −NO2 ; −SO3H ; −COOH
Methyloranž (4´-(N,N-dimethylamino)azobenzen-4-sulfonová kyselina) je azobarvivo často používané jako pH indikátor při titracích. Methyloranž je díky jasné změně barvy často voleným indikátorem pro titrace. Protože mění barvu při pH v oblasti středních kyselin, používá se obvykle pro titraci kyselin.
Když se roztok stává méně kyselý, methyloranž mění svou barvu z červené na oranžovou a následně na žlutou; s rostoucí kyselostí je změna opačná. Je třeba poznamenat, že k celé této změně dochází v kyselém prostředí.
Diazotace (řečtina + latina) je chemická reakce, při které se na aromatické primární aminy působí směsí dusitanu a nadbytku anorganické kyseliny za vzniku diazoniové soli.
C6H5-NH2 + NaNO2 + 2 HCl → [C6H5-N≡N](+)Cl(-) + NaCl + 2 H2O
Reakce probíhá následujícím mechanismem:
- Reakcí dusitanu a kyseliny vzniká kyselina dusitá a sůl příslušné kyseliny:
NaNO2 + HCl → HNO2 + NaCl - Následuje rychlá protonizace kyseliny dusité:
HNO2 + H(+) → H2N(+)O2 - Dalším krokem je pomalá reakce tohoto činidla s primárním aminem za vzniku nitrosaminu:
Ar-NH2 + H2N(+)O2 → Ar-NH-NO + H(+) + H2O - Poté probíhá rychlá reakce přes diazohydroxid až na konečnou diazoniovou sůl:
Ar-NH-NO + H(+) → Ar-N=NO(+)H2 → [Ar-N≡N](+) + H2O
Vzniklé diazoniové soli slouží jako meziprodukt při výrobě například azobarviv, léčiv.
Barevná změna indikátoru: fenolftalein je dobře zachycena na:
http://www.youtube.com/watch?v=_rtx3ZMAoKQ
Co znamená v polygrafii CMYK?
Kombinaci 4 základních barviv (barev), ze kterých lze namíchat jakoukoliv jinou barvu.
Zopakuj si kapitolu: Barvy a jejich vnímání.
Lněný olej je čirý, žlutý olej získávaný ze sušených zralých semen lnu setého (Linum usitatissimum). Olej se získává lisováním za studena, někdy s následnou extrakcí rozpouštědlem.
Lněný olej je hlavním nosičem používaným v olejových barvách. Lze ho použít i jako přísadu, která činí barvy tekutější, průhledné a lesklé.
Je dostupný v různých variantách, např. lisovaný za studena, alkalicky rafinovaný, bělený na slunci, zahušťovaný na slunci nebo polymerizovaný („stand oil“). Používání lněného oleje bylo významným krokem v technologii olejových nátěrových hmot.
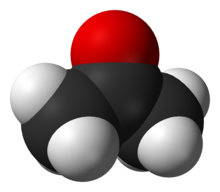
Obr. 30: Model molekuly acetonu
Aceton je základní surovinou chemického průmyslu. Využívá se při syntéze acetonkyanhydrinu, který působením kyseliny sírové přechází na methakrylamid sulfát. Tato sloučenina pak reaguje s methanolem za vzniku methylmetakrylátu - methylesterukyseliny akrylové. To je základní stavební prvek polymeru známého jako plexisklo. Aceton se také využívá na výrobu podpatků a podrážek a jiných gumových dílů obuvi.
Pamatujte, že vlastnosti tiskových barev, vyplývající z jejich složení, musí vyhovovat tiskové technice, pro kterou jsou určeny!
Jak se vyrábí barvy:
https://www.youtube.com/watch?v=Fypi6dAJB8E
Jak se tiskne metodou CMYK - sítotisk:
https://www.youtube.com/watch?v=KW0fLlbt5iA
Tisk pomocí vodního přenosu:
https://www.youtube.com/watch?v=-C12ESHq6mY
Jak se využívají barvy v designu nehtů:
https://www.youtube.com/watch?v=sbQ4X_-hnX4
