Chemické pokusy – praktické postupy
Zde se seznámíme s pracovními postupy vybraných chemických pokusů. Budou také uvedeny pomůcky a chemikálie potřebné k provedení daného pokusu, jeho princip, chemické rovnice a také bezpečnost při práci s potřebnými chemikáliemi.
Reakce kovů s kyselinou chlorovodíkovou
Pomůcky: stojan se zkumavkami, kahan
Chemikálie: kyselina chlorovodíková, kovy (mangan, zinek, měď, hořčík, železo, hliník atd.)
Postup: Zkumavky naplníme maximálně do poloviny zředěnou kyselinou chlorovodíkovou (1:2) a přidáme kousek kovu (manganu, zinku, mědi, hořčíku, železa a hliníku). Pokud některý kov reaguje velmi pomalu, reakční směs můžeme mírně zahřát. Rychlost reakce závisí také na velikosti povrchu kovu (práškový kov bude reagovat rychleji).
Princip: Vyplývá z Beketovovy řady.
Rovnice:
Mn + 2HCl → MnCl2+ H2
Zn + 2HCl → ZnCl2 + H2
Cu + HCl → neprobíhá
Mg + 2HCl → MgCl2 + H2
2Fe + 6HCl → 2FeCl3 + 3H2
2Al + 6HCl → 2AlCl3 + 3H2
Bezpečnostní pokyny: Při práci s kyselinou chlorovodíkovou je nutné používat ochranné rukavice a brýle. Ústí zkumavky při reakci odvrátit od sebe i od ostatních pracujících v laboratoři.

Obr. 1: Reakce kovů s kyselinou chlorovodíkovou. Zleva: železo, zinek, měď, hořčík, mangan a hliník.
Vytěsňování kovů s roztoků svých solí
Pomůcky: stojan se zkumavkami, kahan
Chemikálie: síran hořečnatý, síran zinečnatý, dusičnan olovnatý, síran měďnatý, kovy (hořčík, zinek, olovo, měď).
Postup: Zkumavky naplníme asi do poloviny roztoky solí a přidáváme hořčík, zinek, olovo a měď. Pokud reakce probíhá pomalu, můžeme reakční směs mírně zahřát.
Princip: Vyplývá z Beketovovy řady.
Rovnice:
MgSO4 + Cu → neprobíhá
MgSO4 + Pb → neprobíhá
MgSO4 + Zn → neprobíhá
ZnSO4+ Cu → neprobíhá
ZnSO4+ Pb → neprobíhá
ZnSO4+ Mg → Zn + MgSO4
Pb(NO3)2+ Cu → neprobíhá
Pb(NO3)2+ Mg → Pb + Mg(NO3)2
Pb(NO3)2+ Zn → Pb + Zn(NO3)2
CuSO4+ Pb → Cu + PbSO4
CuSO4+ Mg → Cu + MgSO4
CuSO4+ Zn → Cu+ZnSO4
Bezpečnostní pokyny: Při práci používáme ochranné rukavice a brýle.

Obr. 2: Vytěsňování kovů. Zleva: roztok MgSO4 postupně s Cu, Pb a Zn; roztok ZnSO4 postupně s Cu, Pb a Mg.

Obr. 3: Vytěsňování kovů. Zleva: roztok Pb(NO3)2 postupně s Cu, Mg a Zn; roztok CuSO4 postupně s Pb, Mg a Zn.
Reakce mědi s dusičnanem stříbrným
Pomůcky: Petriho miska
Chemikálie: měděný drát, dusičnan stříbrný
Princip: Vyplývá z Beketovovy řady.
Rovnice: 2AgNO3 + Cu => Cu(NO3)2 + 2Ag
Bezpečnostní pokyny: Při práci používáme ochranné rukavice a brýle.
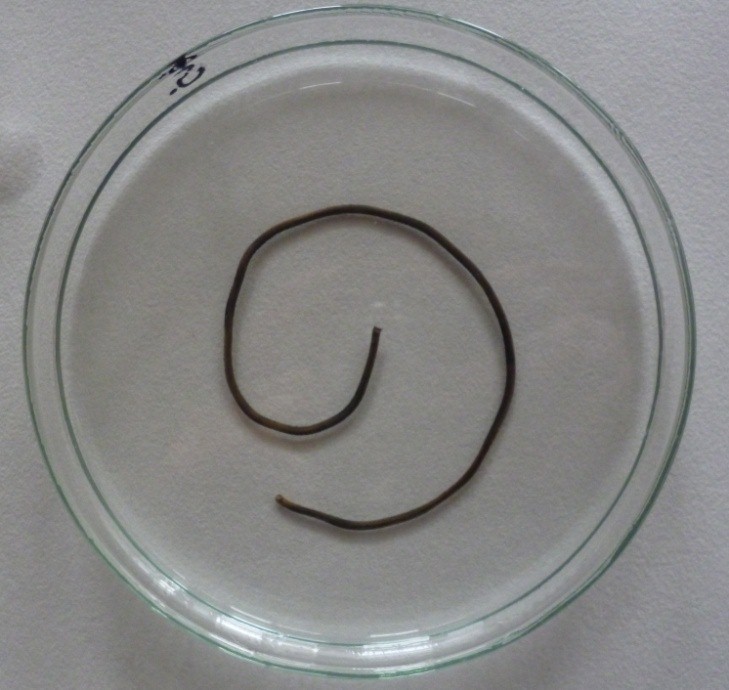
Obr. 4: Reakce mědi s roztokem dusičnanu stříbrného – začátek.

Obr. 5: Reakce mědi s roztokem dusičnanu stříbrného – po 30 minutách.
Příprava a důkaz kyslíku
Pomůcky: zkumavka, stojan na zkumavky, špejle, sirky
Chemikálie: peroxid vodíku, oxid manganičitý (burel)
Postup: Do zkumavky vložíme na špičku lžičky oxidu manganičitého a přidáme asi 1 ml 10% peroxidu vodíku. Vznikající kyslík je těžší než vzduch (má větší hustotu), a proto zůstává ve zkumavce. Dokážeme ho přiložením doutnající špejle.
Rovnice: H2O2 → H2O + O2 (katalyzátorem je burel)
Princip: Katalytický rozklad peroxidu vodíku, disproporcionace kyslíku v méně stabilním oxidačním čísle -I.
Bezpečnostní pokyny: Při práci s peroxidem vodíku používáme ochranné rukavice a brýle.

Obr. 6: Důkaz kyslíku zapálením doutnající špejle.
Hoření některých prvků v atmosféře kyslíku
Pomůcky: demonstrační nebo odměrný válec, kahan
Chemikálie: peroxid vodíku, oxid manganičitý (burel), síra, fosfor, práškové železo atd.
Postup: Kyslík připravíme podle výše uvedeného pokusu v demonstračním nebo odměrném válci. Práškové železo rozžhavíme ve lžičce nad kahanem a poté jej vložíme do válce nasyceného kyslíkem. Podobně můžeme zapálit také kousky roztavené síry, rozžhaveného uhlíku atd.
Rovnice: 3O2 + 4Fe → 2Fe2O3
Princip: Kyslík podporuje hoření.
Bezpečnostní pokyny: Při práci s peroxidem vodíku používáme ochranné rukavice a brýle. Při spalovaní prvků se chráníme ochranným štítem.

Obr. 7: Spalování práškového železa v atmosféře kyslíku.
Příprava a důkaz vodíku
Pomůcky: zkumavka, držák na zkumavky, špejle, sirky
Chemikálie: kyselina chlorovodíková, zinek
Postup: Do zkumavky vložíme pár kousků granulovaného zinku a přidáme asi 2 ml kyseliny chlorovodíkové zředěné vodou v poměru 1:1. Vodík jímáme do zkumavky obrácené dnem vzhůru, protože je lehčí (má menší hustotu) než vzduch. Po naplnění zkumavku ucpeme palcem a přiložíme k plameni.
Princip: Vyplývá z Beketovovy řady.
Rovnice: Zn + 2HCl → H2 + ZnCl2
Bezpečnostní pokyny: Při práci s kyselinou chlorovodíkovou používáme ochranné rukavice a brýle. Při důkazu vzniklého vodíku používáme ochranný štít.
Příprava chloru
Pomůcky: zkumavka, zátka, skleněná trubička
Chemikálie: kyselina chlorovodíková, manganistan draselný
Postup: Do zkumavky nasypeme špetku manganistanu draselného a přidáme asi 1 ml kyseliny chlorovodíkové. Ihned začne vznikat žlutozelený plyn – chlor.
Princip: Oxidace kyseliny chlorovodíkové manganistanem draselným.
Rovnice: 2KMnO4 + 16HCl → 5Cl2 + 2MnCl2 + 2KCl + 8H2O
Bezpečnostní pokyny: Při práci s kyselinou chlorovodíkovou používáme ochranné rukavice a brýle. Pracujeme v digestoři, chlor je jedovatý.
Příprava jodu
Pomůcky: zkumavka, zátka, skleněná trubička, proužek filtračního papíru
Chemikálie: kyselina chlorovodíková, manganistan draselný, jodid draselný
Postup: Podle výše uvedeného pokusu připravíme chlor. Proužek filtračního papíru namočíme do 5% roztoku jodidu draselného. Poté na navlhčené místo papírku zavádíme pomocí sklenění trubičky chlor. Vyloučí se jod.
Princip: Vzájemné vytěsňování halogenů.
Rovnice: Cl2 + 2KI → I2 + 2KCl
Bezpečnostní pokyny: Při práci s kyselinou chlorovodíkovou používáme ochranné rukavice a brýle. Pracujeme v digestoři, chlor je jedovatý.
