Příprava a výroba karbonylových sloučenin
Příprava a výroba aldehydů
Oxidace nebo dehydrogenace primárních alkoholů
Jako výchozí látky se obecně používají primární alkoholy. Průmyslově se provádí katalytická oxidace vzdušným kyslíkem např. za přítomnosti mědi, stříbra, směsných oxidů přechodných kovů; další průmyslově velmi využívanou variantou je dehydrogenace za katalytického účinku mědi nebo stříbra. Laboratorně se používá KMnO4 nebo K2Cr2O7:
R-CH2-OH → R-CH=O + H2O
primární alkohol aldehyd
Oxidace uhlovodíků
Z alkanů vzniká směs oxidačních produktů, významnější je oxidace v postranním řetězci arenů:
C6H5CH3 + O2 → C6H5CHO + H2O
Parciální oxidace ethenu (Wacker-Hoechstův způsob)
Moderní způsob výroby acetaldehydu, v současné době nejvýznamnější výroba. Oxidace probíhá v kapalné fázi, katalyzátor tvoří dvousložkový systém PdCl2 a CuCl2, vlastním katalyzátorem je PdCl2 , který tvoří komplexy s ethenem, CuCl2 slouží k obnovení katalyzátoru:
CH2 = CH2 + PdCl2 + H2O → CH3 - CH=O + Pd + 2HCl
Pd + 2CuCl2 → PdCl2 + 2CuCl
2CuCl + 2HCl + 1/2 O2 → 2CuCl2 + H2O
Speciální postupy - Kučerovova metoda
V současné době zastaralá výrobní metoda, nepoužívá se vzhledem k vysoké ceně ethynu. Jako meziprodukt vzniká vinylalkohol, který rychle přesmykuje na acetaldehyd. (keto-enolová tautomerie):
CH≡CH + H2O → CH2=CH - OH → CH3 - CH=O jako katalyzátor se používají rtuťnaté soli v prostředí kyseliny sírové
Štěpení dvojných vazeb ozonem – ozonolýza
Metoda používaná v laboratorních podmínkách. Alken se oxiduje na nestálý ozonid, který přechází na aldehyd:
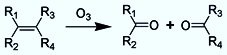
Aldehydy vznikají, pokud jsou R2 a R4 atomy vodíku a R1 a R3 jsou alkyly.
Příprava a výroba ketonů
Metody jako obdobné jako u aldehydů.
Oxidace nebo dehydrogenace sekundárních alkoholů
Oxidační činidla jsou stejná jako pro přípravu aldehydů. Nejběžnější je katalytická dehydrogenace sekundárních alkoholů, typickým katalyzátorem je oxid zinečnatý:
CH3CH(OH) CH3 → CH3COCH3 + H2 kat. ZnO, 350 oC
sekundární alkohol keton
Wacker – Hoechstův způsob – oxidace alkenů
Výroba probíhá obdobně jako u výroby acetaldehydu:
CH3CH = CH2 + PdCl2 + H2O → CH3COCH3 + Pd + 2HCl
Pd + 2CuCl2 → PdCl2 + CuCl
CuCl + 2HCl + 1/2 O2 → CuCl2 + H2O
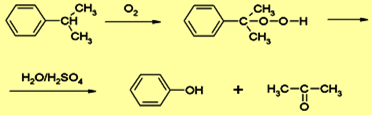
Kumenový způsob – výroba acetonu
Moderní výrobní postup, vznikají 2 průmyslově velmi významné látky - fenol aceton:
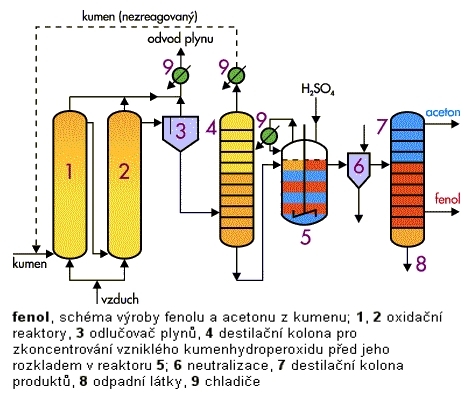
Obr. 1: Kumenová výroba
Štěpení dvojných vazeb alkenů ozonem (ozonolýza)
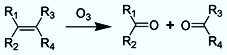
Ketony vznikají, pokud jsou R1,R2,R3 a R4 alkyly.
Hydratace alkynů za přítomnosti iontů Hg2+ v prostředí kys. sírové
Hydratací vzniká nestálá enol forma, která okamžitě přesmykem přechází na stálou ketoformu.
R - CH≡CH + H2O → R - CH(OH)=CH2 → R - CO - CH3 kat. rtuťnaté soli
alkyn nestálý enol keton
Vinylmethylketon vzniká katalytickou hydratací vinylacetylenu:
CH2=CH-C≡CH + H2O → CH2=CH-CO-CH3
vinylacetylen vinylmethylketon
Tepelný rozklad Ca2+nebo Ba2+solí karboxylových kyselin
Jedná se o nejstarší průmyslový způsob výroby, vznikají symetrické ketony.
(R-COO)2Ca → R-CO-R + CaCO3
Ca2+sůl karb. k. keton
Příprava a výroba chinonů
Oxidace arenů nebo fenolů
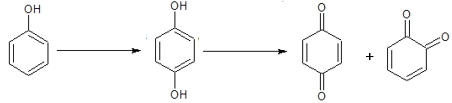 Oxidace fenolu
Oxidace fenolu
Slabou oxidací fenolu vznikají dvojsytné fenoly, silnou oxidací vznikají chinony, u dvojsytných fenolů probíhá oxidace snadno na o-chinon a p-chinon.
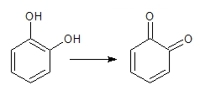 Oxidace dvojsytného fenolu
Oxidace dvojsytného fenolu
Výroba 9,10- antrachinonu (správněji anthra-9,10-chinon) je založena na (1) oxidaci anthracenu vzduchem za přítomnosti katalyzátrou (oxid vanadičný) nebo (2) alkylaci ftalanhydridu.
-
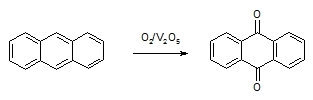
-
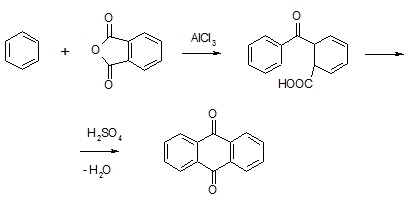 Výroba 9,10- anthrachinonu
Výroba 9,10- anthrachinonu