Rovnovážná konstanta reakce
Konstanta K se nazývá rovnovážná konstanta reakce. Její hodnota vyjadřuje, které ze zúčastněných reakčních složek (tj. zda produkty, nebo výchozí látky) za rovnováhy v reakční směsi převládají.
Podle konvence je rovnovážná konstanta vyjádřena zlomkem, v němž rovnovážné koncentrace produktů jsou v čitateli a rovnovážné koncentrace výchozích látek ve jmenovateli.
Faktory ovlivňující posun chemické rovnováhy
Chemickou rovnováhu lze narušit vnějšími vlivy. Systém vychýlíme z rovnováhy změnou:
-
tlaku a objemu,
-
teploty,
-
koncentrace.
Systém na vychýlení zareaguje a ustaví si novou rovnováhu. Tento Le Chatelierův princip popsali nezávisle na sobě německý fyzik Karl Ferdinand Braun a francouzský chemik Henri Louis Le Chatelier:
Tab. 1: Zákon akce a reakce
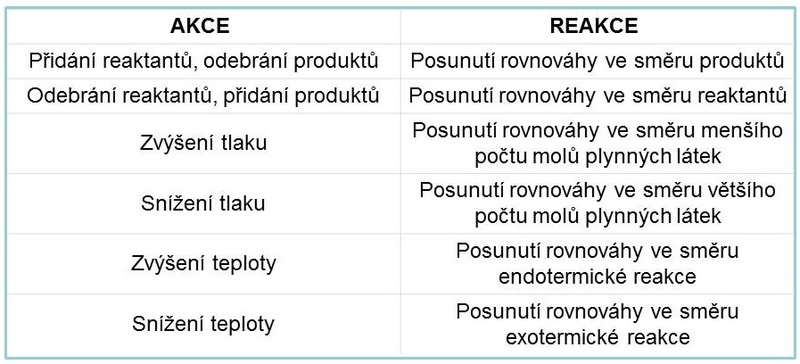
Změna tlaku ovlivňuje chemickou rovnováhu pouze u reakcí, ve kterých se mění počty plynných částic. Katalyzátory (ani inhibitory) neovlivňují chemickou rovnováhu.
Příklad:
Syntéza amoniaku - ovlivnění chemické rovnováhy ve směru na produkty
N2 (g) + 3 H2 (g) ⇄ 2 NH3 (g) ΔH ˂ 0
Řešení:
-
přidání reaktantů, odebrání produktů,
-
snížení teploty,
-
zvýšení tlaku.
- FLEMR, Vratislav a Bohuslav DUŠEK. Chemie I/Obecná a anorganická. 1. vydání. Praha: SPN, 2001, ISBN 80-7235-147-8.
- HONZA, Jaroslav a Aleš MAREČEK. Chemie pro čtyřletá gymnázia 1. díl. Brno: DaTaPrintBrno, 1996, ISBN 80-902200-4-5.
- ŠRÁMEK, Vratislav a Ludvík KOSINA. Obecná a anorganická chemie. 1. vydání. Olomouc: FIN, 1996, ISBN 80-7182-003-2.
Obrázky
-
Obr. 1: volné dílo.commons.wikimedia.org [online]. [cit.20.9.2014]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Ferdinand_Braun.jpg?uselang=cs
- Obr. 2: volné dílo.commons.wikimedia.org [online]. [cit.20.9.2014]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Lechatelier.jpg?uselang=cs
Pokud není uvedeno jinak, autorem obrázků je Mgr. Marie Jankovská.
Příklad:
Jak ovlivníte chemickou rovnováhu ve směru na produkty?
2 SO2 (g) + O2 (g) ⇄ 2 SO3 (g) ΔH ˂ 0
Řešení:
-
přidání reaktantů, odebrání produktů,
-
snížení teploty,
-
zvýšení tlaku.
Karl Ferdinand Braun
(6. června 1850, Fulda, Německo – 20. dubna 1918, New York, USA) byl slavný německý fyzik a nositel Nobelovy ceny.
Henry Louis Le Châtelier
(8. října 1850, Paříž – 17. září 1936, Miribel-les-Échelles) byl francouzský chemik. Proslul definováním tzv. Le Chatelierova principu, který popisuje, jak se změny podmínek, za kterých probíhá chemická reakce, projeví na chemické rovnováze.
Jak ovlivníte chemickou rovnováhu ve směru na produkty?
a) 2 NO (g) + O2 (g) ⇄ 2 NO2 (g) ΔH ˂ 0
b) CaCO3 (s) ⇄ CaO (s) + CO2 (g) ΔH > 0