Stereochemie cykloalkanů
Cykloalkany jsou méně flexibilní (ohebné) než jejich protějšky s přímým řetězcem, alkany. Zatímco v lineárních molekulách je možná rotace kolem jednoduchých vazeb uhlík – uhlík, rotace kolem jednoduchých vazeb v cykloalkanech je značně omezena. Například v ethanu dochází k volné rotaci kolem vazby C–C a tím se neustále mění prostorový vztah atomů vodíku na jednom atomu uhlíku vůči atomům vodíku na druhém atomu uhlíku.
Tab. 1: Konformace ethanu
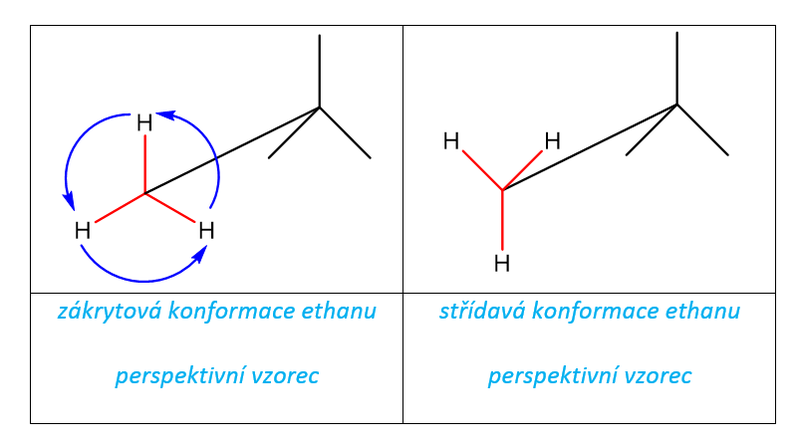
Na rozdíl od volné rotace kolem jednoduchých vazeb v lineárních alkanech mají cykloalkany volnosti mnohem méně.
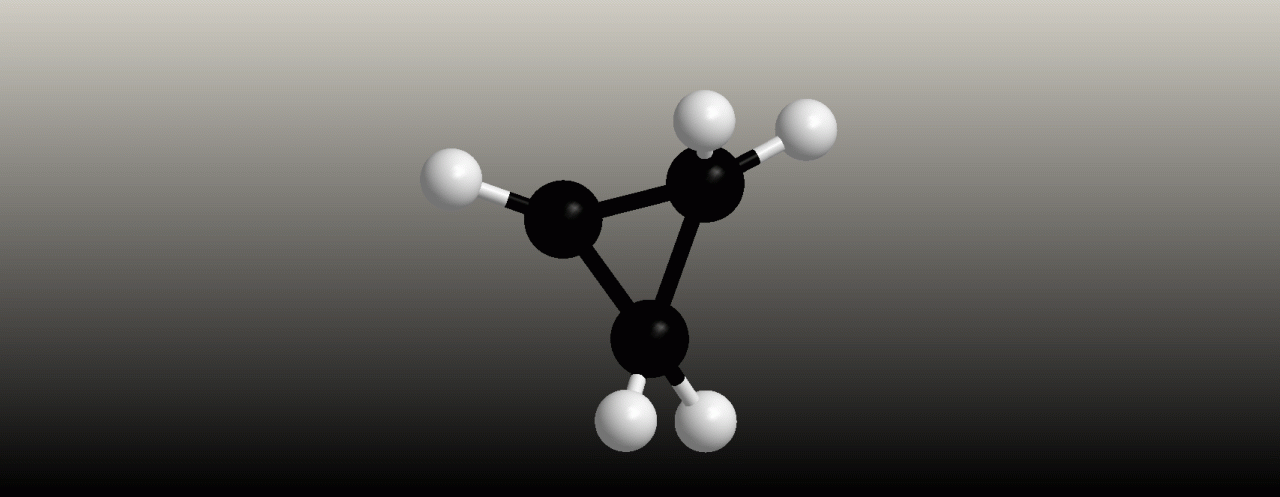
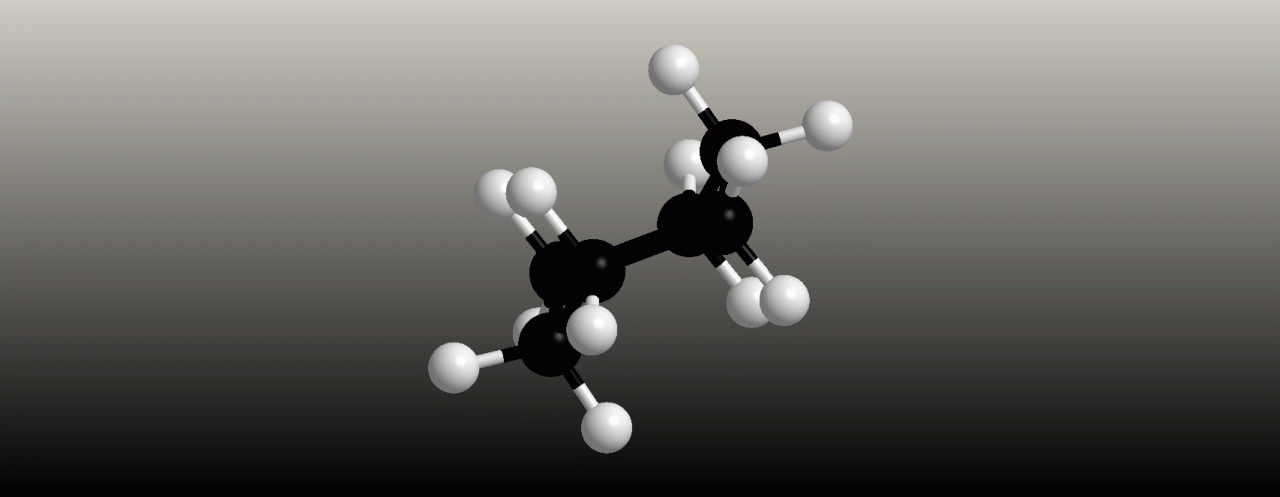
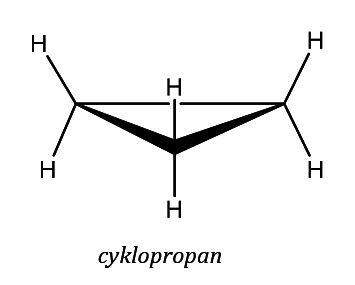
Cyklopropan
Kruh cyklopropanu je rovinný a napjatý. Toto napětí (také nazývané Baeyerovo pnutí) je příčinou zvýšené reaktivity cyklopropanu v porovnání s alkany. Rotace kolem vazeb uhlík – uhlík není bez otevření kruhu možná.
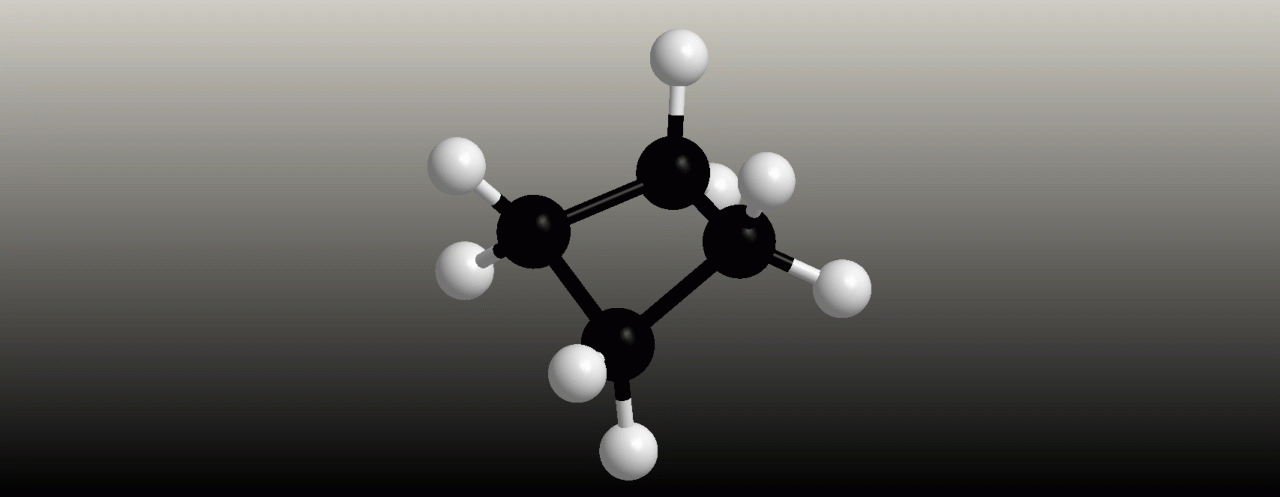
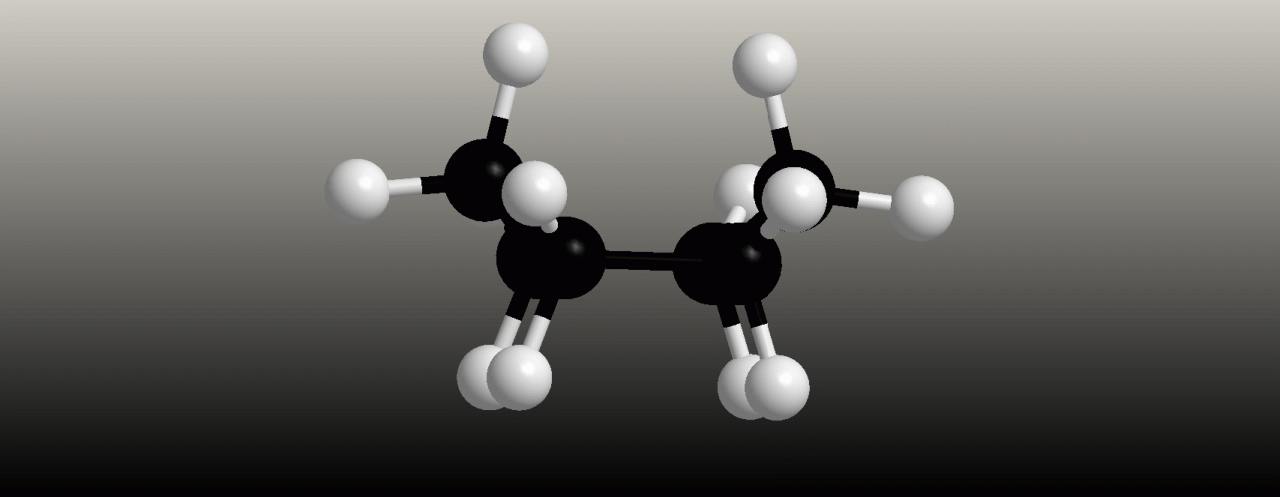
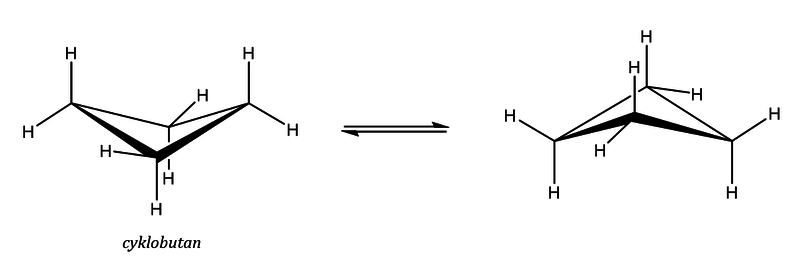
Cyklobutan
Cyklobutan již nemá zcela planární kruh, ale je poněkud přehnutý, jak je vidět z obrázku. Cyklobutan má také napjatý kruh, ale jeho reaktivita je podstatně nižší než u cyklopropanu. U struktury cyklobutanu existuje následující rychlá rovnováha, při níž se struktury rychle překlápí jedna v druhou.
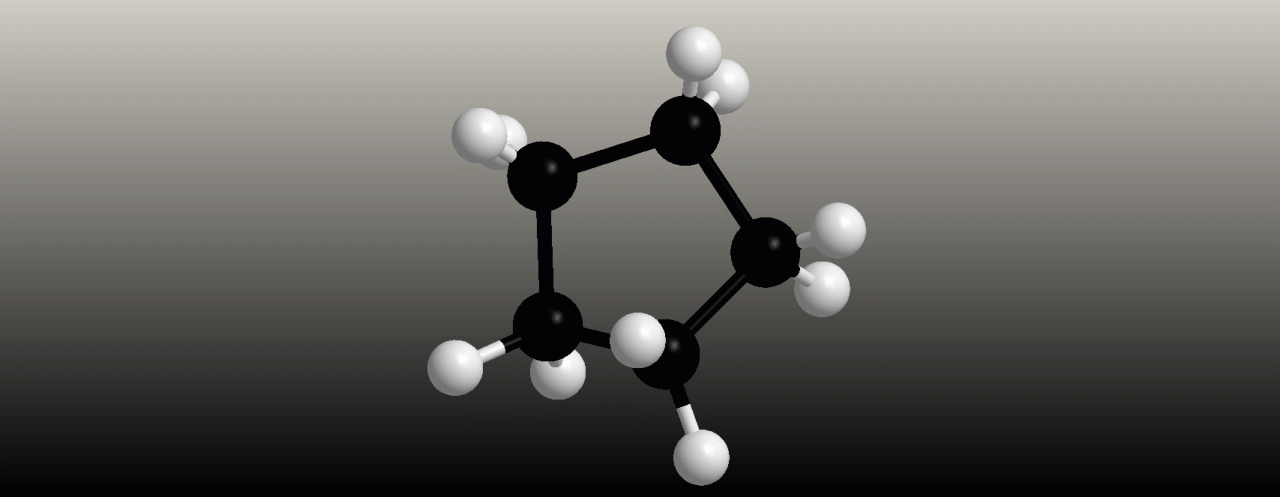
Cyklopentan
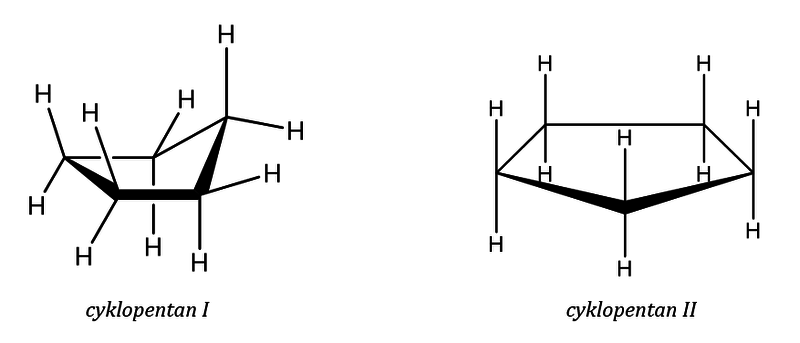
Cyklopentan zaujímá strukturu připomínající otevřenou dopisní obálku (I) a často se kreslí způsobem (II). Cyklopentan má ještě menší napětí kruhu než cyklobutan a jeho vnitřní úhel (108o) je blízký vazebnému úhlu atomu uhlíku v hybridním stavu sp3. Jeho reaktivita se podobá reaktivitě necyklických alkanů.
Cyklohexan
Cyklohexan patří mezi nejstálejší cykloalkany, protože zaujímá takové uspořádání, které nemá žádné napětí kruhu. Cyklohexanový kruh totiž není plochý, nýbrž jeho tvar je lomený.
Cyklohexanové kruhy mohou zaujímat více konformací: židličkovou, zkříženou a vaničkovou.
Tab. 2: Konformace cyklohexanu
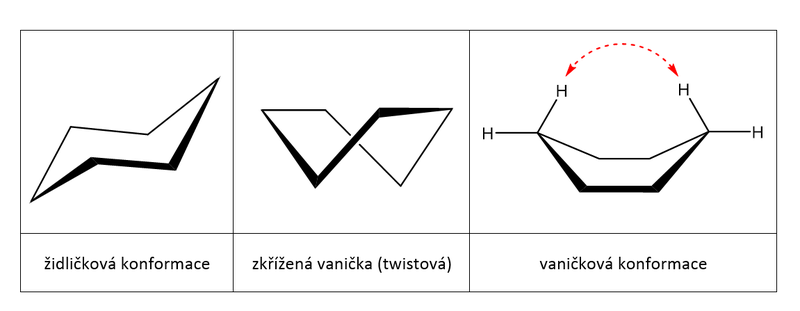
Název židličková konformace je odvozen od podobnosti se židličkou s opěradlem a podnožkou. Tato konformace je stabilnější, protože je energeticky nejchudší; a za normálních podmínek zaujímá víc než je 99% molekul cyklohexanu právě konformaci židličkovou.

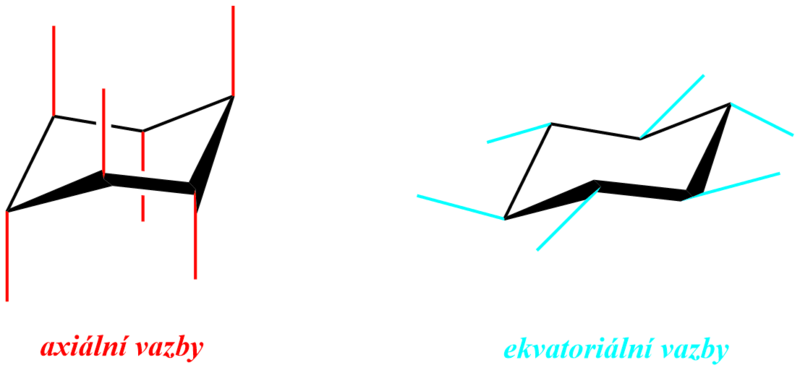
Židličková struktura má celkem dva typy vazeb: axiální a ekvatoriální. Axiální vazby míří nahoru a dolů, jsou kolmé k rovině kruhu, po jedné na každém uhlíku. Ekvatoriální vazby leží v rovině kruhu (po obvodu kruhu), také po jedné na každém uhlíku. Každý atom uhlíku má proto jeden axiální a jeden ekvatoriální atom vodíku.
Protože má židličková konformace cyklohexanu dva typy vazeb, může i židlička existovat ve dvou izomerních formách, které za normální teploty rychle přecházejí jedna v druhou:
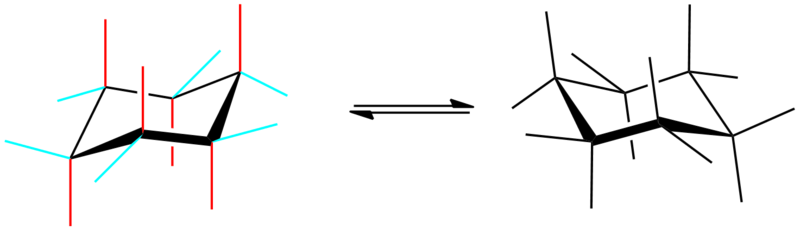
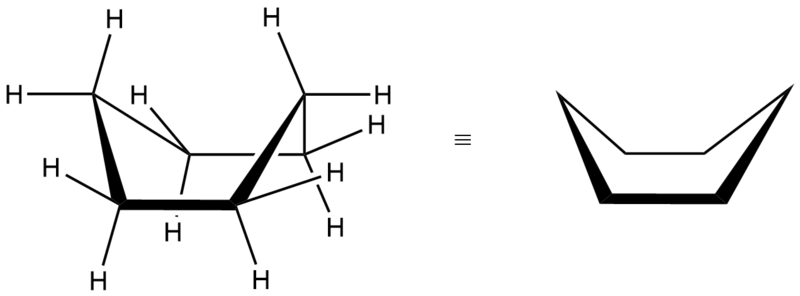
Kromě židličkové konformace cyklohexanu existuje ještě další jeho konformace, známá jako konformace vaničková. Tato konformace je mnohem méně stabilní než konformace židličková, neboť mezi atomy vodíku na prvním a čtvrtém uhlíku dochází ke stérickému pnutí.
Přechodová konformace, jíž musí molekula cyklohexanu projít při přeměně jedné židličkové konformace v druhou nebo v konformaci vaničkovou, se nazývá zkřížená konformace (angl. twisted).

Geometrická izomerie
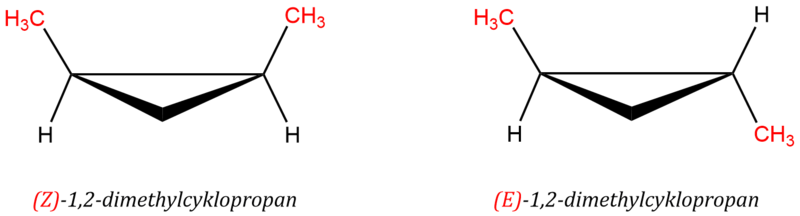
V důsledku cyklické struktury mají cykloalkany dvě strany, „horní“ a „dolní“, proto se u substituovaných cykloalkanů běžně setkáváme s geometrickými izomery, které označujeme jako izomery cis-trans. Označování cis a trans již v současnosti nevyhovuje a nahrazuje se tzv. E/Z konvencí.
Izomer Z má oba substituenty na stejné straně roviny kruhu, E izomer má substituenty na opačných stranách roviny kruhu. Příkladem může být 1,2-dimethylcyklopropan, kdy jeden izomer má oba methyly na stejné straně kruhu, zatímco druhý je má na stranách opačných. Oba izomery jsou stabilními sloučeninami a nemohou být jeden na druhý převedeny, aniž by se přitom neštěpily a opět nevznikaly chemické vazby.