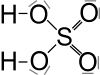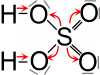
Redoxní děje
Oxidace a redukce – základní pojmy a vztahy
-
Při oxidačně redukčních (redoxních) reakcích dochází k přenosu elektronů a v důsledku toho se mění oxidační čísla některých atomů.
-
Atomy některých prvků při reakci elektrony odevzdávají (oxidují se), jiné elektrony přijímají (redukují se).
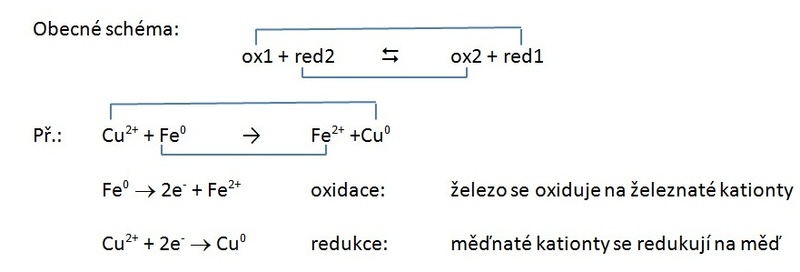
Každý redoxní děj lze tedy rozdělit na dvě poloreakce:
Oxidace – reaktant předá své elektrony, a proto se jeho oxidační číslo zvýší.
Redukce – reaktant přijme elektrony, a proto se jeho oxidační číslo sníží.
|
Ztrátou či přijetím elektronů se výrazně změní vlastnosti daných látek. |
 |
 |
 |
 |
| Obr. 1: Začátek experimentu | Obr. 2: Po několika sekundách | Obr. 3: Po několika hodinách | Obr. 4: Po několika dnech |
| Železný hřebík je vložen do roztoku CuSO4. |
V důsledku uvolňování iontů Fe2+ do roztoku
|
Vrstva Cu výrazně naroste. |
Podstatná část hřebíku je rozpustěna. Cu2+ jsou zcela zredukovány na Cu. Rezavá až hnědá barva je způsobena oxidací sloučeniny železnaté na železitou a také vyredukovanou mědí.
|
Oxidační činidlo
-
je taková látka, která má schopnost přijímat elektrony – je akceptorem elektronů,
jiné látky tak oxiduje (odebírá jim elektrony) a sama se redukuje.
Příklady oxidačních činidel:
-
všechny prvky s výrazně vyšší než průměrnou elektronegativitou:
především kyslík a halogeny (oxidační účinky se snižují s poklesem elektronegativity od fluoru k jodu), -
všechny vzájemné sloučeniny prvků s výrazně vyšší než průměrnou elektronegativitou:
kyslíkaté sloučeniny halogenů (např. NaClO, KClO3, KClO4), dusíku (zvláště v jeho nejvyšším oxidačním čísle V+: kyselina dusičná a její soli), peroxid vodíku, ale také koncentrovaná kyselina sírová, -
sloučeniny prvků s výrazně vyšší než průměrnou elektronegativitou s kovy ve vysokém oxidačním čísle:
např.: MnO4–, CrO42–, Cr2O72–, OsO52– a příslušné oxidy: Mn2O7, CrO3, OsO4, PbO2.
Například:
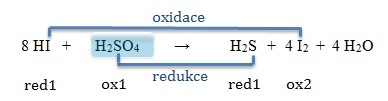
Redukční činidlo
-
látka, která může elektrony poskytovat – je donorem elektronů,
tzn. jiné látky redukuje a sama se oxiduje.
Příklady redukčních činidel:
-
všechny prvky s výrazně nižší než průměrnou elektronegativitou:
především alkalické kovy a kovy alkalických zemin, některé další neušlechtilé kovy (Mg, Zn), -
prvky s vysokou afinitou ke kyslíku, např.: H, C, P, Al,
-
sloučeniny prvků v nižších oxidačních číslech než těch, které tvoří ve svých stálých sloučeninách:
např. redukční účinky mají ionty:
Ti3+ – protože stabilním kationtem je Ti4+ ,
Cr2+ – protože stabilním kationtem je Cr3+ ,
Sn2+– protože stabilním kationtem je Sn4+,
Fe2+– protože stabilním kationtem je Fe3+ (v nekomplexních sloučeninách),
iontové hydridy (NaH, CaH2), CO, -
organické sloučeniny – uhlík má často nižší oxidační čísla než je jeho stabilní IV, typickými příklady jsou aldehydy nebo organokovové sloučeniny.
Mnohé látky mohou vystupovat někdy jako oxidační a jindy jako redukční činidla – reaktivita závisí na konkrétní dvojici oxidovaná – redukovaná látka,
např.: peroxid vodíku:
2 KI + H2O2 + H2SO4 → I2 + K2SO4 + 2 H2O
2 KMnO4 + 5 H2O2 + 3 H2SO4 → 5 O2 + 2 MnSO4 + K2SO4 + 8 H2O
Peroxid vodíku reaguje prudce také jen s pouhým roztokem manganistanu draselného bez účasti kyseliny. V tom případě vzniká vedle kyslíku hnědý oxid manganičitý a hydroxid draselný. Viz video.
Rovnici reakce lze zapsat iontově:
2 MnO4– + 3 H2O2 → 3 O2 + 2 MnO2 + 2 OH– + 2 H2O
Pozn.:
Pokud by reakce manganistanu draselného s peroxidem vodíku probíhala v kyselém prostředí (např. s kyselinou sírovou), vznikala by bezbarvá manganatá sůl, kyslík, síran draselný a voda.