Elektrolýza a její aplikace
|
Elektrolýza je označení pro děje vyvolané působením stejnosměrného elektrického proudu na elektrolyt. |
Elektrolyt je roztok nebo tavenina iontové sloučeniny, která prostřednictvím volných iontů vede elektrický proud.
Elektrolýza je důležitým procesem řady průmyslových výrob i laboratorních technik.
Elektrolýza probíhá při průchodu stejnosměrného elektrického proudu roztokem nebo taveninou elektrolytu. Pohyb elektronů elektrolytem je realizován elektrodami. Elektrony jsou do soustavy přiváděny katodou, ke které jsou v důsledku jejího záporného náboje přitahovány kationty.
Na katodě tedy dochází k redukci.
Opačný děj, odebírání elektronů aniontům, a tedy jejich oxidace, probíhá na elektrodě, která se nazývá anoda.
Jako anodu označujeme elektrodu, na které dochází k oxidačním dějům.
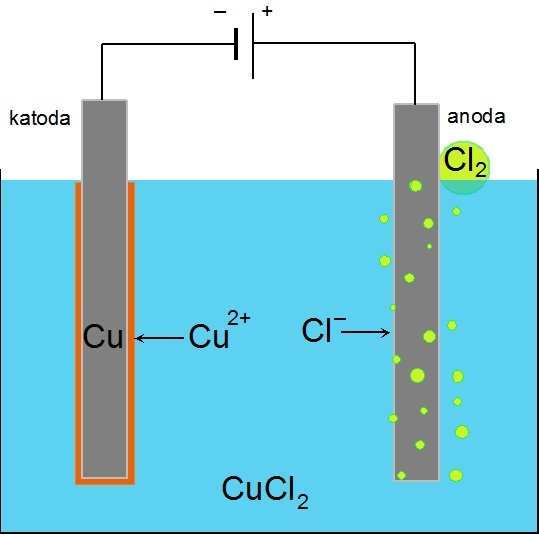 |
| Obr. 1: Schéma elektrolýzy roztoku CuCl2 |
Elektrolýza roztoku chloridu měďnatého
Pokud do roztoku chloridu měďnatého vložíme dvě uhlíkové elektrody a připojíme je ke zdroji stejnosměrného proudu, dochází na záporně nabité elektrodě k redukci měďnatých iontů na kovovou měď a na kladně nabité elektrodě se oxidují chloridové anionty na plynný chlor.
Děj na anodě – anodická oxidace: 2 Cl– → Cl2 + 2e–
Děj na katodě – katodická redukce: Cu2+ + 2e– → Cu0
Měď má kladný elektrodový potenciál, je to ušlechtilý kov, proto se jeho ionty snadno redukují na kovovou měď.
Jiná situace nastane, pokud budeme provádět elektrolýzu vodného roztoku chloridu sodného.
Elektrolýza vodného roztoku chloridu sodného (solanky)
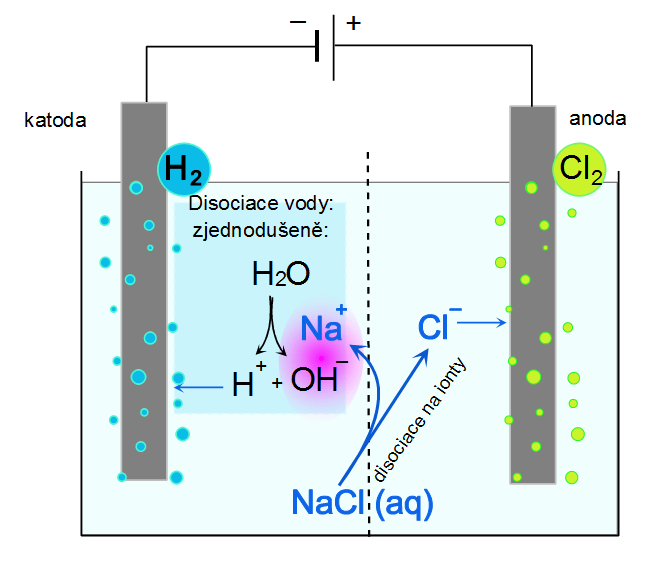 |
| Obr. 2: Schéma elektrolýzy solanky |
- Sodík je kov s výrazně záporným elektrodovým potenciálem, a redukuje se tedy neochotně.
- Ve vodném roztoku NaCl se nacházejí kationty Na+, ale také H3O+, vznikající autoprotolýzou vody H2O + H2O ⇄ H3O+ + OH–.
- Zjednodušme si pro následující výklad oxoniový kation H3O+ na pouhý proton H+.
- Z umístění prvků v řadě napětí kovů plyne, že vodíkové kationty se budou na katodě redukovat přednostně.
- Elektrolýzou nasyceného roztoku NaCl (solanky) tedy vzniká
- na katodě vodík: 2H+ + 2e– → H2,
- na anodě chlor: 2 Cl– – 2e– → Cl2
- a v roztoku zůstává hydroxid sodný Na+ + OH–.
- Obě elektrody musejí být od sebe odděleny polopropustnou (semipermeabilní) membránou, která zabrání reakci chloru s hydroxidem sodným vznikajícím v katodovém prostoru. Chlor s hydroxidem sodným reaguje za laboratorní teploty za vzniku chlornanu a chloridu sodného, při zvýšené teplotě by vznikaly chlorečnan a chlorid sodný.
Pozor! Elektrolýza roztoku NaCl je něco jiného než elekrolýza taveniny NaCl!
Elektrolýza taveniny chloridu sodného
- Soustava je tvořena pouze kationty sodnými Na+ a anionty chloridovými Cl–.
- V tomto případě se na katodě redukuje kovový sodík: Na+ + e– → Na0
- Na anodě vzniká oxidací chloridových aniontů plynný chlór: Cl– → Cl0 + e– ,
atomární chlór se slučuje do molekul: Cl + Cl → Cl2
Elektrolýza je nezastupitelnou metodou průmyslové výroby některých kovů, např. hliníku, hořčíku, sodíku, draslíku, ale i nekovu, jako je fluor.
Využití elektrolýzy
1. Výroba chemických prvků
Elektrolýzou lze vyrábět kovy (Na, K, Ca, Mg, Al) i nekovy (kyslík, vodík, chlor, fluor).
2. Výroba sloučenin
Elektrolyticky se vyrábějí alkalické hydroxidy (NaOH, KOH).
3. Elektrolytická rafinace (čištění) kovů
|
|
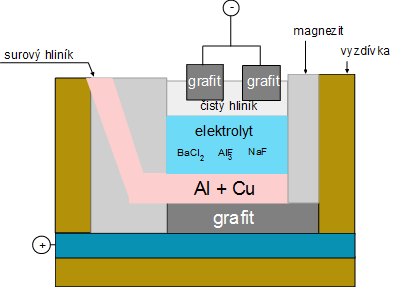
| Obr. 3: Schéma elektrolytické rafinace hliníku |
Tato metoda se používá především při čištění mědi nebo hliníku.
Rafinace hliníku
Rafinace hliníku se provádí trojvrstvovou metodou.
Princip je zřejmý z obrázku.
Spodní vrstvu v elektrolyzéru tvoří tavenina hliníku s mědí (25 % Cu). Její hustota je 3 000 až 3 500 kg·m-3.
Prostřední vrstvou je elektrolyt – tavenina směsi BaCl2, AlF3 a NaF – jeho hustota je 2 700 kg·m-3.
Nejvýše položenou vrstvu tvoří čistý hliník o hustotě 2 300 kg·m–3, který se vyredukovává na grafitových katodách.
Čistota takto vyrobeného hliníku je 99,998 %.
Elektrolytická rafinace mědi
Základem elektrolytické rafinace je rozpouštění měděné anody ponořené v roztoku síranu měďnatého stejnosměrným proudem a vyredukování mědi na katodě. Anodou je litá deska ze surové mědi o tloušťce 25–40 mm a váze 200–300 kg. Katoda je z elektrolyticky vyrobeného měděného plechu, tlustého 0,5–0,6 mm.
Jako elektrolytu se používá okyseleného vodného roztoku síranu měďnatého.
Působením stejnosměrného proudu prochází měď z anody do roztoku a opět se vyloučí na katodě.
| Rozpouštění mědi na anodě: | Cu - 2e- → Cu2+ |
| Vylučování mědi na katodě: | Cu2+ + 2e- → Cu |
Elektrolyticky se čistí měď, která obsahuje drahé kovy (zlato, stříbro), popřípadě selen nebo tellur. Nelze je totiž odstranit žárovou rafinací, tj. vháněním vzduchu do taveniny technické mědi. Tyto kovy jsou pak obsaženy v tzv. anodových kalech.
Na podobném principu, na němž je založena rafinace mědi, se provádí galvanické pokovování.
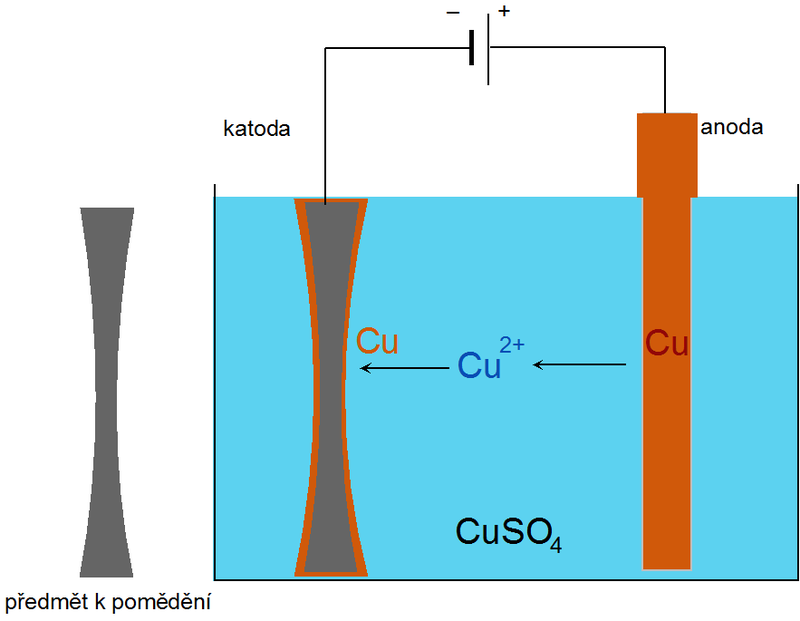 |
| Obr. 4: Schéma galvanického pokovování |
4. Galvanické pokovování
Při galvanickém pokovování jde o vytvoření vrstvy kovu na daném předmětu. Jedná se například o pochromování, poniklování, pomědění, pozinkování. Předmět je vložen do roztoku iontů kovu a zapojen jako záporná elektroda. Jako kladná elektroda slouží kov, jehož povlak má být na daném předmětu vytvořen. Pomocí stejnosměrného proudu se na záporné elektrodě (katodě) redukují ionty kovu z roztoku a jejich úbytek je doplňován rozpouštěním kovové anody. Galvanické pokovování se užívá pro vytvoření vrstvy odolné vůči korozi (nikl, zinek), dekorativní lesklé a tvrdé vrstvy (chrom). Vrstva mědi se používá jako mezivrstva při poniklování či pochromování, která zvyšuje přilnavost a odolnost proti korozi.
5. Polarografie
Polarografie je elektrochemická analytická metoda. V roce 1922 ji objevil český vědec Jaroslav Heyrovský a v roce 1959 za ni obdržel Nobelovu cenu. Tato metoda umožňuje důkazy i stanovení oxidovatelných či redukovatelných látek v roztoku.
Podstata polarografie
Polarografie je analytická metoda, při které sledujeme závislost proudu na napětí vkládaném na článek, který je sestaven z jedné polarizovatelné a jedné nepolarizovatelné elektrody ponořené do analyzovaného roztoku.
Jako polarizovatelná elektroda slouží rtuťová kapková elektroda – rtuť vykapávající ze skleněné kapiláry.
Kapková elektroda má výhodné vlastnosti:
| – | malý povrch | |||
⇒ |
proto náboj na ni přivedený jí udělí velký potenciál | |||
⇒ |
při elektrodových reakcích se přemění velmi malé množství látky, a tak se koncentrace analyzované látky prakticky nezmění |
|||
| – | povrch elektrody se neustále obnovuje, takže není změněn předchozí elektrodovou reakcí | |||
| – | na rtuti je velké přepětí vodíku, což umožňuje provádět analýzu i v kyselých roztocích, aniž by se vylučoval vodík | |||
Jako nepolarizovatelná elektroda se používá rtuťové dno – velkoplošná rtuťová elektroda (rtuť na dně nádobky). Tato elektroda je nepolarizovatelná díky svému velkému povrchu.
 |
|
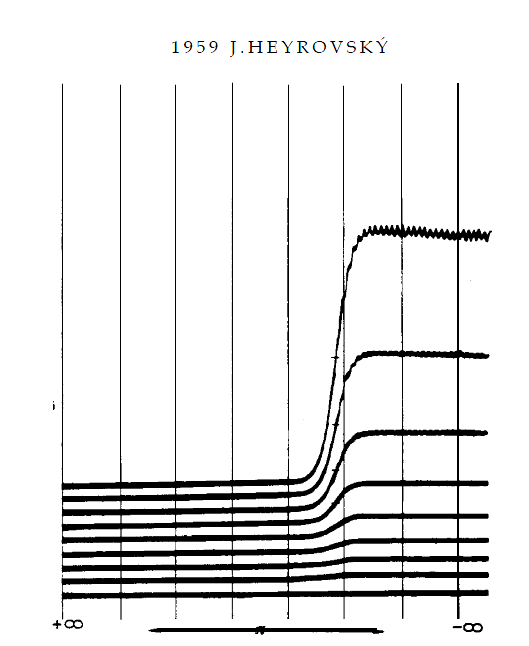
Obr. 6: Polarografické křivky |
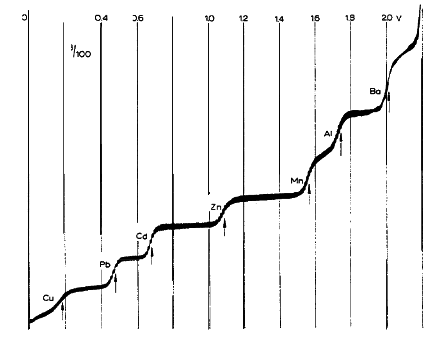 |
| Obr. 5: Polarogram |
Na článek takto vytvořený se vkládá napětí z vnějšího zdroje zpravidla tak, že rtuťová kapková elektroda je katodou. Na povrchu kapky rtuti se vytvoří elektrická dvojvrstva. Při zvyšování potenciálu mezi anodou a katodou dochází k vylučování příslušných iontů na katodě a tím k nárůstu proudu. Proud je limitován množstvím iontů, které mohou ke katodě z roztoku přicházet. Jakmile se množství vylučujících se iontů rovná počtu přicházejících iontů z roztoku, proud se přestane zvětšovat.
 |
| Obr. 7: Polarograf |
Na grafu závislosti proudu na napětí se reakce projeví vytvořením tzv. polarografické vlny. Poloha vlny na vodorovné ose (napětí) je charakteristická pro určitou látku (obr. 5), z výšky vlny lze určit koncentraci příslušné látky(obr. 6).
Polarografie se využívá pro stanovení a detekci anorganických i organických látek o velmi nízkých koncentracích, řádově 10-7 mol.l-1 až 10-12 mol.l-1 . Své uplatnění nachází ve všech odvětvích průmyslu, v nichž se používají chemické analýzy, dále také v biologii, farmacii a lékařství (např. diagnóza rakoviny).
Pozn.: Kliknutím na obrázek jej získáte ve větší velikosti.
6. Galvanoplastika
Galvanoplastika je technologie založená na principu elektrolýzy. Technika práce je totožná s technikou galvanického pokovování, poniklování, pochromování, pomědění či pozinkování. Charakteristický znak galvanoplastiky však spočívá v tom, že jsou vytvářeny silné vrstvy v řádech několika mm. Vytváří se tak skořepiny neboli galvana, které slouží jako formy.
Galvanoplastika má velice širokou škálu využití. Je to metoda, kterou je možné vytvářet tvarově složité součásti. V některých případech je jedinou možnou technologií výroby z hlediska složitosti výrobku. Je také často mnohem finančně výhodnější při výrobě rozměrnějších forem, než kdyby se forma musela obrábět. Proč tomu tak je? Při obrábění vzniká velké množství odpadu cenného kovu. Při galvanoplastice žádný kovový odpad nevzniká. Galvanoplastika je vhodná pro zhotovení různých kopií, jako jsou např. mince, medaile, šperky, nábytkové kování, trojrozměrné plastiky, sochy apod. V současné době je galvanoplastika významnou průmyslovou metodou používanou pro zhotovování forem pro zpracování plastů, lisování hudebních nosičů či štočků používaných v tiskařském průmyslu. Nejvíce používanými kovy v galvanoplastice jsou měď a především nikl. Nikl má velmi dobré mechanické vlastnosti a niklové formy dobře odolávají opakovanému tepelnému namáhání.
Galvanoplastika nachází využití v mnoha oborech:
- strojírenství (nástroje a formy, měřidla, chladiče, výměníky, renovace strojních součástí, elektrody, brusné nástroje s kovovou matricí)
- elektrotechnika (mikrovlnné součástky - vlnovody, speciální vodivé struktury, chladiče, součásti elektronek, houbovité elektrody pro elektrochemické zdroje)
- fyzika (zrcadla, odražeče záření, stínicí prvky)
- hudební průmysl (nástroje pro lisování CD a vinylových gramodesek)
- gumárenství (formy pro lisování podrážek či imitací přírodních materiálů)
- doprava (paraboly světlometů, formy pro lisování palubních desek či kuliček řadicích pák, spalovací komory raketových motorů)
- sklářský průmysl (formy, brusné nástroje s kovovou matricí).
Výroba vinylové desky
Na první pohled by se mohlo zdát, že tato výrobní technologie patří do hudebního pravěku. V období nástupu hudebních CD skutečně došlo v mnoha firmách k likvidaci výroby vinylových gramofonových desek. Brzy však dýdžejové i hudební sběratelé zjistili, že vinylové desky jsou pro ně cennější než CD. Tak se stalo, že se firma v Loděnici u Berouna, která si výrobní technologii ponechala, stala současnou světovou jedničkou ve výrobě vinylových desek. Denně jich vyrobí 25 000 a jsou jejím nejziskovějším výrobkem. Ve firmě pracuje asi 2000 lidí a tržby v roce 2014 dosáhly dvou miliard korun.
Výrobní technologie se v určité fázi shoduje s výrobou CD či DVD. Jde o výrobu niklové matrice, která obsahuje "negativní" záznam zvuku, galvanoplastickou metodou. Z této matrice se lisováním získávají zvuková média.
- Zvuk je transformován na elektrický signál, který je veden přes soustavu zesilovačů.
-

Obr. 8: Galvanoplasticky vyrobená matrice pro lisování LP desek Signál je veden na hrot diamantového nože, kterým se řežou drážky do ocelové nebo měděné desky. Pokud se vyrábí monozáznam, drážka jde jen zleva doprava. Stereozáznam je naopak prostorový a drážka pak směřuje zleva doprava i nahoru a dolů.
- Ocelovou desku je možné přehrát jako běžnou vinylovou desku. Ovšem lisované kopie by byly zrcadlově obrácené, a tedy nepoužitelné. Proto podložka nejdříve zamíří do galvanické lázně, kde se galvanoplastikou získá matrice pro lisování.
- Po nastříkání roztoku dusičnanu stříbrného se na lakovém povrchu s drážkami vyloučí nepatrná elektricky vodivá vrstvička stříbra. Postříbřená laková fólie se zavěsí jako katoda do niklovací lázně, kterou tvoří roztok niklových solí a dalších přísad.
- Pokud je deska z mědi, proces stříbření odpadá a deska putuje přímo do lázně. Stejnosměrný elektrický proud, procházející od niklové anody ke katodě, způsobí, že se na katodě postupně vyloučí potřebná vrstva kovového niklu.
- Oddělením narostlé niklové vrstvy získáme zrcadlový obraz – negativ záznamu – surovou matrici.
- Matrice následně míří do lisovny. Do hydraulického lisu se mezi dvě předehřáté formy s matricemi vloží etiketa jedné strany desky, lisovací hmota a etiketa druhé strany desky. Tlak větší než 100 tun a teplota 160 °C dokonale okopíruje povrch matrice s drážkami. Lisování jedné gramodesky trvá přibližně 25 sekund.
- Po ochlazení formy a otevření lisu se deska vyjme, ořízne, zkontroluje, zabalí a zamíří k zákazníkovi.
Výroba CD a DVD
- Zvukový záznam je převeden na elektrické signály, které ovládají laserový paprsek. Laser vypaluje záznam do speciální citlivé vrstvy na skleněném kotouči.
- Místa zasažená laserem se stanou citlivá na leptání kyselinou. Tato místa jsou pak odleptána spolu se skleněnou vrstvou.
- Takto v materiálu vzniknou prohlubně.
- Skleněný disk se pak galvanoplasticky ponikluje a vznikne niklová matrice.
- Záznam z matrice je přenesen lisováním do kotoučů z polykarbonátu a opatřen světloodrazivou vrstvou z hliníku.
- Nakonec je disk potažen ochrannou vrstvou čirého laku a příslušným potiskem.
- Spirálová stopa na CD o průměru 12 cm je dlouhá 5 km a obsahuje asi 3 miliardy prohlubní. Pouze každé rozhraní mezi prohlubní a rovnou plochou je čtecím laserem interpretováno jako logická jednička, jinak zařízení registruje nulu.
- DVD je vyráběno s využitím laseru o kratší vlnové délce a umožňuje vyšší hustotu záznamu.