Acidobazické indikátory
V laboratoři se často používají pro určení kyselin a zásad látky, které při různých hodnotách pH mění svoje zbarvení = acidobazické indikátory.
V praxi se používají při acidobazické titraci. Využívá se té vlastnosti, že jejich disociovaná a nedisociovaná forma mají rozdílné zbarvení. Při titraci různých látek se používají různé indikátory. Například methyloranž a methylčerveň jsou vhodné pro titraci slabých zásad, fenolftalein pro titraci slabých kyselin.
Příklady:
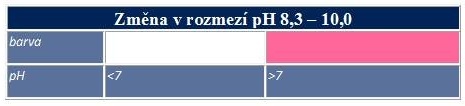
- fenolftalein
Tab. 1: Změna zbarvení fenolftaleinu
- bromthymolová modř
Tab. 2: Změna zbarvení bromthymolové modři

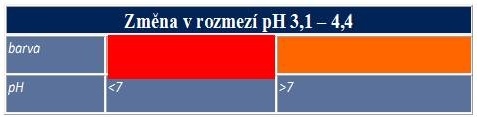
- methylová oranž
Tab. 3: Změna zbarvení methylové oranži
Jednoduchý indikátor se dá připravit extrakcí barviv z květů rostlin nebo listů červeného zelí. Ty obsahují barviva = antokyany.
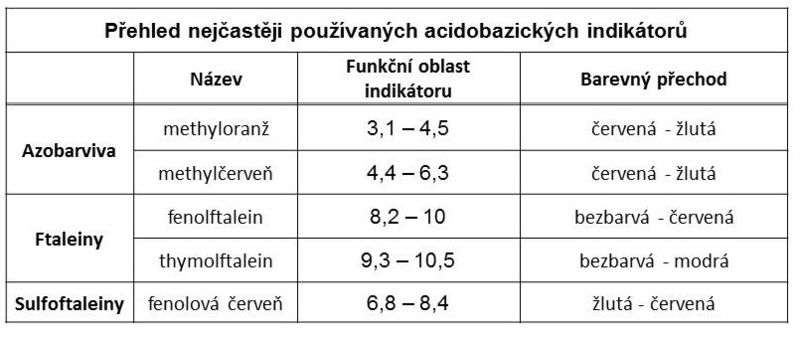
Tab. 4: Přehled nejčastěji používaných acidobazických indikátorů
Obrázky
- Obr. 3: Petrb.creativecommons. [online]. [cit.5.12.2014]. Dostupný na WWW:
http://www.wikiskripta.eu/index.php/Soubor:Ekvivalence.PNG
- Obr. 4: Icewalker.creativecommons. [online]. [cit.5.12.2014]. Dostupný na WWW:
http://www.wikiskripta.eu/index.php/Soubor:Titra%C4%8Dn%C3%AD_k%C5%99ivky.png
Pokud není uvedeno jinak, autorem obrázků je Mgr. Marie Jankovská.
Antokyany jsou ve vodě rozpustné pigmenty, obsažené ve vakuolách některých rostlinných buněk.
Jejich barva se mění v závislosti na pH. Kyselé roztoky antokyanů bývají červené, neutrální fialové a zásadité modré, zelené až žluté.

Obr. 1: Změna zbarvení výluhu z listů červeného zelí

Obr. 2: Změna zbarvení květů pelargonie po namočení do roztoku amoniaku
Kyseliny_a_zasady_ kolem_nas - viz. přílohy
Funkční oblast indikátoru
= barevný přechod, tj. oblast, v níž nastává pozorovatelná změna. Při titraci volíme indikátor tak, aby jeho funkční oblast odpovídala pH okolí bodu ekvivalence na titrační křivce.
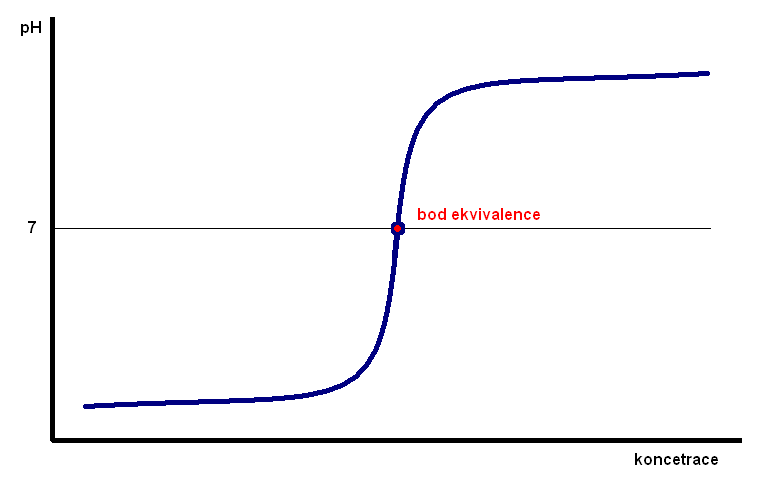
Bod ekvivalence
= konec titrace – stav, kdy látkové množství titračního činidla (jeho látková koncentrace vynásobená spotřebovaným objemem při titraci) je ekvivalentní látkovému množství stanovované látky.
Obr. 3: Křivka bodu ekvivalence
Titrační křivka
= grafické znázornění závislosti změn pH na množství přidávaného titračního činidla.
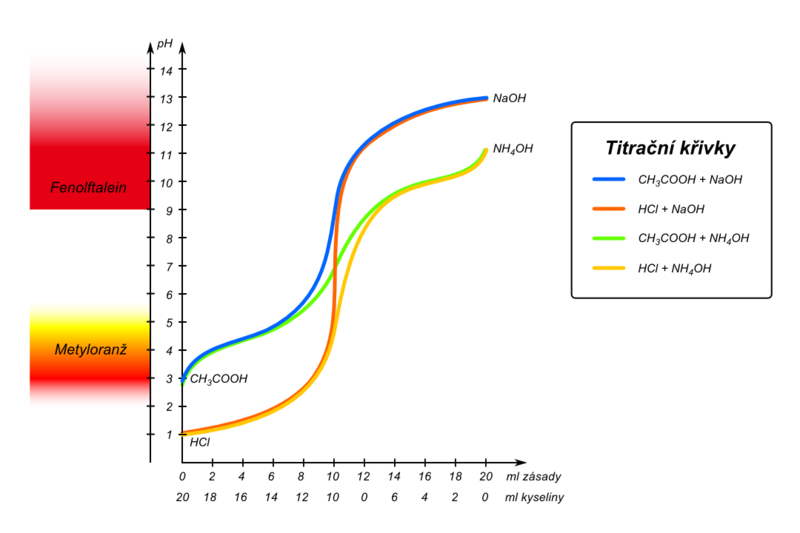
Obr. 4: Titrační křivky