Chemická termodynamika
Termodynamika se zabývá studiem fyzikálních a chemických dějů spojených s energetickými změnami.
Soustava = část prostoru s jeho hmotnou náplní
Typy soustav:
-
otevřená - vyměňuje s okolím energii i hmotu,
-
uzavřená – vyměňuje s okolím pouze energii,
-
izolovaná – nevyměňuje s okolím energii ani hmotu, jedná se o idealizaci, k níž se mohou reálné soustavy pouze blížit.
Stavové veličiny:
-
používáme je k popisu stavu, ve kterém se soustava nachází,
-
jsou závislé jen na počátečním a konečném stavu soustavy, nikoliv na cestě, kterou soustava prošla,
-
dělíme je na:
-
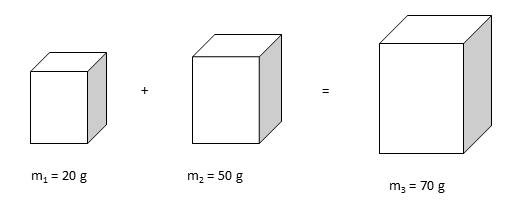
extenzivní – závisí na velikosti soustavy (hmotnost, objem, látkové množství),
-
Obr. 1: Příklad extenzivní veličiny - hmotnost
-
intenzivní – nezávisí na velikosti soustavy (teplota, tlak, hustota).
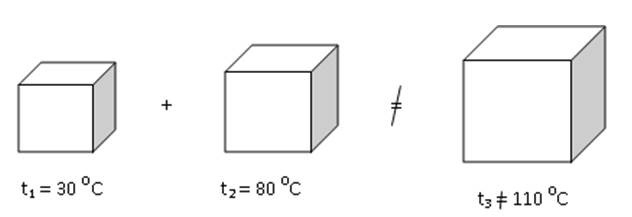
Obr. 2: Příklad intenzivní veličiny - teplota
Pro snahu o udržení alespoň jedné intenzivní veličiny konstantní se většina reakcí provádí za konstantního tlaku = izobarické děje.
Obrázky
-
Obr. 3: Autor neznámý [online]. [cit.20.9.2014]. Dostupný na www: http://www.cesky.porcelan.cz/cs/produkty-sortiment/cibulak-sortiment-dle-kategorii/hrnky-s-vickem/hrnek-cesky-s-1-uchem-s-vikem-s-vyr-80151-00001/251
- Obr. 4: Autor neznámý [online]. [cit.20.9.2014]. Dostupný na www: http://www.e-nadobi.cz/Fotografie/Zbozi/Original/318005.jpg
Pokud není uvedeno jinak, autorem obrázků je Mgr. Marie Jankovská
Popřemýšlejte o příkladech otevřených, uzavřených a izolovaných soustav a poté k jednotlivým obrázkům přiřaďte typ soustavy.
1. Hrníček s víčkem

Obr. 3: Hrníček s víčkem
2. Termoska s čajem

Obr. 4: Termoska s čajem
3. Živý organismus
Obr. 5: Živý organismus
