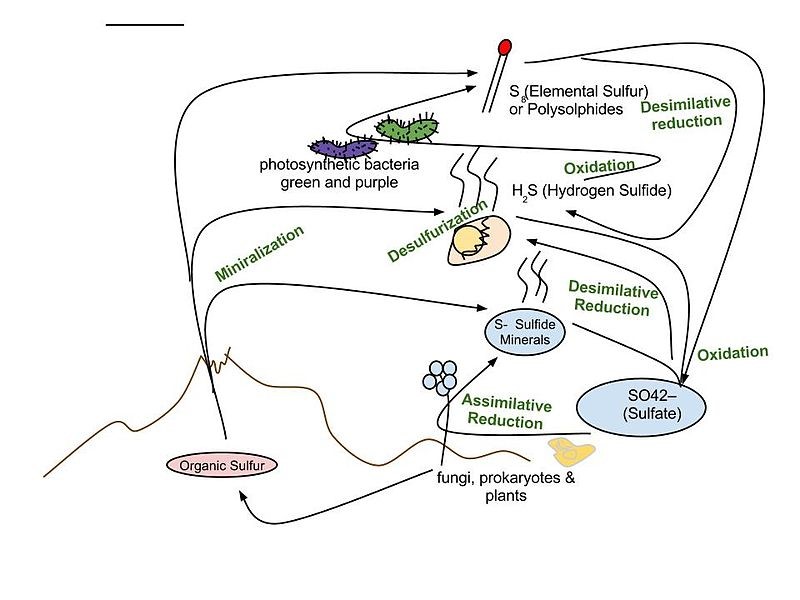
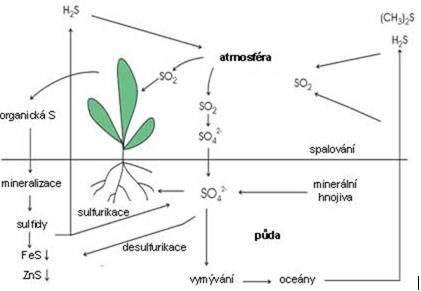
Sirné sloučeniny
Patří mezi ně organické sloučeniny, které v molekule obsahují jeden nebo více atomů síry. Obsažená síra může být dvouvazná, čtyřvazná a šestivazná; může být i součástí cyklu.
Mezi významné sirné sloučeniny patří thioly (thioalkoholy a thiofenoly) a sulfidy (thioethery), které se odvozují od sulfanu náhradou jednoho, případně obou atomů vodíků.
Za nejvýznamnější deriváty je možné považovat sulfonové kyseliny, které se odvozují od kyseliny sulfonové, která je tautomerem kyseliny siřičité.
Řada sloučenin, obsahujících síru, patří mezi přírodní látky; často zodpovídají za charakteristickou chuť a zápach (látky obsažené v česneku, cibuli, sekretu skunka, fytoalexiny v rostlinách čeledi brukvovitých). Také dvě kódové aminokyseliny (cystein, methionin – esenciální AMK) obsahují v molekule síru.