Halogenidy 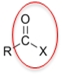
Jsou odvozeny náhradou skupiny – OH v karboxylové skupině halogeny.
Názvosloví
Systematický název
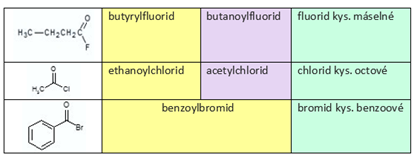
Název acylu (systematický nebo latinský) + (di, tri, …) + název halogenu + „-id“.
Opisný název
Halogenid + 2.pád příslušné kyseliny, např. chlorid kyseliny octové.
Příklady:
Vlastnosti
Obvykle těkavé až olejovité kapaliny, silně dráždivého nepříjemného zápachu. Vyšší jsou látky tuhé, nižší na vzduchu dýmají. Hustota roste s hmotností halogenu. Jsou rozpustné v benzenu, sirouhlíku, ale ve vodě a ethanolu se rozkládají. Jedná se o velice reaktivní látky, reaktivnější než karbonylové sloučeniny, protože halogen snižuje elektronovou hustotu na karbonylovém uhlíku. Reaktivita se snižuje od acylfluoridů k acyljodidům. V organické syntéze se užívají jako acylační činidla. Většina reakcí, do kterých vstupuje acylchlorid, probíhá mechanismem nukleofilní substituce.
Významné reakce
Hydrolýza: S vodou se rozkládají a poskytují příslušnou kyselinu a halogenvodík:
CH3CH2COCl + H2O → CH3CH2COOH + HCl
Alkoholýza: Reakcí s alkoholem vznikají estery:
CH3COCl + CH3CH2OH → HCl + CH3COOCH2CH3
Amonolýza: Reakcí s amoniakem vznikají amidy:
C6H5COCl + NH3 → HCl + C6H5CONH2 (NH3 +HCl → NH4Cl)
Reakcí se solemi karboxylových kyselin vznikají anhydridy:
CH3COCl + CH3COONa → (CH3CO)2O + NaCl
Reakce s Grignardovým činidlem: Nejdříve vznikají ketony, ty dále reagují s přebytečným alkylmagnesiumhalogenidem na terciární alkoholy:
CH3COCl + RMgBr → CH3COR + MgBrCl
Redukce: Probíhá působením silně redukčních činidel, např. lithiumaluminiumhydridem, může dojít k redukci až na alkohol, jako meziprodukty jsou ethanoláty lithný a hlinitý (používá se např. pro přípravu alkoholů z vyšších mastných kyselin):
4 CH3COOH + LiAlH4 + 4 H2O → 4 CH3CH2OH + LiOH + Al(OH)3
Příprava
Acylhalogenidy lze připravit z karboxylových kyselin nebo jejich solí zahříváním s chloridem fosforitým, fosforečným nebo thionylchloridem (dichlorid kyseliny siřičité). Z hlediska izolace je nejvhodnější látkou thionylchlorid, protože v průběhu reakce vzniká oxid siřičitý a chlorovodík, které jsou v plynném stavu a ze směsi se dobře oddělují:
RCOOH + SOCl2 → RCOCl + HCl + SO2
Obdobně:
3 RCOOH + PCl3 → 3 RCOCl + H3PO3
RCOOH + PCl5 → RCOCl + HCl + POCl3
Průmyslově vhodné jsou pak postupy reakcí sodných solí organických kyselin s trichloridem kyseliny fosforečné nebo dichloridem kyseliny sírové, protože poskytují dobře oddělitelné nejedovaté produkty. Metody jsou použitelné i v případě vícesytných kyselin.
Použití
Acetylchlorid CH3COCl slouží jako acylační činidlo, používá se např. k výrobě léčiv, barviv.
Benzoylchlorid C6H5COCl má využití při výrobě barviv, parfémů, organických peroxidů, léčiv a pryskyřic. V alkalickém prostředí reaguje s peroxidem vodíku a vzniká dibenzoylperoxid, který se používá jako katalyzátor polymeračních reakcí, bělící prostředek, k léčbě akné, jako dezifekční prostředek, antiseptikum při popálenínách a k přípravě perbenzoové kyseliny.
Výroba dibenzoylperoxidu:
2 C6H5COCl + Na2O2 → ( C6H5CO)2O2 + 2 NaCl
dibenzoylperoxid