Kyslík, oxygenium, 8O, O2, O = O
Stabilnější elektronovou konfiguraci Ne atomy kyslíku získávají přijetím dvou elektronů za vzniku aniontu O2–, vytvořením dvou jednoduchých nebo jedné dvojné kovalentní vazby (H – O – H, O = O, O = C = O), vytvořením jedné jednoduché vazby a přijetím elektronu (OH–).
Téměř ve všech sloučeninách má oxidační číslo –II, jen v peroxidech –I. (Ve sloučeninách s fluorem má kladná oxidační čísla I a II.)
Existují tři izotopy kyslíku: 16O, 17O, 18O
Výskyt
Kyslík je nejrozšířenější prvek na Zemi. Volný tvoří 21 objemových procent atmosféry. Vázaný je ve vodě, minerálech, horninách a v živých organismech.
Příprava a výroba kyslíku
Kyslík se připravuje rozkladem látek bohatých na kyslík:
2 H2O2 → 2 H2O + O2
Peroxid vodíku se rozkládá teplem a ještě lépe v přítomnosti katalyzátoru, kterým může být například burel.
2 KNO3 → 2 KNO2 + O2
2 HgO → 2 Hg + O2
2 PbO2 → 2 PbO + O2
2 KMnO4 → K2MnO4 + O2 + MnO2
2 KClO3 → 2 KCl + 3 O2
4 KClO3 → 3 KClO4 + KCl
KClO4 → KCl + 2 O2
Můžeme ho rovněž připravit elektrolýzou vody.
Vyrábí se frakční destilací kapalného vzduchu nebo elektrolýzou vody.
Vlastnosti kyslíku
Je to bezbarvý plyn bez chuti, bez zápachu, nehoří, podporuje hoření. Je částečně rozpustný ve vodě (důležité pro dýchání vodních živočichů), dá se zkapalnit a ztužit (modrý). Tvoří dvouatomové molekuly.
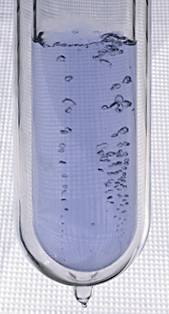
Obr. 1: Zkapalněný kyslík
Kyslík je velmi reaktivní, má oxidační účinky. Přímo se slučuje s většinou prvků za vzniku oxidů.
Za běžné teploty reaguje pomalu např. při rezavění:
4 Fe + 3 O2 → 2 Fe2O3
Při vyšší teplotě reaguje rychle (hoření) – vzniká tepelné a světelné záření:
C + O2 → CO2
2 Mg + O2 → 2 MgO
S + O2 → SO2
Použití kyslíku
Kyslík má široké použití při výrobě kovů v hutnictví, při výrobě oceli ze surového železa, při autogenním svařování a řezání kovů, jako náplň do dýchacích přístrojů. Může sloužit i jako pohon raketových motorů (kapalný kyslík) nebo při čištění odpadních vod.
Přepravuje se v ocelových lahvích s modrým pruhem.
Ozon O3
Vyskytuje se ve vyšších vrstvách atmosféry (25 - 30 km nad Zemí), kde tvoří tzv. ozonovou vrstvu, která chrání živé organismy před UV zářením. Vzniká z O2 při elektrickém výboji:
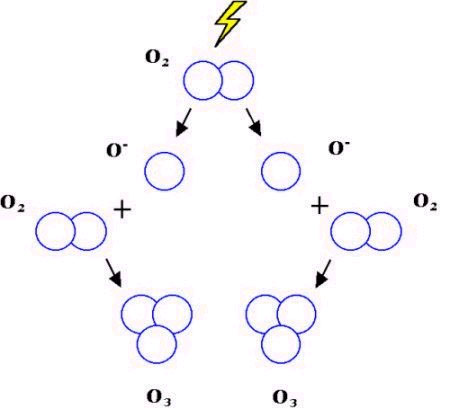
Obr. 2: Schéma vzniku ozónu
Je to velmi reaktivní plyn, má silné oxidační účinky, ničí bakterie. Má charakteristickou vůni. Ve velkých koncentracích je jedovatý. Používá se k dezinfekci pitné vody.
Oxidy
Oxidy jsou dvouprvkové sloučeniny kyslíku s jinými prvky.
Rozdělují se podle prostorové struktury na:
- molekulové oxidy, které tvoří většina nekovů s vysokou elektronegativitou (Cl2O7, SO3, N2O5) a některé kovy s vyššími oxidačními čísly (Mn2O7, OsO4),
- oxidy s atomovou strukturou (mezi atomy je kovalentní vazba), které tvoří prvky ze střední části periodické tabulky (většina kovů a některé nekovy),
- iontové oxidy obsahující anionty O2– a kationty kovu vázané iontovou vazbou, tvoří je alkalické kovy a kovy alkalických zemin.
Podle chemických reakcí s vodou, kyselinami a zásadami se oxidy dělí na:
Kyselinotvorné oxidy (molekulové oxidy a oxidy kovů s ox. číslem větším než V),které se slučují s vodou za vzniku kyslíkatých kyselin:
SO3 + H2O → H2SO4
Oxidy ve vodě nerozpustné reagují se zásadami za vzniku solí:
SiO2 + 2 NaOH → Na2SiO3 + H2O
Zásadotvorné oxidy (iontové oxidy a oxidy kovů s oxidačním číslem menším než IV) se slučují s vodou na hydroxidy:
CaO + H2O → Ca(OH)2
Oxidy ve vodě nerozpustné reagují s kyselinami za vzniku solí:
MgO + 2 HCl → MgCl2 + H2O
Amfoterní oxidy (oxidy kovů s atomovou strukturou a s nižším oxidačním číslem atomu) nereagují s vodou, ale reagují s kyselinami i se zásadami za vzniku solí:
ZnO + 2 HCl → ZnCl2 + H2O
ZnO + 2 NaOH + H2O → Na2[Zn(OH)4] – tetrahydroxozinečnatan sodný
Neutrální oxidy (CO, N2O) nereagují s vodou ani s kyselinami ani se zásadami.
Voda H2O
Výskyt vody
Voda je nejběžnější a nejrozšířenější sloučenina – pokrývá dvě třetiny zemského povrchu. Je složkou organismů (v lidském těle je vody 50 - 72 %) a základní podmínkou života na Zemi. Voda je složkou půdy, je součástí struktury minerálů a hornin (krystalová voda v hydrátech).
Vlastnosti vody
Voda se vyskytuje ve všech třech skupenstvích jako vodní pára (molekuly H2O), voda (vodíkové vazby), led (vodíkové vazby). Led má pravidelnou prostorovou strukturu (sněhové vločky, ledové krystaly).
Vodíkové vazby jsou příčinou vysoké teploty tání a varu (v porovnání s H2S) a anomálie vody – voda má maximální hustotu při 4 °C.
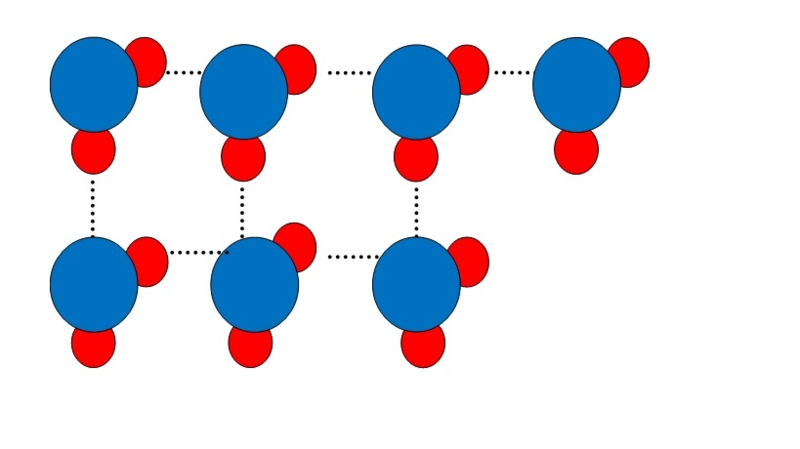
Obr. 3: Vodíkové vazby mezi molekulami vody
Molekula vody je lomená. Vazby mezi vodíkem a kyslíkem jsou polární, voda je tedy polární rozpouštědlo.
Destilovaná voda je pro lidský organismus škodlivá.
Pitná voda obsahuje rozpuštěné látky, které způsobují její tvrdost.
Rozlišujeme tvrdost vody přechodnou (je způsobená přítomností Ca(HCO3)2, Mg(HCO3)2) a trvalou (způsobenou CaSO4, MgSO4).
Přechodnou tvrdost vody lze odstranit povařením.
Trvalou tvrdost odstraníme přidáním sody Na2CO3:
CaSO4 → Ca2+ + SO4 2–
Na2CO3 → 2 Na+ + CO32–
Ca2+ + SO42– + 2 Na+ + CO32– → CaCO3 + 2 Na++ SO42–
Můžeme vodu předestilovat nebo využít ionexů.
Druhy vody
Podle množství rozpuštěných látek rozlišujeme vodu slanou (cca 3% roztok) a sladkou, která může být minerální (cca nad 1% rozpuštěných solí), tvrdá (cca 0,05% roztok), měkká a destilovaná.
Podle obsahu nečistot se voda rozlišuje na destilovanou, pitnou, užitkovou a odpadní.
Ve vodárnách se upravuje voda z podzemních zdrojů či z některých vodních nádrží na pitnou. K úpravám se používají síta, usazovací nádrže a pískové filtry, kde se voda zbavuje nežádoucích pevných látek. Může se čistit i přidáním chemických látek (např. KMnO4 zbaví vodu nadměrného množství železa), na závěr se dezinfikuje chlorem, ozonem popř. UV-zářením.
V čistírnách odpadních vod se odpadní voda přečišťuje na užitkovou, která se vypouští do vodních toků. K čištění se používají síta, usazovací nádrže, kde se voda čistí chemicky a biologicky pomocí bakterií.
Peroxid vodíku H2O2
Peroxosloučeniny mají dva atomy kyslíku navzájem vázané kovalentní vazbou: – O–I – O–I –
Laboratorně lze peroxid vodíku připravit reakcí:
BaO2 + H2SO4 → BaSO4 + H2O2
Peroxid vodíku je bezbarvá olejovitá kapalina v bezvodém stavu výbušná. Je rozpustný ve vodě. Chová se jako slabá kyselina, její soli jsou peroxidy M2IO2 a hydrogenperoxidy MIHO2. Je nestálý, rozkládá se na vodu a kyslík:
2 H2O2 → 2 H2O + O2
Jako katalyzátory lze využít MnO2, Pt, jako inhibitory močovinu nebo H2SO4.
Peroxid vodíku má oxidační účinky:
2 KI + H2O2 + H2SO4 → I2 + K2SO4 + 2 H2O
Má však i redukční účinky:
2 KMnO4 + 5 H2O2 + 3 H2SO4 → 5 O2 + K2SO4 + 2 MnSO4 + 8 H2O
Používá se jako dezinfekční prostředek při poranění, bělící prostředek (na textil, papír, odbarvování vlasů), k čištění odpadních vod.
Obrázky
|
|
... při koncetraci kyslíku ve vzduchu pod 20% se u člověka objevují bolesti hlavy, dušnost, klesne-li koncentrace pod 15%, ztrácí člověk vědomí? |
... zdrojem ozonu jsou i kopírky nebo laserové tiskárny? Neměly by proto být v nevětrané místnosti.
Vytvořte vzorce sloučenin:
oxid dusný
oxid křemičitý
peroxid barnatý
oxid manganičitý
oxid wolframový
Vytvořte názvy sloučenin:
CaO
Na2O2
As2O3
Fe2O3 ∙ n H2O
SeO2