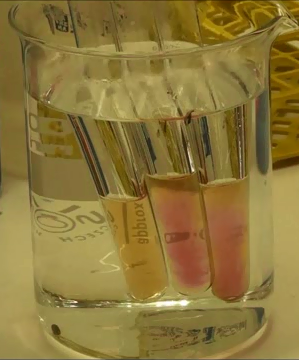Vlastnosti a reakce alkoholů
Fyzikální vlastnosti
Alkoholy mají poměrně vysoké teploty varu, protože vytvářejí vodíkové vazby. Nejnižší alkoholy jsou kapaliny příjemné vůně a chuti, libovolně se mísí s vodou. S molekulovou hmotností ubývá příjemné vůně, chuti i rozpustnosti ve vodě, od C4 jsou kapaliny s nepříjemnou vůní, vyšší jsou pevné krystalické látky. Rozpustnost alkoholů ve vodě stoupá s počtem hydroxylových skupin v molekule. Alkoholy s dvěma a více hydroxylovými skupinami jsou sladké.
Biologické vlastnosti
Některé alkoholy mají výrazně toxické vlastnosti, především methanol, etylenglykol i ethanol. Otravy se projevují alkoholovým opojením, bolestmi zažívacího ústrojí, otupením smyslů, narušením rovnováhy, změnami chování, ztrátou vědomí, u methanolu slepotou. Časté jsou nežádoucí interakce s léčivy (antidepresiva, hypnotika, antibiotika, paralen,…).
Chemické vlastnosti alkoholů
Vycházejí z přítomnosti polarizované hydroxyskupiny C – Oδ -– Hδ+.
Alkoholy mají amfoterní charakter, v přítomnosti různých látek se mohou chovat jako kyseliny nebo zásady. Rozdíl elektronegativit prvků v hydroxylové skupině způsobuje polaritu vazby a její slabě kyselý charakter; dva volné elektronové páry u kyslíkového atomu způsobují zásaditý charakter.
Vznik alkoholátů
Působením alkalických kovů tvoří alkoholy tzv. alkoholáty (alkoxidy), jedná se o silné zásady srovnatelné s hydroxidy alkalických kovů:
2 R – OH + 2 Na → 2 R – ONa + H2
Vznik etherů
Alkoholáty mají vlastnosti nukleofilních činidel, reagují s halogenderiváty za vzniku etherů:
R1 – ONa + R2 – X → R1 – O – R2 + Na+ + X-
Reakce se silným kyselinami
Působením silných anorganických kyselin (např. kyselina sírová) vznikají oxoniové soli, které za přítomnosti vody hydrolyzují zpět na alkohol a anorganickou kyselinu:
R – OH + HO – SO2 – OH ⇆ R – O+H2 + -O – SO2 – OH alkoxonium síran
R – O+H2 + -O – SO2 – OH ⇆ R – OH + 2 H3O+ + SO42-
Oxoniové soli nelze izolovat v pevném stavu, při izolaci dochází k rozkladu na alkohol a kyselinu.
Lucasův test
Reakce s HCl slouží k rozlišení terciárních, sekundární a primárních alkoholů, nejsnadněji reagují terciární, primární prakticky nereagují:
R-OH + HCl ⇆ R – OH2+ Cl- → R-Cl + H2O
alkoxonium chlorid
Oxidace
Primární a sekundární alkoholy podléhají snadno oxidaci na karbonylové sloučeniny. V případě primárních alkoholů probíhá oxidace na aldehydy, případně až na karboxylové kyseliny:
primární alkoholy → aldehydy → karboxylové kyseliny.
Oxidaci se provádí bud reakcí s kyslíkem nebo dehydrogenací na katalyzátorech.
R- CH2OH + ½ O2 → R-CHO + H2O oxidace na aldehyd
CH3OH → H-CHO + H2 dehydrogenace na formaldehyd
R-CHO + ½ O2 → R-COOH oxidace na karboxylovou kyselinu
R-CH(OH)R + ½ O2 → R-CO-R + H2O oxidace na keton
CH3 – CH(OH) – CH3 → CH3 – CO – CH3 propanon (aceton, dimethylketon)
Terciární alkoholy jsou při působení oxidačních činidel stálé: terciární alkoholy → neoxidují se. Při silné oxidaci může dojít ke štěpení řetězce.
Esterifikace
Esterifikace je kondenzační reakce, při které reagují alkoholy s organickými nebo méně často anorganickými kyselinami za vzniku esteru:
R1 – COOH + R2 – OH → R1–COO– R2 + H2O
org.kyselina alkohol ester
CH3COOH+CH3OH → CH3COOCH3 + H2O
k. octová methanol methylacetát (methylester k. octové)
HNO3 + R – OH → R – O – NO2 + H2O
kys. dusičná alkohol alkylnitrát
Eliminace – dehydratace
Odštěpením vody vzniká alken, např. dehydratací ethanolu vzniká ethen:
CH3-CH2-OH → CH2 = CH2 + H2O kat, t
Při eliminaci ze sekundárních a terciárních se odštěpuje – OH skupina s vodíkem toho C, který má nejmenší počet H -atomů, získává se hlavně nejvíce alkylovaný alken – Zajcevovo pravidlo.
Mezimolekulární dehydratací vzniká ether:
2CH3-CH2-OH → CH3-CH2-O-CH2-CH3 + H2O

Obr. 1: Primární, terciární a sekundární alkohol