Anhydridy 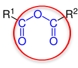
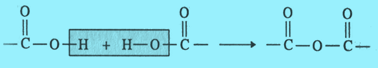
Vznikají spojením dvou skupin COOH karboxylových kyselin za současného odštěpení molekuly vody. Jako dehydratační činidlo se používá oxid fosforečný.
Rozdělení
-
jednoduché – zbytky stejných karboxylových kyselin,
-
smíšené - zbytky různých karboxylových kyselin,
-
cyklické.
Názvosloví
Systematický název
Základ názvu název kyseliny (latinský nebo systematický) + anhydrid.
Opisný název
Slovo anhydrid + 2.pád příslušné kyseliny, např. anhydrid kyseliny octové a propionové.
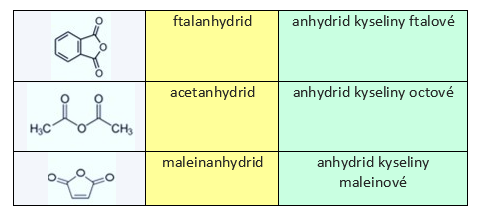
Tab. 1: Příklady názvů anhydridů
Vlastnosti
Anhydridy nižších karboxylových kyselin jsou ostře páchnoucí kapaliny, vyšší anhydridy jsou krystalické látky. Mají vyšší teploty varu než odpovídající kyseliny. Všechny anhydridy jsou téměř nerozpustné ve vodě, ale poměrně rychle s vodou reagují. Rozpouštějí se například v diethyletheru. Patří mezi silná acylační činidla, jsou ale méně reaktivní než halogenidy odpovídajících kyselin.
Důležité reakce
Andyridy karboxylových kyselin jsou výborná acylační činidla (ale slabší než acylhalogenidy, reakcí vznikají nejrůznější deriváty karboxylových kyselin.
Hydolýza: reakcí anhydridů s vodou se obnovují původní kyseliny.
CH3-CO-O-CO-CH3 + H2O → 2 CH3COOH
Alkalická hydrolýza: reakce s hydroxidem alkalického kovu probíhá rychleji, protože hydroxidy jsou silnější nukleofilní činidla než voda. Při této reakci vzniká voda a sůl karboxylové kyseliny.
(RCO)2O + 2 NaOH → 2 RCOONa + H2O
Alkoholýza: reakcí anhydridů s alkoholy nebo fenoly vznikají estery a karboxylové kyseliny, nukleofilním činidlem v této rekci je alkohol nebo fenol.
CH3-CO-O-CO-CH3 + R´OH → CH3-CO-O-R´ + CH3COOH
Amonolýza: reakcí anhydridů s amoniakem, případně primárním nebo sekundárním aminem, vzniká amid nebo substituovaný amid karboxylové kyseliny a karboxylová kyselina.
(RCO)2O + 2 NH3 → 2 RCONH2 + RCOOH
Reakce s halogenvodíkovými kyselinami: působením halogenvodíkových kyselin se tvoří acylhalogenid a kyselina.
(RCO)2O + HX → 2 RCOX + RCOOH
Příprava
Obecně anhydridy vznikají dehydratací z příslušných kyselin za přítomnosti dehydratačních činidel, např. oxidu fosforečného.
2 RCOOH → (RCO)2O + H2O
V praxi se častěji využívá reakce acylhalogenidu karboxylové kyseliny s její sodnou solí. Reakce probíhá mechanismem nukleofilní substituce .
R-CO-ONa + R´-CO-Cl → R-CO-O- CO-R´ NaCl
V technické praxi jsou využívány i speciální metody výroby anhydridů, např. katalytická oxidace aromatických uhlovodíků (výroba maleinanhydridu a ftalanhydridu).
Tyto výroby probíhají za poměrně vysokých teplot 400-500oC a jako katalyzátory se používají kat.V2O5 + P2O5.(1)
- maleinahydrid oxidací benzenu:
C6H6 + 9/2 O2 → C2H2(CO)2O + 2CO2 + 2 H2O
- maleinanhydrid oxidací směsí C4 uhlovodíků:
2 CH3CH2CH2CH3 + 7 O2 → 2 C2H2(CO)2O + 8 H2O
- ftalanhydrid oxidací o - xylenu:
C6H4(CH3)2 + 3 O2 → C6H4(CO)2O + 3 H2O
- ftalanhydrid oxidací naftalenu:
C10H8 + 9/2 O2 → C6H4(CO)2O + 2 H2O + 2CO2
Využití
Využívají se jako acylační činidla.
Acetanhydrid (CH3CO)2O patří k nejvýznamnějším z anhydridů, používá se při výrobě kyseliny acetylsalicylové. Průmyslová výroba je založena na karbonylaci methylesteru kyseliny octové:
CO + CH3COOCH3 → (CH3CO)2O katalyzátor: jodid lithný, jodid rhoditý
Maleinanhydrid C2H2(CO)2O  je pevná bezbarvá látka ostře páchnoucí, používá se k výrobě nenasycených polyesterů.
je pevná bezbarvá látka ostře páchnoucí, používá se k výrobě nenasycených polyesterů.
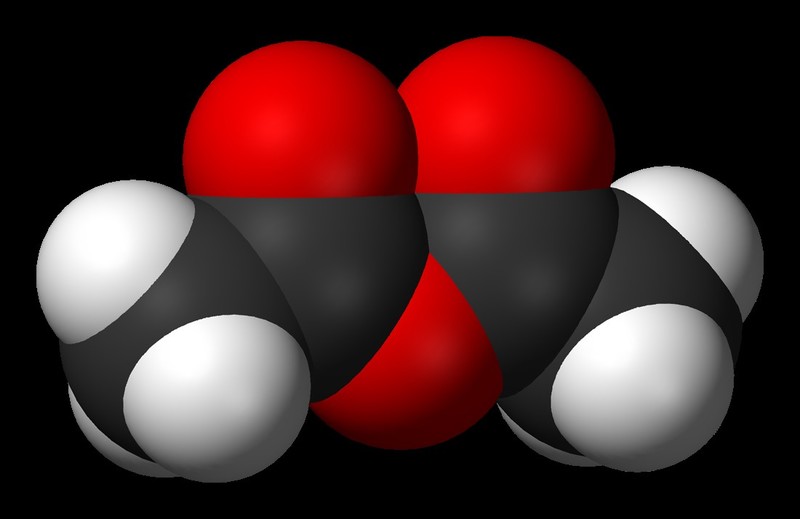
Obr. 1: Model acetanhydridu


