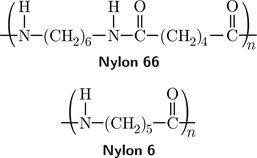
Amidy karboxylových kyselin 
Odvozují se náhradou –OH skupiny karboxylové skupiny aminoskupinou - NH2. Oba atomy vodíku aminoskupiny - NH2 mohou být substituovány uhlovodíkovými zbytky.
Názvosloví
Systematický název
Základ je odvozen od názvu kyseliny (latinský nebo systematický) + amid, atom uhlíku se započítává, např. acetamid, butandiamid, sukciamid, méně často se tvoří způsobem: uhlovodíkkarboxamid (uhlík se nezapočítává), např. cyklopentankarboxamid.
Opisný název
Tvoří se spojením slova amid, případně diamid a 2.pádem kyseliny, např.amid kyseliny octové, amid cyklopentankarboxylové kyseliny, diamid kyseliny jantarové
Tab. 1: Příklady názvů amidů

Vlastnosti
Amidy organických kyselin jsou kapalné (formamid) nebo krystalické látky s vysokými body tání a varu, což je způsobno přítomností vodíkových můstků mezi jejich molekulami. Amidy jsou málo reaktivní, nelze z nich přímo připravit jiné funkční deriváty. Varem s vodou poskytují amoniak a příslušnou karboxylovou kyselinu. Amidové vazby se vyskytují v bílkovinách a stabilizují je. Dehydratací vznikají nitrily. Složité amidy jsou biologicky významné, např. součást bílkovin apod.
Reakce
Hydrolýzou vznikají příslušné karboxylové kyseliny a amoniak, u substituovaných vzniká sekundární amin:
kyselá hydrolýza
R-CO-NH2 + H2O + H+ → R-COOH + NH4+ vzniká kyselina
zásaditá hydrolýza
R-CO-NH2 + OH- → R-COO- + NH3 vzniká sůl karboxylové kyseliny
Dehydratací vzniká nitril: R-CO-NH2 → R-C≡N + H2O
Hoffmannovo odbourávání amidů
Jedná se o reakci s alkalickým chlornanem nebo bromnanem (NaOCl, KOBr) za vzniku aminů s řetězcem o 1 uhlík kratším:
R-CO-NH2 + NaOCl → R-NH2 + NaCl + CO2
Příprava
Amidy se obvykle připravují reakcí chloridů nebo anhydridů kyselin s amoniakem nebo primárním, případně sekundárním aminem. Funkční deriváty karboxylový kyselin lze převést na amidy za mírnějších podmínek než samotné kyseliny, reaktivita klesá v řadě: chloridy > anhydridy > estery.
R-CO-X + NH3 → R-CO-NH2 + HX
halogenid amid
R-CO-O-CO-R + 2 NH3 → R-CO-NH2 + R-COONH4
anhydrid amid amonná sůl
Často se získávají termickým rozkladem amonných solí, které vznikají reakcí kyseliny s amoniakem.
R-COOH + NH3 → R-CO-ONH4 → R-CO-NH2 + H2O
kyselina amonná sůl amid
Využití
Acetamid CH3CONH2 je hygroskopická a krystalická látka, má použití v syntéze.
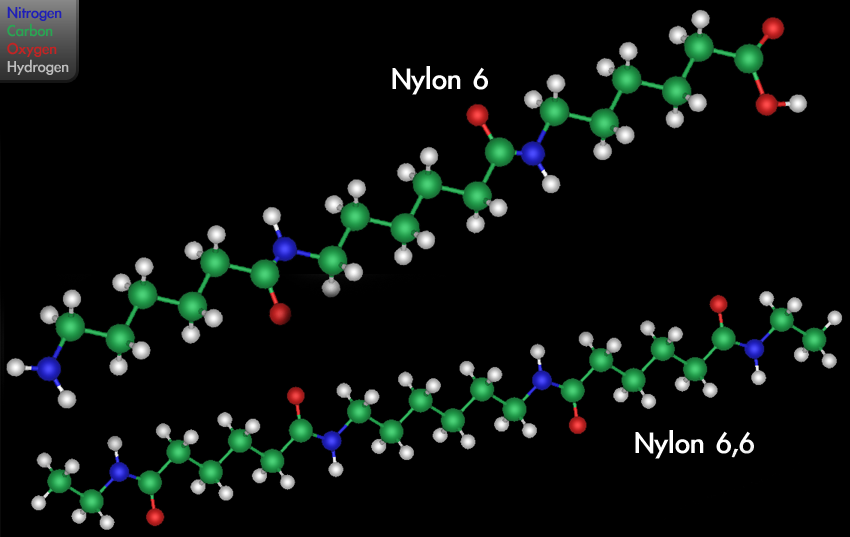
Polyamidy PA (nylon) je synteticky připravené textilní vlákno. Vzniká reakcí diaminu (hexamethylendiamin) s dikarboxylovou kyselinou (kyselina adipová). Molekuly jsou spojeny amidickou vazbou. Kevlar je para-aramidové vlákno s velkou pevností a mechanickou odolností, nahrazuje a odlehčuje metalické ochranné a funkční prvky; používá se k výrobě neprůstřelných vest, popruhů, ochranných oděvů apod.
Obr. 1: Nylon

Obr. 2: Vzorec para-aramidu