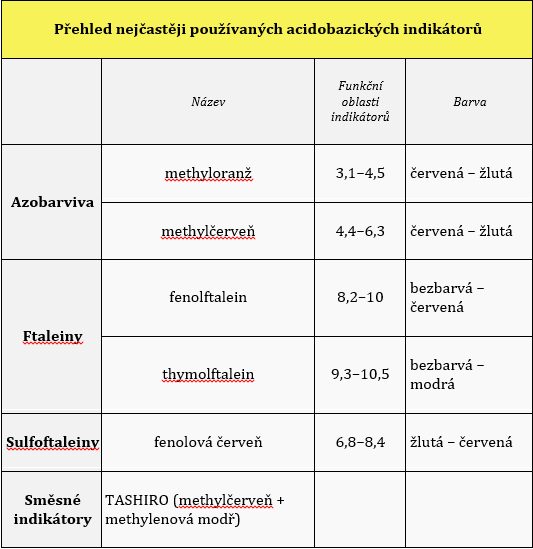
Vlastnosti a reakce aminů
Fyzikální vlastnosti
Nižší aminy (methylamin, dimethylamin, trimethylamin) jsou hořlavé plyny, dobře rozpustné ve vodě, mají charakteristický čpavý zápach páchnoucí po rybách.
Střední aminy jsou kapalné, páchnou po rybině; některé diaminy mají mrtvolný zápach, např. kadaverin, což je pentan-1,5-diamin (cadaver = mrtvola).
Vyšší aminy jsou kapaliny nebo tuhé látky, bez zápachu; se stoupajícím počtem uhlíkových atomů v molekule zároveň klesá rozpustnost ve vodě.
Biologické vlastnosti
Většinou mají výrazné biologické účinky; jsou toxické nebo dráždivé, některé jsou karcinogenní (benzidin, β-naftylamin), jiné mají výrazné fyziologické účinky (histamin, adrenalin, amfetamin).
Chemické vlastnosti
Aminoskupiny obsahují volný elektronový pár, to způsobuje zásadité a nukleofilní vlastnosti. Zásaditost aminů je ve srovnání s amoniakem vyšší a roste s počtem alkylových substituentů, které působí svým +I efektem. U terciárních aminů však působí již i sterické důvody a objemné substituenty zásaditost snižují.
Aromatické aminy jsou méně zásadité, protože dochází k zapojení volného elektronového páru dusíku do aromatického jádra (konjugace s π-elektrony aromatického jádra) a bude hůře přijímat H+:
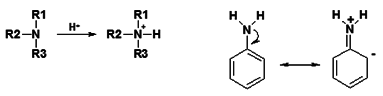
Aminy se chovají jako nukleofilní činidla a atakují místa s elektronovým deficitem δ+. Se zvětšujícím se počtem a objemem uhlovodíkových substituentů klesá reaktivita charakteristické skupiny.
CH3NH2 + H2O → CH3NH3+OH- methylamoniumhydroxid
Reakce s kyselinami - vznikají amoniové soli:
CH3CH2NH2 + HCl → CH3CH2NH3+Cl- ethylamonium-chlorid
Amoniové soli jsou dobře rozpustné ve vodě. Z vodných roztoků lze působením alkalického hydroxidu uvolnit amin:
CH3CH2NH3+Cl- + NaOH → CH3CH2NH2 + NaCl + H2O ethylamin
Reakce s alkylhalogenidy – vzniká dialkyl-, trialkyl- až tetraalkyl-amonium chlorid, v zásaditém prostředí přechází na sekundární, terciární aminy, případně až na kvartérní amoniovou sůl:
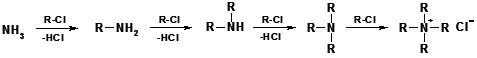
NH3 + RX → RNH3+X- → RNH2 primární
RNH2 + RX → RNH2+X- → R2NH sekundární
R2NH + RX → R3NH+X- → R3N terciární
R3N + RX → R4N+X- kvartérní amoniová sůl
Kvartérní soli jsou obdobou amonného kationtu NH4+, všechny vodíky jsou nahrazeny uhlovodíkovými zbytky.
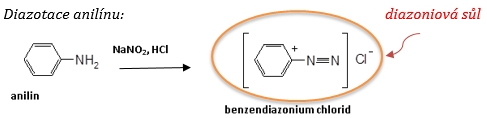
Diazotace
Je reakce primárních aromatických aminů s kyselinou dusitou za vzniku diazoniových solí Ar-N+≡NX- s charakteristickou diazoskupinou.
Reakce probíhá za nízkých teplot (kolem 0 °C) a přebytku minerální kyseliny. Kyselina dusitá je nestabilní, proto je při reakci vytěsňována z dusitanu silnější kyselinou.
Diazoniové soli jsou reaktivní, nestálé, v suchém stavu se výbušně rozkládají za uvolnění dusíku, zpracovávají se v suspenzi. Mají velký význam pro další syntézy – kopulace při výrobě barviv a Sandmayerovy reakce.
C6H5-NH2 + NaNO2 + 2 HCl → [C6H5--N≡N](+)Cl- + NaCl + 2 H2O
Průběh diazotace
"Reakcí dusitanu a kyseliny se uvolní nestálá kyselina dusitá, ta se rychle protonizuje:
NaNO2 + HCl → HNO2 + NaCl HNO2 + H(+) → H2N(+)O2.
Následně probíhá pomalá reakce s primárním aminem za vzniku nitrosaminu:
Ar-NH2 + H2N(+)O2 → Ar-NH-NO + H(+) + H2O. Nakonec proběhne rychlá reakce přes diazohydroxid až na diazoniovou sůl:
Ar-NH-NO + H(+) → Ar-N=NO(+)H2 → [Ar-N≡N](+) + H2O "(1)
Kopulace
Je reakce diazoniových solí s aromatickými aminy a fenoly za vzniku azosloučenin Ar-N=N-Ar se skupinou azo -N=N-.
Reakce s fenoly probíhá v zásaditém prostředí (pH 8-10), z fenolu vzniká fenolát, který způsobuje vyšší + M efekt. Pro rekci s aminy se používá mírně kyselé prostředí.
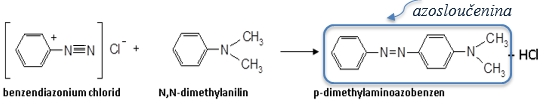
Reakce probíhá do polohy 4 (para); pokud je obsazena, potom probíhá reakce do polohy 2 (ortho).
Azosloučeniny mají často charakter barviv, tzv. azobarviv.
Barevnost org. sloučenin je dána přítomností skupiny zvané chromofor (u azobarviv -N=N-). Chromofor je součástí rozsáhlého konjugovaného π-elektronového systému, který pohlcuje určitou vlnovou délku elektromagnetického vlnění ve viditelné oblasti světla a látka se jeví jako barevná (odražené světlo se jeví v barvě doplňkové).
Mezi azobarviva patří i indikátory, např. pH indikátory methyloranž a methylčerveň. Změna zabarvení v kyselém a zásaditém prostředí je způsobena vnitřním přesmykem v molekule (často přesmyk vodíku).

Obr. 1: Methyloranž při různých hodnotách pH
Příklad výroby Oranž II:
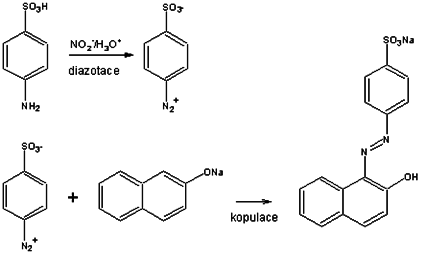
Kopulace diazotované kyseliny sulfanilové s alkalickým roztokem 2-naftolu (2)
Sandmayerovy reakce
Reakce diazoniových solí s nukleofily za vzniku různě substituovaných aromatických derivátů a současného odštěpení dusíku. Slouží k přípravě substituovaných aromatických sloučenin.
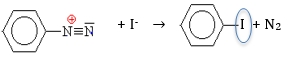
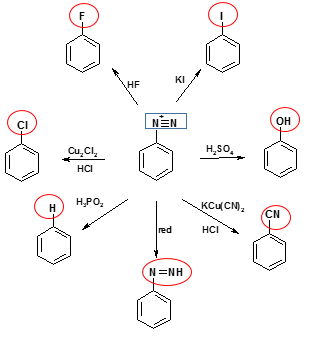
Využití Sandmayerovy reakce (3)
Elektrofilní aromatická substituce
Aminoskupina je substituent 1. třídy, aktivuje silně aromatické jádro, orientuje další substituce do polohy 2 (ortho) a 4 (para).
Bromace probíhá snadno až do 3. stupně (3):
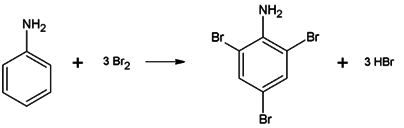 viz video
viz video
Nitrace může vést k oxidaci aminoskupiny, proto se skupina chrání acetylací (3):
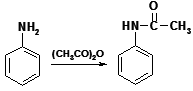
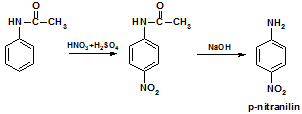
Substituce aminoskupiny probíhá poměrně obtížně – prakticky nikdy se neprovádí!