Teplota varu
Úkol: Stanovení teploty varu ve zkumavce s vloženou kapilárou.
Pomůcky: stojan, vařič, kapiláry, lihový kahan, pipety, držák na zkumavky, svorka, kádinka, zkumavka se silikonovým olejem, malá zkumavka s teploměrem, tyčinka.
Chemikálie:
-
ethanol (ethylalkohol)
-
propan-1-ol (n-propylalkohol)
-
butan-1-ol (n-butanol)
-
pentan-1-ol (n-amylalkohol).
Bezpečnost práce:
Práce s elektrickým vařičem, horký olej, brýle.
Pracovní postup:
Malou zkumavku připojenou k teploměru vypláchneme alkoholem, který stanovujete, do ní odpipetujeme 0,4 ml zkoumaného alkoholu. Kapiláru zatavíme na lihovém kahanu a vsuneme do alkoholu ve zkumavce tak, aby byla zataveným koncem nahoru a sahala až na dno. Zkumavku s teploměrem osušíme buničinou a vsuneme do větší zkumavky s olejem. Upevníme držákem ke stojanu tak, aby nedosahovala až na dno v kádince a hladina oleje byla vyšší než hladina oleje ve zkumavce. Zapneme vařič na nízký stupeň. Během vyhřívání mícháme olejem, aby nevznikl utajený var (v kádince tyčinkou, ve zkumavce nadzvednutím teploměru). Až začne z kapiláry unikat rychlý proud bublinek, zapíšeme první teplotu a vypneme vařič. Držák se zkumavkami a teploměrem vysuneme nad kádinku a upevníme. Druhou teplotu zapíšeme, když do kapiláry se začne nasávat kapalina. Zjištěná teplota varu - průměr z obou teplot. Ostatní alkoholy stanovíme stejným způsobem. (Obr. 2)
Závěr:
Zjištěné hodnoty zapíšeme do tabulky, vypočítáme průměr.
| alkoholy | teplota varu čisté látky | 1. zjištěná teplota varu | 2. zjištěná teplota varu | průměr z obou teplot |
| ethanol (ethylalkohol) | ||||
| propan-1-ol (propan1-ol) | ||||
| butan-1-ol (n-butanol) | ||||
| pentan-1-ol (n-amylalkohol) |
Teplota tání
Úkol: Stanovení teploty tání organických látek na kovovém bloku.
Pomůcky: kovový blok, třecí miska, tlouček, lžička, špachtle, kapiláry, lihový kahan, skleněná trubice, teploměr.
Chemikálie: kyselina benzoová, kyselina citronová, močovina, kyselina sorbová.
Bezpečnost práce: Zásady práce s lihovým kahanem.
Pracovní postup:
Chemikálie rozetřeme ve třecí misce. Kovový blok upevníme do stojanu a do většího otvoru vsuneme teploměr. Zatavíme kapiláru nad lihovým kahanem a naplníme rozetřenou látkou tak, aby byl povrch dobře vidět v otvoru bloku. Zahříváme nad plamenem lihového kahanu a lupou pozorujeme látku v kapiláře. Zpočátku zahříváme rychleji a asi 20oC před požadovanou teplotou snížíme zahřívání, aby teplota stoupala 4oC za minutu. Začátek teploty tání borcení látky, konec teploty tání zkapalnění.(Obr. 3)
|
|
teplota tání čisté látky |
začátek teploty tání |
konec teploty tání |
|
kyselina benzoová |
|
|
|
|
kyselina citronová |
|
|
|
|
kyselina sorbová |
|
|
|
|
močovina |
|
|
|
Závěr:
Vyhodnoťte čistotu chemikálií.
Která látka byla nejčistší? (nejvíce se blíží teplotě tání čisté látky a má úzké rozmezí teplot).
Hustota kapalin
Úkol: Stanovení hustoty hustoměrem, pyknometrem, hydrostatickými vahami. Stanovení % obsahu sacharózy cukroměrem a % obsahu ethanolu lihoměrem.
Pomůcky: pyknometr, erlenmeyerova baňka, válec na měření hustoty, hustoměr, teploměr, hydrostatické váhy, lihoměr, cukroměr.
Chemikálie: NaHCO3, kyselina vinná, sacharóza, ethanol.
Bezpečnost práce: Zařaďte použité látky do skupin nebezpečnosti.
Úkol: Výpočty:
Připravte 300g 3 % roztoku NaHCO3.
Připravte 300g 5 % roztoku kyseliny vinné.
Připravte 300g 6 % roztoku sacharózy.
Připravte 300ml 86% roztoku ethanolu.
Pracovní postup:
1. Stanovte hustotu pyknometricky.
2. Stanovte hustotu pomocí hustoměru.
3. Stanovte hustotu pomocí hydrostatických vah.
Sestavte váhy a zavěste měřící tělísko. Pomocí šroubků na konci vahadla upravte nulovou polohu hrotu (musí být uprostřed stupnice). Vytemperujte roztok a nalijte do válce tak, aby bylo měřící tělísko celé ponořené v kapalině. Na rameno vah postupně zavěšujte závaží od největšího až po nejmenší tak, až hrot opět bude uprostřed stupnice. Přečtěte hustotu, tělísko umyjte a stejným způsobem zjistěte hustotu dalších látek.(Obr. 4)
4. Stanovte % sacharózy cukroměrem a % ethanolu lihoměrem.
| roztoky | pyknometr | hustoměr | hydrostatické váhy | tabulky |
| NaHCO3 | ||||
| kyselina vinná | ||||
| sacharóza | ||||
| ethanol |
Závěr:
Výsledky porovnejte s hustotou čistých látek uvedených v tabulkách.
Dynamická viskozita
Úkol: Stanovení dynamické viskozity roztoku sacharózy pomocí Höpplerova viskozimetru.
Pomůcky: Höpplerův viskozimetr, stopky, tyčinka, kádinky, váhy, lžička, pyknometr, teploměr.
Chemikálie: sacharóza, ethanol.
Bezpečnost práce: Práce se sklem a hořlavinou.
Úkol:
Připravte 150g 10% roztoku sacharózy.
Připravený roztok vytemperujte na 20°C a stanovte hustotu pyknometrem.
Výpočet přípravy 150 g 10% roztoku sacharózy:
Výpočet hustoty:
| m – suchý pyknometr | |
| m1 – pyknometr s destilovanou vodou | |
| m2 – pyknometr s roztokem sacharózy |
Pro výpočet hustoty (ρ) měřené kapaliny platí vztah:
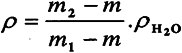
ρ 10% roztoku sacharózy =
Pracovní postup:
Trubici viskozimetru z jedné strany uzavřeme plochou zátkou a zašroubujeme šroubovou hlavicí. Otočíme a naplníme roztokem asi 2cm pod okraj, vložíme zváženou kuličku, zátku s otvorem, uzavřeme plochou zátkou a zašroubujeme. V trubici nesmí být vzduchová bublina. Upravíme vodorovnou polohu viskozimetru a 5x měříme dobu pádu kuličky od vrchní rysky k nejspodnější po otočení o 180°(viz obrázek). Z pěti měření vypočítáme průměr a v sekundách dosadíme do vzorce. (Obr. 5)
10% sacharóza
| 1. měření | 2. měření | 3. měření | 4. měření | 5. měření | průměr | |
| doba pádu (s) |
Výpočet:
η = s . ( ρ kuličky — ρ roztoku ) . K kuličky [Pa.s]
viskozita = sekundy x (hustota kuličky – hustota roztoku) x konstanta kuličky
Závěr:
Dynamickou viskozitu přepočítejte na kinematickou a výsledky porovnejte s tabulkami.
/ hustota roztoku v kg.m-3/
|
viskozita |
dynamická /η/ |
kinematická /ν/ |
tabulky /ν/ |
rozdíl |
|
10% sacharóza |
|
|
|
|
Kinematická viskozita
Úkol: Stanovení kinematické viskozity 80 % roztoku glycerolu pomocí Ubbelohdova viskozimetru.
Pomůcky: Ubbelohdův viskozimetr, stopky, odměrný válec 50ml a 250ml, kádinka 100ml, tyčinka, teploměr, pipetík.
Chemikálie: glycerol, ethanol.
Bezpečnost práce: Práce se sklem a hořlavinou.
Pracovní postup:
a) výpočet přípravy 50g 80%roztoku glycerol (hustota 100% glycerolu =1,26 g.ml-1).
b) postup měření
Vytemperujeme 80% glycerol na 20oC, odpipetujeme 15ml, přeneseme do trubice č.1. Uzavřeme prstem trubici č. 3 a nasáváme pipetíkem glycerol do trubice č. 2 až k hornímu okraji nejvyšší koule. Viskozimetr stojí v 250 ml odměrném válci kolmo. Pipetík i prst uvolníme z trubice a měříme 5x dobu za kterou glycerol proteče od horní rysky po spodní. Ihned po ukončení viskozimetr umyjeme vodou a vypláchneme ethanolem. (Obr. 6)
2 3 1
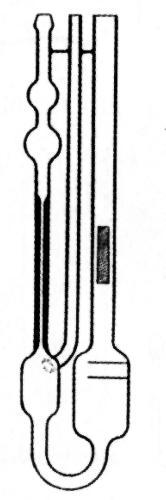
Obr. 1: Ubbelohdův viskozimetr
| 1. měření | 2.měření | 3.měření | 4.měření | 5.měření | průměr | |
| naměřená doba |
Výpočet:
√ = K .t . 106 (m2 . s-1)
K – konstanta viskozimetru (je pro každý viskozimetr charakteristická, lze ji najít na trubici viskozimetru)
t – vypočítaná průměrná hodnota času (v sekundách)
Závěr:
Výsledek porovnejte s tabulkami.
Měření pH
Úkol: Měření pH daných látek na pH metru ACI.
Pomůcky: univerzální pH papírky, kádinka 100ml, teploměr, erlenmeyerova baňka 100ml, pH metr ACI 1.
Chemikálie: roztoky - kyseliny askorbové, hydrogenuhličitanu sodného, sacharózy.
Pracovní postup: (Obr. 7)
-
Spojíme elektrodu s pH metrem a zapojíme pH-metr do zásuvky.
-
Přístroj zapneme černým tlačítkem doprava.
-
Vytemperujeme vzorky a standardy na 20°C a změříme pH u vzorků univerzálním papírkem.
-
Z elektrody sundáme ochranou krytku, opláchneme destilovanou vodou a osušíme buničinou.
-
Kombinovanou elektrodu vsuneme do standardu pH 7 tak hluboko, aby byl ponořený černý kroužek na elektrodě a pravým kolečkem (označeným pH 7) nastavíme na displeji hodnotu 7,00.
-
Elektrodu opláchneme destilovanou vodou, osušíme buničinou a vsuneme do standardu pH 4 nebo pH 9 (podle pH univerzálního papírku) a levým kolečkem (označeným pH-X) nastavíme na displeji hodnotu 4,00 nebo 9,00.
-
Elektrodu opláchneme, osušíme a vsuneme do vzorku. Na displeji odečteme hodnotu pH vzorku při prvním pře bliknutí.
-
Elektrodu opláchneme destilovanou vodou, osušíme a nasadíme ochranou krytku s uchovávacím roztokem.
| roztoky | hodnota pH |
| kyselina askorbová | |
| hydrogenuhličitan sodný | |
| sacharóza |
Závěr: Porovnejte výsledky měření na pH metru.
Refraktometrie
Úkol: Měření závislosti indexu lomu roztoku sacharózy na jeho koncentraci. Naměřené hodnoty zapište do tabulky, vypracujte graficky.
Pomůcky:kapkový refraktometr Abbe 3-6, erlenmeyerova baňka 100 ml, teploměr, střička, odměrný válec, buničina.
Chemikálie: sacharóza.
Bezpečnost práce: Práce s elektrickým přístrojem.
Výpočty:
Vypočítejte a připravte 50 g 2%, 5%, 7%, 9%, 12% roztoku sacharózy.
Měření na kapkovém refraktometru Abbe 3-6
Připravené roztoky sacharózy vytemperujeme na 20oC.Po odtažení krytu hranolu kápneme na hranol refraktometru roztok sacharózy. Kryt uzavřeme a zapneme osvětlení hranolu a stupnice. Zaostříme okulárem a kompenzačním kolečkem zprava nahoře odstraníme barevné spektrum. Velkým kolečkem vpravo dole posuneme rozhraní světla a stínu do středu nitkového kříže. Na horní stupnici přečteme hodnotu v % a na dolní stupnici index lomu. Před měřením dalšího roztoku, hranol opláchneme destilovanou vodou a osušíme buničinou.(Obr. 8)
| roztoky sacharózy | Abbe % | n | tabulky n |
Závěr:
Zjištěné hodnoty sestavte do tabulky a porovnejte přesnost měření pomocí tabulek.
Vypracujte graf závislosti indexu lomu na koncentraci.
Zdroje
- AUTOR NEUVEDEN. wikipedidia.cz [online]. [cit. 8.11.2014]. Dostupný na WWW: http://cs.wikibooks.org/w/index.php?title=Pyknometrick%C3%A9_stanoven%C3%AD_hustoty&oldid=22763>
- BARTOVSKÁ, L. a ŠIŠKOVÁ. Fyzikální chemie povrchů a koloidních soustav. VŠCHT. Praha, 1999.
- KLOUDA, Pavel. Fyzikální chemie: studijní text pro SPŠCH. 2., upr. a dopl. vyd. Ostrava: Pavel Klouda, 2002. 139 s. ISBN 80-86369-06-4.
Obrázky
- Obr. 1: Autor neznámý. ISBN [online]. [cit. 17.11.2014]. Dostupný na WWW: ISBN http://vydavatelstvi.vscht.cz/knihy/uid_es-001/hes; http://vydavatelstvi.vscht.cz/knihy/uid_es-001/hesla/mereni_viskozity.html.
- Obr. 2: Archiv autora
- Obr. 3: Archiv autora
- Obr. 4: Archiv autora
- Obr. 5: Archiv autora
- Obr. 6: Archiv autora
- Obr. 7: Archiv autora
- Obr. 8: Archiv autora








