Nitrily karboxylových kyselin 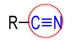
Nitrily jsou organické sloučeniny, které ve svých molekulách obsahují funkční skupinu -C≡ N.
Názvosloví
Systematický název
Základ je odvozen od názvu kyseliny (latinský nebo systematický) + (-di) nitril, např. akrylonitril CH2=CH-C≡N.
Radikálový způsob
Tvoří se spojením: alkyl + kyanid, např. ethylenkyanid CH2=CH-C≡N.
Opisný název
Tvoří se slovem nitril a 2.pádem názvu kyseliny, např. CH2=CH-C≡N nitril kyseliny akrylové.
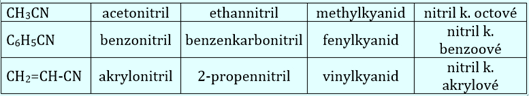
Tab. 1: Názvy nitrilů
Vlastnosti
Nižší nitrily jsou kapaliny často příjemné vůně, vyšší jsou krystalické látky. Mají nižší teplotu varu než příslušné kyseliny i amidy. Jsou dobře rozpustné ve vodě, často se jedná o jedovaté látky.
Reakce
Hydrolýza probíhá alkalická nebo kyselá, podle reakčních podmínek vznikají amidy nebo i samotné kyseliny:
R-C≡N + H2O → RCONH2 → RCOOH + NH3
Redukce nitrilů probíhá za přítomnoti katalyzátorů vodíkem (Raneyův Ni, Co) nebo LiAlH4, vzníkají primární alifatické i aromatické aminy; průmyslově významná je redukce dinitrilu kysliny adipové na hexamethylendiamin:
N≡C-(CH2)4-C≡N + 4H2 → NH2-CH2-(CH2)4-CH2-NH2
Příprava
Katalytická dehydratace amidů - jako katalyzátor se používá především P2O5,dále AlPO4, SOCl2.
R – CO – NH2 → R – C≡N + H2O
Reakcí primárních nebo sekundárních alkylhalogenidů s kyanidy alkalických kovů.
C2H5-Br + KCN →C2H5-CN + KBr
Speciální výrobní postupy
Sandmayerova reakce (diazoniová sůl + kyanid)
Ar-N+ ≡NCl - + KCN → Ar-C≡N + N2 + KCl
Amoxidace methanu na platinovém katalyzátoru za vysokých teplot vede ke vzniku kyanovodíku.
CH4 + NH3 + 3/2 O2 → H - C≡N + 3 H2O
Amoxidací propylenu za podobných podmínek vzniká akrylonitril.
CH2 = CH - CH3 + NH3 + 3/2 O2 → CH2 = CH - C≡N + 3 H2O
Adicí kyanovodíku na butadien vzniká dinitriladipát.
CH2 = CH -CH = CH2 + 2 HCN → N≡C-(CH2)4-C≡N + 3 H2O
Použití
Slouží jako výchozí látky k přípravě karboxylových kyselin a jejich funkčních derivátů. Mezi průmyslově nejvýznamnější nitrily patří kyanovodík a akrylonitril.
Kyanovodík HC≡N je vysoce toxická, bezbarvá, těkavá kapalina (25,7°C) s vůní po hořkých mandlích. Ve vodě se rozpouští, vzniká slabá kyselina kyanovodíková. Anorganické soli se nazývají kyanidy, kyanid draselný se nazývá cyankali. Kyanovodík se vyrábí katalytickou amoxidací methanu, jako katalyzátor se používá platina, reakce probíhá při teplotách nad 1000°C
CH4 + NH3 + 3/2O2 → HC≡N + 3 H2O
Používá se pro organické syntézy, k získávání drahých kovů (kyanidování).
Acetonitril (methylkyanid) CH3C≡N je kapalina s příjemnou vůní, používá se jako rozpouštědlo, k výrobě léčiv.
Akrylonitril CH2=CH-C≡N je bezbarvá jedovatá kapalina, vyráběl se adicí na ethyn, moderně amoxidací propenu. Používá se k výrobě polymeru PAN (polyakrylonitrilu), který se používá k výrobě syntetických vláken.
Zdroje
- WIKIPEDIA.ORG. [online]. [cit. 2014-4-19]. Dostupné z: http://cs.wikipedia.org/wiki/Cyklon_B
Obrázky
- Obr. 1: COMMONS.WIKIMEDIA.ORG. CyklonB [online]. 31.1. 2006 [cit. 29.10.2014]. Dostupné z: http://commons.wikimedia.org/wiki/File:CyklonB.jpg
- Obr. 2: KNIŽNÍ KLUB 2013. Cyankáli v šampaňském [online]. [cit. 26.12. 2014]. Dostupné z: http://www.agatha.cz/dilo/roman/cyankali-v-sampanskem
Kontrolní otázka
Navrhni 2 rozdílné přípravy acetonitrilu
děje zapiš rovnicí.
Znázorni hydrolýzu nitrilu kyseliny benzoové
děj zapiš rovnicí.
Procvič si
Znázorni rovnicí vznik polyakrylonitrilu.
Historie

Obr. 1: Cyklon B
Cyklon B
byl původně název insekticidu vyráběného německou firmou IG Farben jako dezinfekční a dezinsekční činidlo. Po chemické stránce se jednalo o granulovanou křemelinu, která byla nasycená kyanovodíkem. Po otevření obalu se začal uvolňovat plynný kyanovodík.
Za druhé světové války (od r. 1941) byl používán k hromadnému vyvražďování vězňů v plynových komorách, hlavně v táborech Auschwitz-Birkenau a Majdanek. (1)






