Síra, sulfur, 16S
Síra se vyskytuje v přírodě buď volná v blízkosti sopek a sirných pramenů, nebo vázaná v minerálech.
Ze skupiny sulfidů je to např. pyrit FeS2, chalkopyrit CuFeS2, chalkosin Cu2S, galenit (leštěnec olověný) PbS, sfalerit (blejno zinkové) ZnS, cinabarit (rumělka) HgS.
Ze síranů jsou nejznámější baryt (těživec) BaSO4, sádrovec CaSO4 ∙ 2 H2O, Glauberova sůl Na2SO4 ∙ 10 H2O.
Síra je biogenní prvek, je součástí bílkovin.
Získává se vytavováním – síra se přehřátou vodní párou roztaví, tavenina se vytlačuje na povrch teplým stlačeným vzduchem.
Vlastnosti
Síra se vyskytuje v několika alotropických modifikacích (krystalových strukturách). Alotropie je výskyt prvku v několika krystalových strukturách v závislosti na vnějších podmínkách.
Za obyčejné teploty síra krystalizuje v kosočtverečné soustavě, při zahřátí nad 96 °C přechází na soustavu jednoklonnou. Nad 119 °C síra kapalní, dalším zahříváním houstne, hnědne, potom řídne. Vře při 445 °C, vznikají hnědočervené páry, jejichž ochlazením se vytváří sirný květ.
Amorfní modifikace síry jsou sirný květ, který vzniká ochlazením sirných par, a plastická síra, jež vzniká náhlým ochlazením kapalné síry (nalitím roztavené síry do vody). Získaná hmota se dá tvarovat, plasticita je ale jen přechodná.
Krystalická síra tvoří cyklické osmiatomové molekuly, jejichž atomy neleží v rovině:
Obr. 1: Molekula síry
Síra je žlutá látka nerozpustná ve vodě, rozpouští se v nepolárních rozpouštědlech (např. v sirouhlíku CS2). Za běžné teploty je stálá, při vyšší teplotě reaguje téměř se všemi prvky (exotermické reakce):
S + O2 → SO2
S + 3 F2 → SF6
Fe + S → FeS
S + 2 Cl2 → SCl4
C + 2 S → CS2
Použití
Síra se využívá k výrobě H2SO4, SO2, CS2, Na2S2O3, siřičitanů, sulfidů, zápalek, přípravků na hubení škůdců na rostlinách, barviv, mastí a při vulkanizaci kaučuku.
Sloučeniny síry
Sulfan H2S vzniká v přírodě rozkladem bílkovin obsahujících síru, je i součástí sopečných plynů, zemního plynu, koksárenského plynu, svítiplynu, vzduchu. Často bývá přítomen v minerálních vodách a zkažených vejcích.
Laboratorně se připravuje reakcí sulfidu železnatého s kyselinou chlorovodíkovou:
FeS + 2 HCl → H2S + FeCl2
Sulfan je bezbarvý po zkažených vejcích páchnoucí prudce jedovatý plyn. Má redukční účinky:
2 HNO3 + 3 H2S → 2 NO + 3 S + 4 H2O
Na vzduchu hoří. Částečnou oxidací vzniká síra a voda:
2 H2S + O2 → 2 S + 2 H2O
Úplná oxidace probíhá podle reakce:
2 H2S + 3 O2 → 2 SO2 + 2 H2O
Způsobuje černání stříbra:
2 Ag + H2S → Ag2S + H2
Ve vodě se rozpouští na sulfanovou vodu, která se používá v analytické chemii ke kvalitativním důkazům kationtů.
Sulfidy jsou binární sloučeniny síry s elektropozitivnějšími prvky. Dělí se na rozpustné ve vodě (Li2S, Na2S, K2S, CaS, SrS, BaS, (NH4)2S) a nerozpustné ve vodě (sulfidy většiny zbývajících kovů).
Rozpustné sulfidy se připravují neutralizací sulfanu hydroxidy:
H2S + 2 KOH → K2S + 2 H2O
nebo redukcí síranů uhlíkem za vyšší teploty:
CaSO4 + 4 C → CaS + 4 CO
Nerozpustné sulfidy se získávají slučováním kovů se sírou:
Fe + S → FeS
Zn + S → ZnS
nebo srážením sulfidovými anionty – roztoky H2S, Na2S a (NH4)2S:
Cu2+ + S2– → CuS
2 Sb3+ + 3 S2– → Sb2S3
Sulfidy za vyšší teploty reagují s kyslíkem, jedná se o tzv. pražení sulfidů:
2 ZnS + 3 O2 → 2 ZnO + 2 SO2
Ag2S + O2 → 2 Ag + SO2
4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2
Tab. 1: Zbarvení sulfidů
|
sulfid |
barva sraženiny |
sulfid |
barva sraženiny |
|
MnS |
růžová |
CdS |
žlutá |
|
FeS |
černá |
Hg2S |
černá |
|
Fe2S3 |
černá |
HgS |
černá |
|
CoS |
černá |
SnS |
hnědá |
|
NiS |
černá |
PbS |
černá |
|
CuS |
černá |
As2S3 |
žlutá |
|
Ag2S |
černá |
Sb2S3 |
oranžová |
|
ZnS |
bílá |
Bi2S3 |
černohnědá |
Oxid siřičitý SO2 se vyskytuje ve vzduchu, kam se dostává jako průmyslový odpadní plyn, který vzniká při spalování látek obsahujících síru. Reakcí s vodní parou a dešťovou vodou pak způsobuje kyselé deště. Je rovněž přítomen v sopečných plynech.
Připravuje se rozkladem siřičitanů kyselinami:
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
hořením sulfanu:
2 H2S + 3 O2 → 2 SO2 + 2 H2O
reakcí mědi s koncentrovanou H2SO4:
Cu + 2 H2SO4 → CuSO4 + SO2 + 2 H2O
Vyrábí se spalováním síry:
S + O2 → SO2
dříve i pražením pyritu:
4 FeS2 + 11 O2 → 8 SO2 + 2 Fe2O3
Oxid siřičitý je bezbarvý plyn štiplavého zápachu, dráždí dýchací cesty, pro nižší organismy je jedovatý.
Má redukční účinky:
Cl2 + SO2 + 2 H2O → 2 HCl + H2SO4
ale i oxidační účinky:
2 H2S + SO2 → 3 S + 2 H2O
V přítomnosti katalyzátoru V2O5 reaguje s kyslíkem:
2 SO2 + O2 → 2 SO3
S vodou vzniká nestálá slabá dvojsytná kyselina siřičitá:
SO2 + H2O → H2SO3
Používá se při výrobě H2SO4, bílení, čištění ropy, ničení mikroorganismů (síření sudů, dezinfekce úlů). Způsobuje kyselé deště.
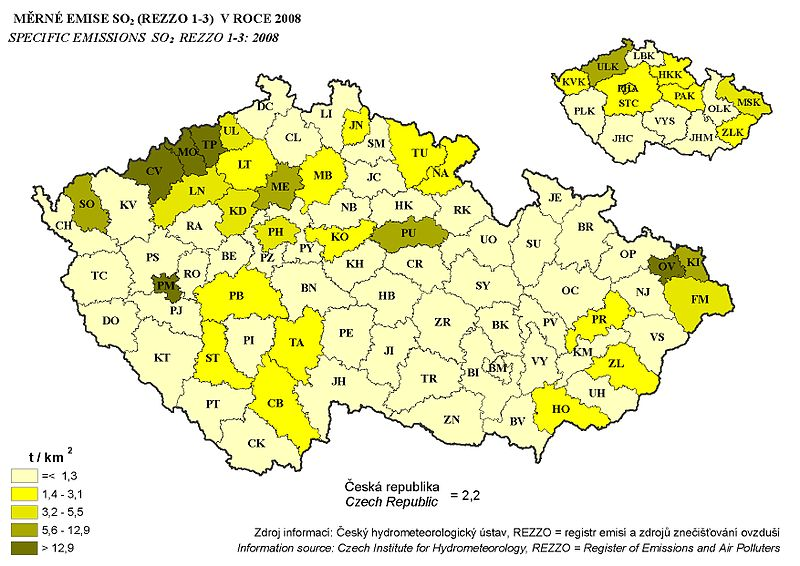
Obr. 2: Měrné emise SO2 v roce 2008
Oxid sírový SO3 se vyrábí reakcí oxidu siřičitého s kyslíkem v přítomnosti katalyzátoru V2O5:
2 SO2 + O2 → 2 SO3
Existuje ve všech třech skupenstvích, v plynném stavu tvoří molekuly SO3, v kapalném a pevném skupenství polymeruje.
S vodou reaguje až explozivně:
SO3 + H2O → H2SO4
Používá se k výrobě H2SO4.
Kyselina sírová H2SO4 se vyrábí následujícími reakcemi:
S + O2 → SO2
2 SO2 + O2 → 2 SO3
SO3 + H2SO4 → H2S2O7 (používaná H2SO4 je zředěná)
H2S2O7 + H2O → 2 H2SO4 (vznikající H2SO4 je koncentrovaná)
Kyselina sírová je silná dvojsytná kyselina, disociuje do dvou stupňů:
H2SO4 ⇄ H+ + HSO4–
HSO4– ⇄ H+ + SO42–
Je to bezbarvá olejovitá hustá kapalina dokonale mísitelná s vodou za vzniku velkého množství tepla. Koncentrovaná kyselina (96-98%) má dehydratační vlastnosti (odnímá látkám vodu) – je hygroskopická:
CuSO4 ∙ 5 H2O → CuSO4 + 5 H2O (změna modré barvy na bílou)
C12H22O11 → 12 C + 11 H2O (změna bílé barvy na černou)
Koncentrovaná má oxidační účinky:
Cu + 2 H2SO4 → CuSO4 + SO2 + 2 H2O
Koncentrovaná nereaguje se železem (pasivuje se), proto se může převážet v ocelových cisternách.
Zředěná nemá oxidační účinky a reaguje jen s kovy vlevo od vodíku v řadě napětí kovů:
Zn + H2SO4 → ZnSO4 + H2
Kyselina sírová je nejdůležitější anorganická kyselina v laboratořích a téměř ve všech odvětvích průmyslu. Používá se k výrobě hnojiv, výbušnin, plastů, barviv a léčiv nebo jako náplň do akumulátorů.
Sírany (sulfáty) jsou soli kyseliny sírové.
Rozlišují se sírany nerozpustné ve vodě (např. PbSO4, Hg2SO4, HgSO4, BaSO4, SrSO4), které se připravují srážením:
Ba2+ + SO42– → BaSO4
Nejméně rozpustný je síran barnatý – toho se využívá při důkazu síranových aniontů:
BaCl2 (aq) + Na2SO4 (aq) → BaSO4 (s) + 2 NaCl (aq)
Další skupinou jsou sírany rozpustné ve vodě, které se připravují neutralizací:
2 KOH + H2SO4 → K2SO4 + 2 H2O
nebo rozpouštěním obecných kovů ve zředěné H2SO4:
Fe + H2SO4 → FeSO4 + H2
nebo rozpouštěním ušlechtilých kovů v koncentrované H2SO4:
Cu + 2H2SO4 → CuSO4 + SO2 + 2 H2O
Můžeme také rozpouštět oxidy, hydroxidy a uhličitany ve zředěné H2SO4:
CuO + H2SO4 → CuSO4 + H2O
Cd(OH)2 + H2SO4 → CdSO4 + 2 H2O
MgCO3 + H2SO4 → MgSO4 + CO2 + H2O
Některé sírany krystalují s vodou – vznikají skalice: modrá skalice CuSO4 ∙ 5 H2O, zelená skalice FeSO4 ∙ 7 H2O, bílá skalice ZnSO4 ∙ 7 H2O. Modrá skalice se používá k dezinfekci bazénů a jako fungicid v zemědělství.


Obr. 3: Modrá skalice Obr. 4: Zelená skalice
Hydrogensírany známe jen od alkalických kovů. Jsou dobře rozpustné ve vodě.
Kamence jsou podvojné sírany prvků s oxidačním číslem I a III např. KCr(SO4)2 ∙ 12H2O dodekahydrát síranu draselnochromitého, KAl(SO4)2 ∙ 12 H2O dodekahydrát síranu draselnohlinitého, NH4Fe(SO4)2 ∙ 12 H2O dodekahydrát síranu amonnoželezitého.
Thiosíran sodný Na2S2O3 obsahuje thiosíranový anion, který se od síranového liší tím, že má jeden z atomů kyslíku nahrazen atomem síry s oxidačním číslem –II. Používá se k odstraňování přebytku chloru z pitné vody a jako ustalovač při vyvolávání černobílých fotografií.
- BÁRTA, Milan. Chemické prvky kolem nás. 1. vydání. Brno: Edika, 2012. 112s. ISBN 978-80-266-0097-8.
- BENEŠOVÁ, Marika a Hana SATRANOVÁ. Odmaturuj z chemie. 1.vydání. Brno: Didaktis, 2002. 208 s. ISBN 80-86285-56-1.
- DVOŘÁČKOVÁ, Svatava. Rychlokurz chemie. 1. vydání. Olomouc: Rubico, 2000. 238 s. ISBN 80-85839-42-3.
- FLEMR, Vratislav a Bohuslav DUŠEK. Chemie I/Obecná a anorganická. 1. vydání. Praha: SPN, 2001. 120 s. ISBN 80-7235-147-8.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie I v kostce. 1. vydání. Havlíčkův Brod: Fragment, 1996. 120 stran. ISBN 80-7200-056-X.
- ŠRÁMEK, Vratislav a Ludvík KOSINA. Obecná a anorganická chemie. 1. vydání. Olomouc: FIN, 1996. 262 stran. ISBN 80-7182-003-2.
Obrázky
- Obr. 1: Archív autora.
- Obr. 2: Neznámý autor. commons.wikimedia.org [online]. [cit. 2014-3-20]. Dostupný na www: http://commons.wikimedia.org/wiki/File:130310m22.jpg?uselang=cs.
- Obr. 3: Dohnálek, Petr Adam. commons.wikimedia.org [online]. [cit. 2014-10-18]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Cupri_sulfas_pentahydricus_-001-.jpg?uselang=cs.
- Obr. 4: Leiem. commons.wikimedia.org [online]. [cit. 2014-10-18]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Iron%28II%29_sulfate_heptahydrate.JPG?uselang=cs.
- Obr. 5: Descouens, Didier. commons.wikimedia.org [online]. [cit. 2014-5-10]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Soufresicile2.jpg?uselang=cs.
- Obr. 6: Radtke, Christoph. commons.wikimedia.org [online]. [cit. 2014-3-24]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Pyrit_1.jpg?uselang=cs.
- Obr. 7: Karelj. commons.wikimedia.org [online]. [cit. 2014-3-24]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Galenit_4.jpg?uselang=cs.
- Obr.8: Weetzig, Elke. commons.wikimedia.org [online]. [cit. 2014-5-10]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Chalkopyrit_mineralogisches_museum_bonn.jpg?uselang=cs.
- Obr. 9: Karelj. commons.wikimedia.org [online]. [cit. 2014-5-10]. Dostupný na www: http://upload.wikimedia.org/wikipedia/commons/d/dc/Sfalerit_1.jpg?uselang=cs.
- Obr. 10: Géry, Parent. commons.wikimedia.org [online]. [cit. 2014-5-10]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Cinabre_1.JPG.
- Obr. 11: Lavinsky, Rob. commons.wikimedia.org [online]. [cit. 2014-3-24]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Alstonite-Baryte-216041.jpg.
- Obr. 12: Khruner. commons.wikimedia.org [online]. [cit. 2014-10-18]. Dostupný na www: http://commons.wikimedia.org/wiki/File:Mineral_-_Selenite_by_Khruner.png?uselang=cs.
„Sírou to smrdí v pekle.“ Síra až tolik nezapáchá, ale její sloučeniny jsou v tomto oboru mistry. Sulfan (postaru sirovodík) je plyn, na který je náš čich ze všech nejcitlivější. Uvolňuje se například při rozkladu bílkovin, když se kazí vejce nebo maso. Může za zápach, kterým zamoříme okolí, když provedeme flatulenci (prdneme si). Sloučeniny síry mohou za zápach z úst. Sloučeninami síry značkujeme zemní plyn, abychom se včas dověděli o jeho úniku. Charakteristický zápach má oxid siřičitý vznikající při hoření síry. To bude zřejmě plyn, se kterým má řada z nás spojené peklo.
Který minerál obsahuje více síry - baryt nebo sádrovec?
Mr(BaSO4) = 233,4; Mr(CaSO4 ∙ 2 H2O) = 172,1;
Ar(S) = 32,1
Výsledek:
baryt 13,75 %, sádrovec 18,65 %